РОЗДІЛ 4
ЛІКУВАННЯ ХВОРИХ НА АКНЕ
4.1 Методика лікування
Використання системних ретиноїдів для лікування середньотяжких та тяжких форм акне стало ключовою подією в еволюції терапевтичних підходів при цьому захворюванні. Їх вплив на різні ланки патогенезу акне дозволив одержати терапевтичний ефект, що не був досягнутий будь-яким іншим методом лікування.
Однією із задач дослідження було оцінити та довести ефективність одного із запропонованих методів комплексного лікування хворих на тяжкі та середньотяжкі форми акне. Три терапевтичні групи (61 пацієнт) отримали такі види терапії: перша група (20 пацієнтів) – системні ретиноїди та системні антибіотики, друга група (20 пацієнтів) – системні ретиноїди та топічні антибактеріальні засоби, третя група (21 пацієнт) – системні ретиноїди.
Із сучасних препаратів групи системних ретиноїдів було обрано «Акнетін», тому що він був створений за спеціальною технологією, яка підвищує біодоступність. Акнетін призначали при акне середньої тяжкості по 0,4 мг/кг з подальшим зниженням дози, починаючи з третього місяця на 8 мг. Тяжкі форми акне лікувалися «Акнетіном» у дозі 0,4 мг/кг впродовж 4–5 місяців з подальшим зниженням дози. Лікування тривало 6-7 місяців.
Вибір системного та топічного антибактеріального засобу було зроблено, враховуючи дані про чутливість мікроорганізмів під час проведення мікробіологічного дослідження.
Системний антибіотик з групи тетрациклінів «Юнідокс солютаб» (по 100 мг 2 рази на добу протягом 14 днів) з подальшим призначенням «Акнетіну» застосовувався в першій групі пацієнтам, що мали велику площу гнійного запалення, раніше не приймали препарати цього ряду або довго застосовували антибактеріальні засоби топічно.
У другій групі, тим пацієнтам, що в анамнезі мали прийом системних антибіотиків упродовж 6 місяців або мали протипоказання до них, було призначено топічний антибактеріальній засіб «Фузідерм» гель на ділянки висипу 3 рази на добу впродовж місяця в комбінації із системними ретиноїдами («Акнетін»).
Третя група отримувала системні ретиноїди – «Акнетін» у зазначених раніше дозуваннях.
Динаміка регресу елементів висипу оцінювалася кожний місяць терапії, зіставляючи регрес вузлів, папуло-пустул та комедонів у різних терапевтичних групах.
4.2 Динаміка регресу клінічних проявів дерматозу
Кількість вузлів у першій групі до лікування була 17,5±1,06, після першого місяця лікування – 7,83±0,61, після другого місяця лікування – 1,72±0,37, після третього місяця – 0,17±0,12, після четвертого місяця жодного вузла не спостерігалося (табл. 4.1, рис. 4.1).
Кількість вузлів зменшується повільніше при застосуванні комбінації системних ретиноїдів та топічних антибіотиків, ніж при інших схемах лікування, але на третьому місяці кількість вузлів стала однаковою для всіх терапевтичних груп, що свідчить про те, що незалежно від виду комплексної терапії, але при наявності у ній системних ретиноїдів спостерігався регрес гострозапальних елементів висипу.
До лікування спостерігалося у середньому (36,11±3,79) папуло-пустул, після першого місяця лікування – 17,89±1,79, після другого місяця лікування – 6,28±1,04, після третього місяця – 1,72±0,42, після четвертого місяця – 0,17±0,12, після п’ятого місяця терапії – 0,11±0,08 (рис. 4.2).
Таблиця 4.1 – Динаміка кількості елементів висипу при застосуванні різних терапевтичних схем
| Групи хворих | Термін спостереження | ||||||
| До лікування | 1 міс. | 2 міс. | 3 міс. | 4 міс. | 5 міс. | ||
| Вузли (M±m) | |||||||
| I
(n=18) |
17,5 ±1,06 # |
7,83 ±0,61* |
1,72 ±0,37* |
0,17 ±0,12* |
0 | 0 | |
| II
(n=18) |
14,44 ±0,71 |
9,89 ±0,7 *# |
4,0 ±0,78 *# |
0,44 ±0,18* |
0 | 0 | |
| III
(n=20) |
13,35 ±1,3 |
6,25 ±0,7*# |
2,1 ±0,57* |
0,3 ±0,11 * |
0,05 ±0,05* |
0 | |
| Папуло-пустули (M±m) | |||||||
| I
(n=18) |
36,11 ±3,79 |
17,89 ±1,79* |
6,28 ±1,04* |
1,72 ±0,42* |
0,17 ±0,12* |
0,11 ±0,08 |
|
| II
(n=18) |
34,06 ± 2,43 |
18,33 ±2,1 * |
4,72 ±0,9 * |
0,94 ±0,38* |
0,11 ±0,08* |
0,06 ±0,06 |
|
| III
(n=20) |
42,2 ±3,51 |
28,0 ±2,97*# |
11,6 ±1,98*# |
3,25 ±1,06* |
0,4 ±0,2 * |
0,2 ±0,09 |
|
| Комедони (M±m) | |||||||
| I
(n=18) |
72,0±3,8 | 40,39±3,0* | 13,44±1,46* | 2,27±0,74* | 0,06±0,06 * | 0 | |
| II
(n=18) |
103,1±9,4 # | 59,9±7,68* | 21,11±4,15* | 6,22±1,98* | 0,67±0,42 * | 0,11±0,11* | |
| III
(n=20) |
88,7±6,7 | 67±5,76 * | 37,2±4,3 *# | 13,25±2*# | 3,75±1,23 *# | 1,55±0,68 | |
Примітка. * – значимо (р<0,05) менше порівняно з попереднім значенням; # – значимо (р<0,05) відрізняється від показника в інших групах у той самий термін лікування.
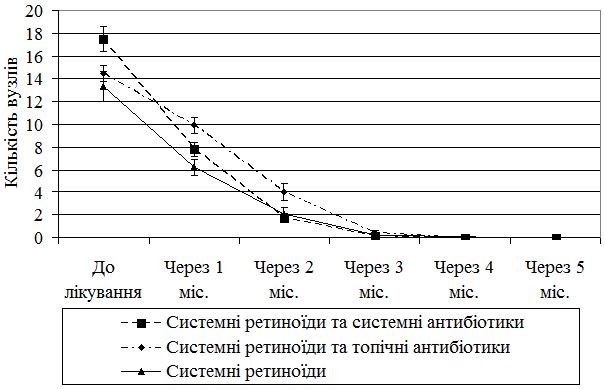
Рисунок 4.1 – Динаміка регресу вузлів у трьох групах спостереження.
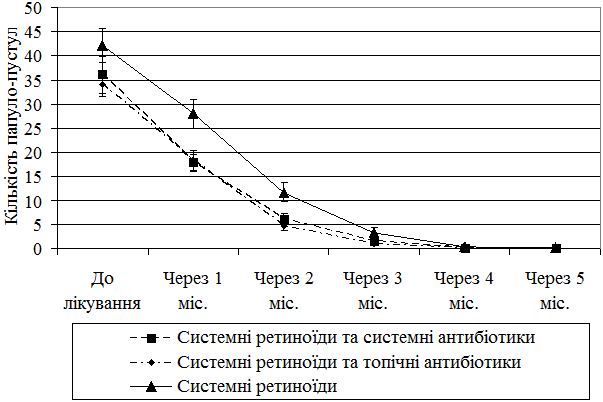
Рисунок 4.2 – Динаміка регресу папуло-пустул у трьох групах спостереження.
Кількість комедонів у першій групі до лікування склала 103,1±9,4, після першого місяця лікування – 59,9±7,68, після другого місяця – 21,11±4,15, після третього місяця – 6,22±1,98, після четвертого місяця – 0,67±0,42, після п’ятого місяця – 0,11±0,11 (рис. 4.3).
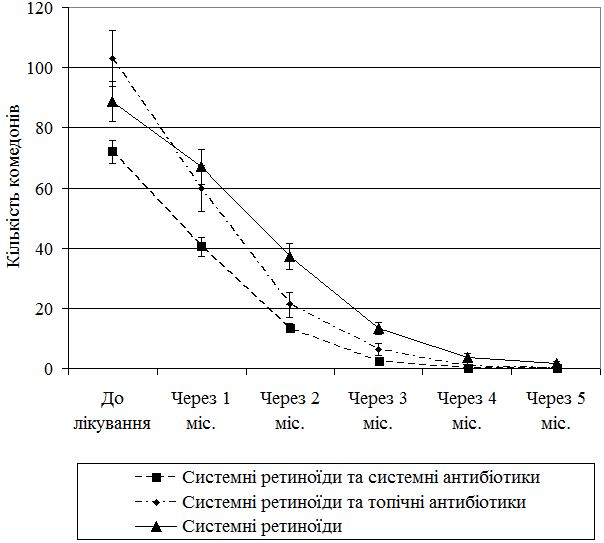
Рисунок 4.3 – Динаміка регресу кількості комедонів у трьох групах спостереження.
Кількість вузлів у другій групі до лікування була в середньому 14,44±0,71, після першого місяця лікування – 9,89±0,7, після другого місяця – 4,0±0,78, після третього місяця – 0,44±0,18, після четвертого місяця вузли не спостерігалися.
У другій групі до лікування у середньому спостерігалося 34,06±2,43 папуло-пустул, після першого місяця лікування – 18,33±2,1, після другого місяця – 4,72±0,9, після третього місяця – 0,94±0,38, після четвертого місяця – 0,11±0,08, після п’ятого місяця – 0,06±0,06.
У середньому динаміка регресу папуло-пустул у перший місяць терапії демонструвала зменшення в середньому в два рази в першій та другій терапевтичних групах. У випадку застосування системних ретиноїдів та топічної антибактеріальної терапії спостерігався більш швидкий регрес папуло-пустульозних елементів, що також у динаміці підтверджувалося мікробіологічними дослідженнями.
Кількість комедонів у другій групі до лікування становила 72,0±3,8, після першого місяця лікування – 40,39±3,0, після другого місяця – 13,44±1,46, після третього місяця – 2,27±0,74, після четвертого місяця – 0,06±0,06, після п’ятого місяця комедони не виявлялися.
Кількість вузлів у третій групі до лікування була 13,35±1,3, після першого місяця лікування – 6,25±0,7, після другого місяця – 2,1±0,57, після третього місяця – 0,3±0,11, після четвертого місяця – 0,05±0,05, після п’ятого місяця терапії вузли не спостерігалися.
У третій групі до лікування спостерігалося 42,2±3,51 папуло-пустул, після першого місяця лікування – 28,0±2,97, після другого місяця – 11,6±1,98, після третього місяця – 3,25±1,06, після четвертого місяця – 0,4±0,2, після п’ятого місяця терапії – 0,2±0,09.
Кількість комедонів у третій групі до лікування становила 88,7±6,7, після першого місяця лікування – 67±5,76, після другого місяця – 37,2±4,3, після третього місяця – 13,25±2,0, після четвертого місяця – 3,75±1,23, після п’ятого місяця – 1,55±0,68. Регрес комедонів був поступовим та повільним у всіх групах спостереження, що свідчило про системну дію ретиноїдів на процеси салоутворення та саловиділення.
4.3 Клінічні випадки з груп спостереження
Клінічні випадки, які були розглянуто в розділі клінічний опис, мають безпосереднє відношення до розділу «лікування», тому що всі ці пацієнти, результати лікування яких буде представлено нижче, отримували патогенетичну терапію та входили в одну з терапевтичних груп дослідження.
Пацієнт Т., 23 роки. В анамнезі стимуляція розвитку соматотропным гормоном. Діагноз: акне тяжкого ступеня (рис. 4.4 і 4.5).
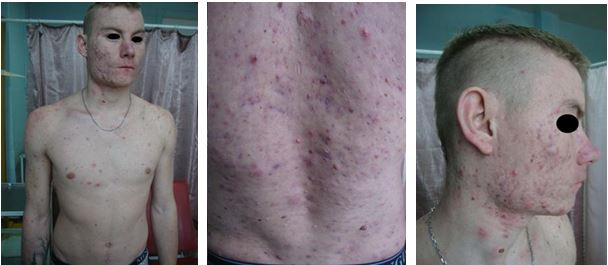
Рисунок 4.4 – Пацієнт Т., 23 роки. В анамнезі стимуляція розвитку соматотропним гормоном. Діагноз: акне тяжкого ступеня. До лікування.
Після обстеження та виключення протипоказань до терапії йому було призначено: «Юнідокс солютаб» по 100 мг 2 рази на добу протягом 10 діб (з урахуванням анамнестичних даних, що в останнє він отримував системний антибактеріальний препарат роду цефалоспоринів півроку тому), «Акнетін» по 0,4 мг/кг/добу протягом 5 місяців, емолієнти, фотозахисний крем, репаруючий стік для губ «Cicaplast».
Особливість випадку полягає в анамнестичних даних, а також у торпідному перебігу дерматозу: кількість гострозапальних елементів висипу на тулубі зменшувалася на багато повільніше, ніж на шкірі обличчя.
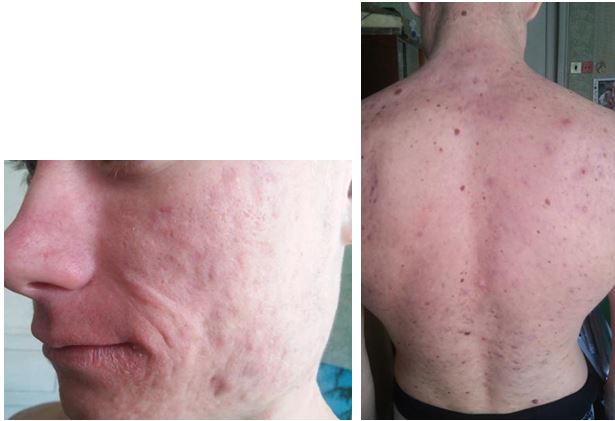
Рисунок 4.5 – Пацієнт Т., 23 роки, після проведеного лікування.
Клінічний випадок пацієнта Д., 14 років, частково (анамнез та скарги до лікування) описано у розділі «клінічна характеристика хворих» (рис. 4.6).
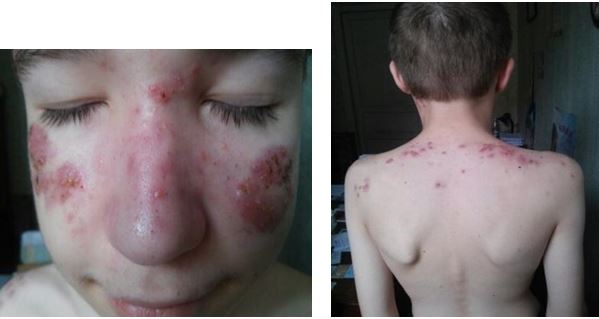
Рисунок 4.6 – Пацієнт Д.,14 років – до лікування.
Діагноз: акне тяжкого ступеня. Був обстежений загальноклінічно: патологічних відхилень і протипоказань до терапії системними ретиноїдами немає.
Було призначено терапію у вигляді системних ретиноїдів («Акнетін» по 16 мг на добу протягом 4 місяців) та топічних антибактеріальних засобів («Фузідерм» гель 3 рази на добу).
Наприкінці третього місяця терапії спостерігався значний регрес вузлів на обличчі та повністю було припинено процес формування пустульозних елементів на шкірі тулуба (рис. 4.7).
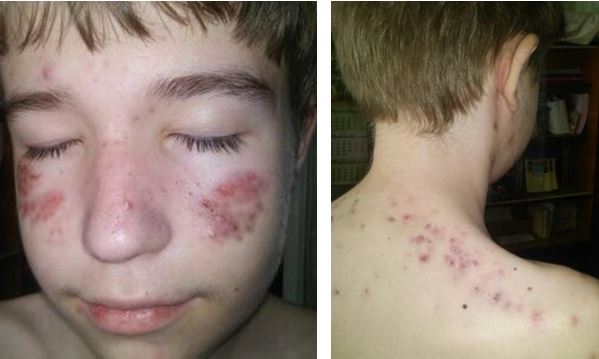
Рисунок 4.7 – Пацієнт Д.,14 років, у процесі терапії.
У результаті проведеної терапії можна зазначити повний регрес гострозапальних елементів висипки, формування нормотрофічних рубців (рис. 4.8).
Пацієнт Л., 33 роки, був обстежений загальноклінічно: патологічних відхилень і протипоказань до терапії не було. При обстеженні органів малого тазу виявлено хронічний простатит.
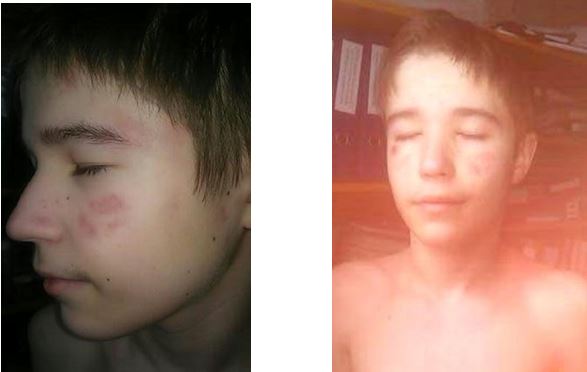
Рисунок 4.8 – Пацієнт Д., 14 років – після проведеноі терапії.
Діагноз: акне тяжкого ступеня. Підриваючий фолікуліт Гоффмана.
До лікування у пацієнта спостерігався виражений гнійний процес. Було призначено системні антибіотики та системні ретиноїди (рис. 4.9).
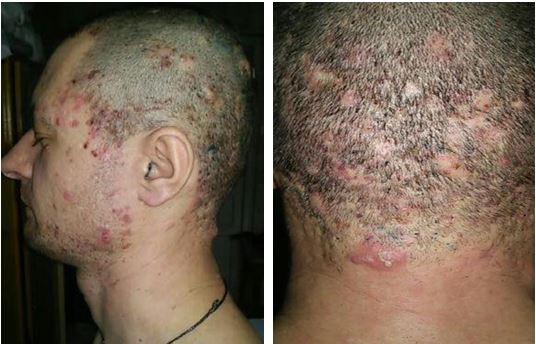
Рисунок 4.9 – Пацієнт Л., 33 роки, до лікування.
У процесі терапії (через 2 місяці після її початку) спостерігалося сплощення гострозапальних елементів на волосистій частині голови, наростаюча сухість шкірних покривів обличчя (рис. 4.10).
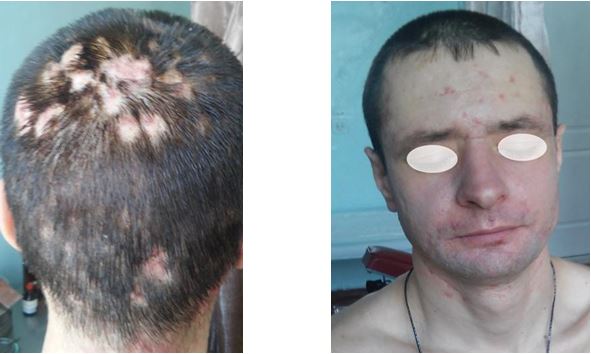
Рисунок 4.10 – Пацієнт Л., 33 роки, у процесі лікування.
Після проведеного лікування нових гострозапальних елементів висипки не спостерігалося, поновилося зростання волосся на місцях, де раніше були інфільтрати. Пацієнт отримував також підтримуючу терапію (рис. 4.11).
Анамнез наступного пацієнта також описано в клінічній характеристиці – С., 22 роки, встановлено діагноз: акне тяжкого ступеня, індукований прийомом «спортивного харчування» (рис. 4.12). Отримав терапію: системні ретиноїди «Акнетін» 32мг на добу, зовнішньо антибактеріальні засоби. При виборі антибактеріального засобу було прийнято до уваги дані анамнезу: пацієнт два місяці тому приймав системні антибактеріальні засоби. Обов’язково було наголошено на відміні прийому «спортивного харчування».
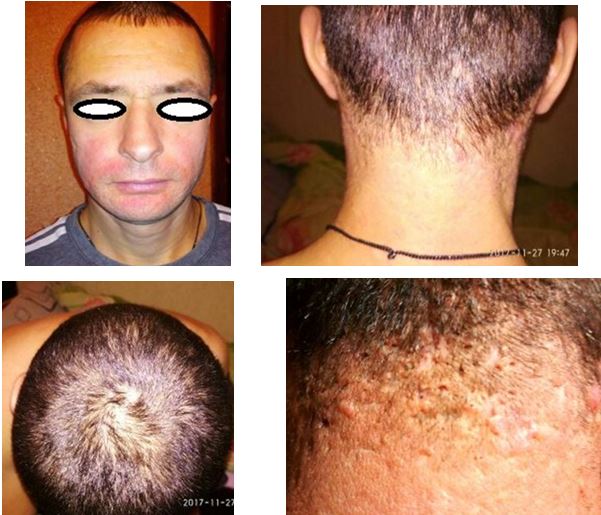
Рисунок 4.11 – Пацієнт Л., 33 роки, після проведеного лікування.
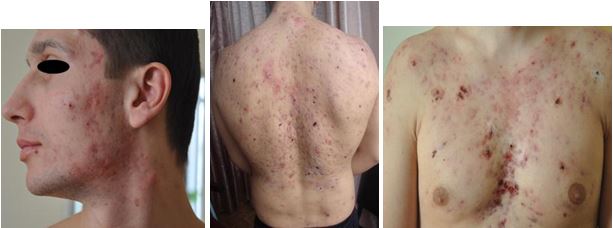
Рисунок 4.12 – Пацієнт С., 22 роки, до терапії.
Регрес елементів висипу на обличчі спостерігався в кінці другого місяця терапії. На тулубі регрес гострозапальних елементів акне був повільнішим, особливо на ділянках, що були ерозовані. Особливістю випадку також був хвилеподібний перебіг акне, що можливо обумовлений вживанням гормональних стимуляторів у «спортивному харчуванні». Після проведеної терапії пацієнт знаходився в ремісії близько року, після чого знову почав прийом «спортивного харчування» і наголосив на посиленні саловиділення та появі нових гнійних елементів (рис. 4.13). Був пролікований повторно та отримав підтримуючу терапію.
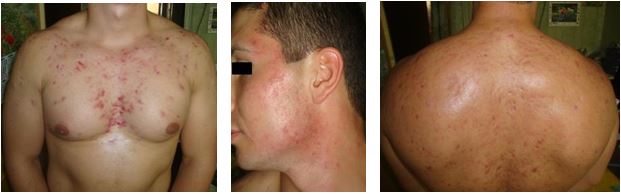
Рисунок 4.13 – Пацієнт С., 22 роки. Після терапії.
У випадку акне, спровокованого курсом масажу, у пацієнтки після обстеження було призначено «Акнетін» по 16 мг на добу, фотозахисний крем та емолієнти (рис. 4.14 і 4.15).
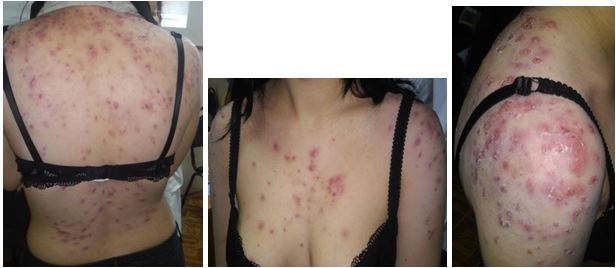
Рисунок 4.14 – Пацієнтка Г., 31 рік, акне тяжкого ступеня, до лікування.
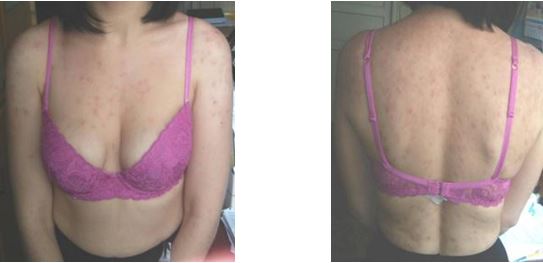
Рисунок 4.15 – Пацієнтка Г., 31 рік, після проведеної терапії.
Особливість випадку полягає в тому, що висип локалізувався лише на шкірі тулуба ( там, де максимально був спричинений механічний та хімічний вплив на шкіру під час масажу), був представлений великими папуло-пустульозними елементами, які повністю регресували до початку 4-го місяця без застосування антибактеріальної терапії.
Наступний клінічний випадок було описано частково в клінічному огляді: хворий А., 18 років, який провокував загострення дерматозу самостійно: прикладав до обличчя гарячі компреси (рис. 4.16). Після обстеження та виключення протипоказань хворому було призначено системні ретиноїди по 32 мг на добу 5 місяців та зовнішньо фотозахисні засоби і емолієнти. Регрес гострозапальних елементів був достатньо швидким: вже наприкінці першого місяця гіперемія зменшилася в рази, були відсутні гнійні кірки та процес утворення нових елементів було майже припинено.
Наступна пацієнтка мала в анамнезі довготривалий прийом доксицикліну та іі анамнез описано у клінічному огляді (рис. 4.17, 4.18). Враховуючи це, їй було призначено системні ретиноїди («Акнетін» по 24 мг на добу з подальшим зниженням дози). Цей випадок характеризувався складним анамнезом та значною психоемоційною лабільністю пацієнтки: вона виказувала недовіру дії препарату та методу лікування. Регрес гострозапальних елементів висипу було досягнуто на другому місяці терапії. Ефект від проведеної терапії дуже позитивно вплинув на іі самооцінку та психоемоційний стан.
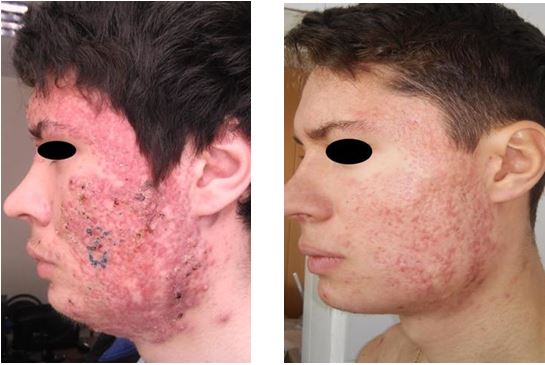
Рисунок 4.16 – Хворий А., 18 років, акне тяжкого ступеня.
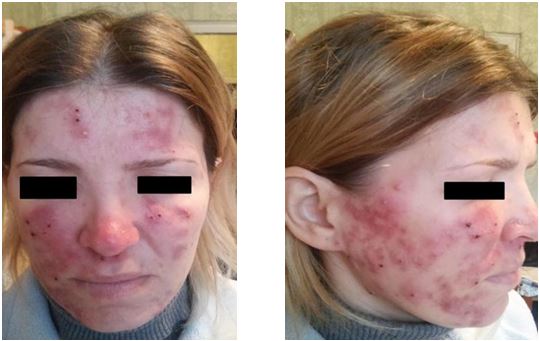
Рисунок 4.17 – Пацієнтка Н., 33 роки. До терапії.
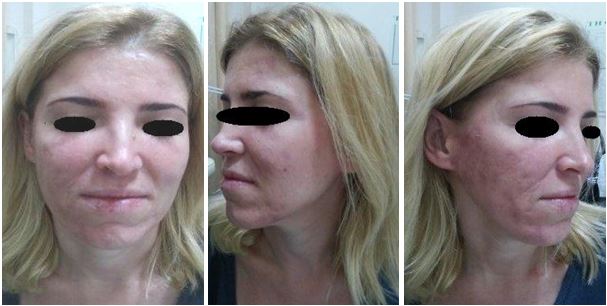
Рисунок 4.18 – Пацієнтка Н., 33 роки, після проведеної терапії.
4.4 Підтримуюча терапія
При тяжких формах акне у пацієнтів, що мали спадковість, ранній дебют дерматозу, малу ефективність лікування в минулому, застосовувалася підтримуюча терапія, під час якої хворі отримували Акнетін по 8 мг щоденно протягом 2-4 тижнів (у середньому 1 місяць), потім по 8 мг через день протягом 2-4 тижнів, потім по 8 мг 1 раз на три дні протягом 2–4 тижнів і нарешті по 8 мг 1 раз на тиждень протягом 1 місяця.
Підтримуючу терапію отримали 17 пацієнтів, під час якої спостерігалася стійка ремісія. Поодинокі елементи висипу з’являлися у 3 пацієнтів. Їх появу вони пов’язували з переохолодженням або зловживанням солодощами.
4.5 Косметологічний супровід пацієнтів під час терапії системними ретиноїдами
Під час проведення терапії системними ретиноїдами у трьох групах спостереження пацієнтам було рекомендовано застосування емолієнтів, фотозахисних та репаруючих засобів. Хворі щоденно застосовували фотозахисний крем комфорт «Anthelios 50+» на всі відкриті ділянки шкіри (з обов’язковою умовою поновлення впродовж дня, якщо пацієнт пітнів або приймав душ), для слизової губ застосовували залежно від сезону два стики: взимку «Cicaplast» губи, який має посилений репаруючий ефект за рахунок провітаміну В5, а в сезони, що характеризувалися більш активною інсоляцією, призначався стік «Аnthеlios», який мав фотозахисний ефект.
«Effaclar H» – гідратуючий крем, що був створений спеціально для хворих на акне, які отримують лікування, що супроводжується сухістю шкіри, застосовувався впродовж дня на шкіру обличчя за потребою. У разі якщо наростаюча сухість шкіри рук завдавала дискомфортних почуттів (частіше спостерігалося у жінок, які часто контактують з водою та хімічними засобами), призначався крем «Cicaplast» руки – за потребою. Якщо спостерігалася виражена сухість шкіри тіла, призначався миючий засіб та бальзам «Lipicar».
У пацієнтів, які отримували системні ретиноїди, для профілактики носових кровотеч та кон’юнктивітів призначалися зволожуючі засоби для слизових за показаннями. Для слизової носу застосовувалися «Аква Маріс» з декспантенолом 3-4 рази на день, а для очей – очні краплі «Оптінол» з гіалуроновою кислотою 2-3 рази на день. Також під час лікування було рекомендовано шампунь «Vichy» для чутливої шкіри голови.
Враховуючи стан шкіри під час лікування системними ретиноїдами, пацієнтам було надано рекомендації виключити з косметологічного догляду всі види косметичних процедур, що мають температурну, опромінюючу або відлущувальну дію, а саме: лазерну та воскову епіляцію, пілінги, скрабування, маски з підсушуючим ефектом, відвідування лазні, солярію, засмагання.
4.6 Комплаєнтність хворих на акне та її взаємозв’язок з ефективністю терапії
Під час терапії спостерігалося зниження комплаєнтності хворих на акне, які отримували системні ретиноїди, а саме було констатовано випадки ретиноїдного дерматиту у 14 пацієнтів, ретиноїдного ангуліту у 9 пацієнтів та підвищення трансаміназ, загального холестерину або загального білірубіну у 12 пацієнтів, що обумовлювало порушення, або недотримання рекомендацій щодо дієти та косметичного догляду під час прийому системних ретиноїдів.
У пацієнтів зі змінами у біохімічному аналізі крові було виявлено порушення дієти, а саме зловживання алкоголем, вживання багато жирної їжі, 1 пацієнт приймав полівітамінний комплекс із вмістом вітаміну А без відома лікуючого лікаря та незважаючи на те, що йому були надані рекомендації. Серед пацієнтів, що мали ці зрушення, переважали студентів, які зловживали «фастфудом» або вживали багато випічки на основі трансжирів. Треба зазначити, що під час терапії пацієнти з акне, які отримували системні ретиноїди, проходили щомісячний контроль біохімічних показників та ліпідограми, тобто було здійснено постійний моніторинг змін цих показників. Це дозволяло виявляти ці зрушення, а також контролювати зворотні зміни. Для корекції підвищених показників призначався гепатопротектор «Антраль» по 0,2 мг 3 рази на добу впродовж місяця, корекція дози системних ретиноїдів не проводилася.
У пацієнтів, які мали такі ускладнення терапії, як ретиноїдний дерматит або ретиноїдний ангуліт чи хейліт, спостерігалося нехтування рекомендаціями щодо косметичного догляду шкіри під час лікування системними ретиноїдами: вони забували або не поновлювали фотозахисний крем протягом дня на відкритих ділянках шкіри, не зволожували шкіру та слизові, не вважаючи це важливим компонентом профілактики ускладнень. Пацієнтка пред’являла скарги на періодичний свербіж, висипку, локалізовану на відкритих ділянках шкіри рук (рис. 4.19).
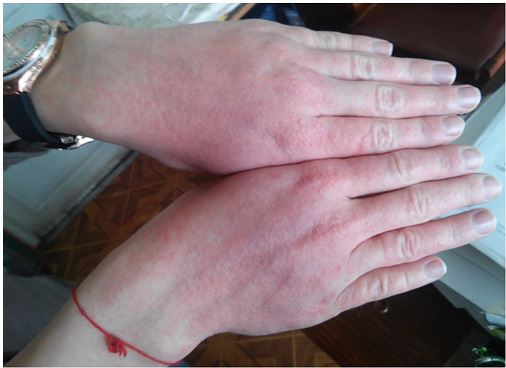
Рисунок 4.19 – Ретиноїдний дерматит шкіри рук у пацієнтки з акне, що отримувала системні ретиноїди та не дотримувалася рекомендацій щодо нанесення та поновлення фотозахисного крему впродовж дня.
У випадках появи ретиноїдного дерматиту пацієнтам нагадували та знову наголошували на дотриманні рекомендацій щодо догляду за шкірою під час лікування та симптоматично призначали «Цетрин» по 1 таблетці 1 раз на добу впродовж 10 днів, інтенсивний зволожуючий та фотозахисний догляд. Зниження дози системних ретиноїдів у таких випадках не проводилося та було досягнуто позитивний терапевтичний ефект.
Один пацієнт не дотримувався рекомендацій щодо профілактики ускладнень, а саме не застосовував зволожуючі засоби для слизової губ. Звернувся зі скаргами на болісність під час розмови, сухість періоральної ділянки, тріщини та кірки (рис. 4.20). Було призначено репаруючий стік «Cicaplast» та мазь «Банеоцин» 3 рази на добу протягом 7 днів. Вибір антибактеріального засобу в даному випадку залежав не стільки від вимог до антибактеріального компоненту, скільки до основи лікарського засобу: в «Банеоцині» основа – гліцерин, який має пом’якшувальну дію.
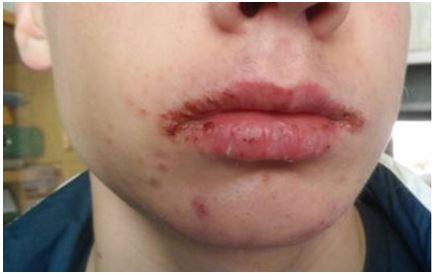
Рисунок 4.20 – Ретиноїдний ангуліт у поєднанні із вторинною інфекцією
у хворого на акне, що отримував системні ретиноїди.
За час спостереження пацієнтів з акне були виділені деякі актуальні психологічні проблеми при спілкуванні, що мають місце бути у кожного лікаря, який займається лікуванням даної патології.
1. Часто пацієнт негативно налаштований, так як до цього у нього був неуспішний досвід лікування цього дерматозу або у докторів або при застосуванні лікувальної косметики самостійно.
2. Пацієнти часто сприймають проблему і глибоко і поверхнево одночасно.
З одного боку вони вважають це лише зовнішньою косметичною проблемою, з іншого боку – основною причиною невдач у житті. Особливо жінки вважають дефекти шкіри, властиві акне, причиною невдач в особистому житті, неуспіху в кар’єрі або основою неприйняття їх у суспільстві.
У той же самий час вони приходять на прийом до лікаря лише за «маззю», яка, на їх погляд, може вирішити всі проблеми в їхньому житті, не враховуючи того, що це абсолютно ніяк не може вирішити проблеми гормонального дзеркала, захворювань шлунково-кишкового тракту і психо-адаптивних здібностей.
3. Проблема при призначенні системних ретиноїдів полягала в тому, що часто пацієнти перед застосуванням ознайомлюються з інформацією в інтернеті і, досконально вивчивши інструкцію, заявляють про небажання приймати препарат. При цьому вони апелюють фактами і думками форумів, яким складно протистояти з огляду на те, що цієї інформації з ряду причин вони довіряють більше. Побороти це переконання і достукатися до розумної потреби застосування цього препарату саме у цього пацієнта – займає зазвичай багато часу.
Важливість досягнення певного психоемоційного розташування пацієнта і ряд дій і психологічних прийомів, які допомагають домогтися довіри до лікаря як фахівця незаперечна і необхідна при веденні пацієнта з акне.
4. Часто пацієнти відмовляються виконувати призначення і вимагають аргументованого пояснення необхідності того чи іншого препарату. Це зобов’язує лікаря проводити міні-лекцію, щоб пацієнт розумів, що не тільки лікар знає як вирішувати проблему його здоров’я, але і він сам може сприяти поліпшенню результатів лікування.
5. При застосуванні системних ретиноїдів виникає необхідність призначення сонцезахисних препаратів. Це обумовлено дією препарату, який робить більш фоточутливою шкіру. Частою обставиною у веденні таких пацієнтів стає їх самостійне скасування сонцезахисного крему в «несонячні» дні або взимку.
6. З огляду на статистику захворюваності щодо віку, досить часто на прийом приходять пацієнти в супроводі своїх старших родичів – мам і бабусь, які відзначають замкнутість, проблематику перехідного віку і нерозуміння між поколіннями. Тут можливі ситуації, коли підліток дуже хоче лікуватися сам бо розуміє важливість вирішення цієї проблеми або рішення про лікування прийнято батьками і бабусями і пацієнт не зацікавлений в отриманні позитивних результатів лікування, що ускладнює роботу лікаря.
Часто таким дітям закуповують ліки і вони виконують неякісно або не виконують рекомендації. На прийом до лікаря приходять потім його родичі і сумніваються в його кваліфікації і досвідченості вирішення проблеми. Важливо досягти розуміння і розібратися, в чому проблема неуспіху. Якщо не буде вирішена це завдання, підліток не буде вилікуваний, матиме комплекси, які в подальшому стануть причиною і виправданням його неуспіху в навчанні, роботі та особистому житті.
7. При бесіді з пацієнтом підліткового періоду або пацієнта, який приймає спортивні добавки, лікар практичної медицини може зіткнутися з небажанням спілкуватися або зізнаватися в тому, що він приймає ці препарати. Часто пацієнт у цій бесіді вирішує психологічне завдання – що для нього важливіше – здоров’я і стан його шкіри або поліпшення конституційних особливостей, що буде більш впливовим при прийнятті його в суспільстві і більш вагомим при спілкуванні з протилежною статтю.
8. Однією з проблем при спілкуванні з пацієнтом виявляється різниця уяв термінів лікування у доктора і пацієнта. Часто пацієнт недооцінює проблему і тривалий прийом препаратів стає для нього нездійсненним завданням. Тут важливим фактором спілкування з пацієнтом є здатність доктора донести про важливість вирішення проблеми і про можливі наслідки, які можуть виникнути при нехтуванні лікуванням.
9. Фінансова неготовність часто стає стіною при призначенні лікування. Тут від доктора потрібна неабияка обізнаність у ціновій політиці певних препаратів і пошуком задовільної альтернативи згідно клінічної картині захворювання у даного пацієнта.
10. Цілком очікуване погіршення перебігу дерматозу при застосуванні системних ретиноїдів також часто впливає на отримання позитивного ефекту від лікування. Так як пацієнти, зіткнувшись з ним, трактують заплановане погіршення стану шкіри як то, що препарат їм не підходить або не є ефективним.
Підсумовуючи дані щодо комплаєнтності хворих на акне, хотілося би зазначити, що зниження її у вигляді недотримання рекомендацій може призвести до ускладнень терапії та зниження її ефективності, яких можливо було б уникнути або мінімізувати.
4.7 Дослідження рівня тривожності у пацієнтів з акне до та після проведеної терапії
Під час обстеження хворих було звернуто увагу на основні психологічні особливості пацієнтів, а саме на психоемоційну лабільність та депресивні стани. З метою оцінки цих проявів та оцінки впливу терапіі на психоемоційний стан було проведено наступне дослідження.
Тест Спілбергера-Ханіна – це єдина методика, яка дозволяє диференційовано вимірювати тривожність як особистісну властивість і як стан, пов’язаний з поточною ситуацією.
Реактивна тривожність характеризує стан людини в даний момент часу, яке характеризується суб’єктивно пережитими емоціями: напругою, занепокоєнням, заклопотаністю, нервозністю в даній конкретній обстановці або обставинах. Виникає ця реакція як емоційна реакція на стрес і може бути різною за інтенсивністю.
При аналізі результатів треба мати на увазі, що загальний підсумковий показник по кожній із підшкал може перебувати в діапазоні від 20 до 80 балів. При цьому, чим вищим є підсумковий показник, тим вищим є рівень тривожності.
Висока тривожність і дуже висока тривожність (вище 46 балів) прямо може бути пов’язана з наявністю невротичного конфлікту, емоційними зривами і психосоматичними захворюваннями.
Особи, що належать до високотривожних, схильні сприймати загрозу своїй самооцінці і життєдіяльності у великому діапазоні ситуацій і реагувати на них вираженим станом тривожності.
Низька тривожність (менше 12 балів) характеризує стан як депресивний, неактивний з низьким рівнем мотивацій. Іноді дуже низька тривожність у показниках тесту є результатом активного витіснення особистістю високої тривоги з метою показати себе в кращому світлі.
Відповідно до думки авторів методики, особам з високим рівнем тривожності слід формувати почуття впевненості й успіху. Їм необхідно зміщати акцент із зовнішньої вимогливості, категоричності, високої значимості в постановці завдань на змістовне осмислення діяльності та навчитися розбивати великі завдання на більш дрібні.
Для людей з низьким рівнем тривожності, навпаки, потрібно пробудження активності, підкреслення мотиваційних компонентів діяльності, збудження зацікавленості, формування почуття відповідальності у вирішенні тих чи інших завдань.
У дослідження увійшли 61 пацієнт з акне середнього та тяжкого ступеня: з них 40 чоловіків і 21 жінка. До лікування вони відзначали психологічний дискомфорт при спілкуванні, у 14 жінок відзначалася психоемоційна лабільність і тривожність з приводу своєї зовнішності. Цим пацієнтам було проведено тестування за методикою Спілбергера-Ханіна.
До початку терапії високий та надвисокий рівень тривожності (45 і більше балів) був діагностований у 34 пацієнтів: серед них 15 жінок та 19 чоловіків, середній рівень тривожності – у 13 пацієнтів (11 чоловіків та 2 жінки), у 14 (4 жінки та 10 чоловіків) – низький рівень тривожності (табл. 4.2, рис. 4.21).
Таблиця 4.2 – Розподіл дослідних хворих за статтю і рівнем тривожності
| Низький рівень тривожності | Середній рівень тривожності | Високий та надвисокий рівень тривожності | ||||
| Чоловіки | Жінки | Чоловіки | Жінки | Чоловіки | Жінки | |
| До лікування | 10 | 4 | 11 | 2 | 19 | 15 |
| Після лікування | 7 | 1 | 29 | 13 | 4 | 7 |
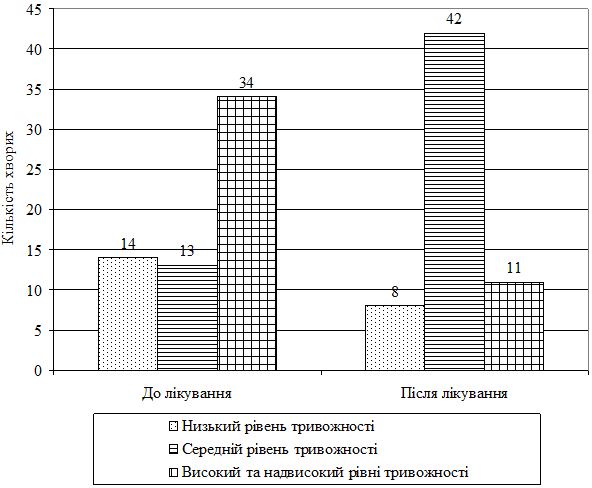
Рисунок 4.21 – Динаміка рівня тривожності хворих у процесі терапії
Після проведеної терапії надвисокий та високий рівень тривожності було діагностовано у 11 пацієнтів з акне середнього та тяжкого ступеня тяжкості, з них 7 жінок та 4 чоловіка. Середній бал тривожності було діагностовано у 42 пацієнтів, з яких було 13 жінок та 29 чоловіків. Низький рівень тривожності було виявлено у 8 пацієнтів, з них 1 жінка та 7 чоловіків. Дані дослідження не корелювали з типом проведеної терапії та тяжкістю дерматозу, оскільки були обумовлені можливо тільки психотипом досліджуваного пацієнта.
Узагальнюючи результати дослідження тривожності за допомогою методики Спілбергера-Ханіна, можна відзначити, що високий та надвисокий рівні тривожності у пацієнтів з акне до лікування становив 34 пацієнта, а після лікування його було діагностовано у 11 пацієнтів, що обумовило його зниження після терапії майже втричі. Середній рівень тривожності зріс до 42 пацієнтів після лікування з діагностованого у 13 пацієнтів до лікування. Низький рівень тривожності було діагностовано у 14 пацієнтів до лікування і у 8 пацієнтів після лікування. Важливо зазначити, що високий рівень тривожності та психоемоційна лабільність до лікування відзначалася частіше у жінок, у той час як низький рівень тривожності як маркер депресії превалював більше у чоловіків.
4.8 Косметологічний супровід хворих на акне в період ремісії
Враховуючи те, що акне є хронічним рецидивуючим дерматозом, однією з цілей роботи було розробити не тільки більш ефективний спосіб лікування, а й профілактичні заходи, які будуть запобігати рецидивам та подовжувати період ремісії. Через 1,5-2 місяці після закінчення терапії та поновлення саловиділення було проведено курс косметологічних процедур 23 пацієнтам з акне. Процедура проводилася щомісячно. Також пацієнти застосовували себорегулюючу косметику «Effaclar duo».
Основною метою розробки цієї методики було максимальне подовження ремісії за рахунок косметологічного впливу на основну патогенетичну ланку акне – фолікулярний гіперкератоз.
Методика полягала у наступному:
1. Очищення шкіри за допомогою засобу на безлужній основі.
2. Нанесення на шкіру слабкого розчину фруктових кислот, експозиція 3-5 хвилин, очищення шкіри.
3. Ультразвукове скрабування за допомогою апарату. Перед початком проведення шкіру зрошували термальною водою.
4. Скрабування шкіри за допомогою ексфоліюючого засобу з грубими абразивними частинками. Інтенсивність впливу регулювалася силою тиску під час масажу.
5. «Прохолодне гідрування» – процедура нанесення просочених гелем алое бинтових смужок на шкіру обличчя під поліетиленову плівку і рушник. Експозиція 20 хвилин.
6. Екстракція комедонів після зняття маски на бинтах.
7. Обробка шкіри антисептиком.
8. Нанесення маски з протизапальним ефектом. Експозиція 20 хвилин.
9. Після видалення маски наносився крем-догляд: себорегулюючий або фотозахисний.
У групі пацієнтів (38 осіб), які в період ремісії використовували тільки себорегулюючу космецевтику, рецидиви акне відзначили 14 осіб. Вони констатували появу нових комедонів у себозалежних зонах Т і U, у 8 пацієнтів з’являлися гострозапальні елементи висипу. Пацієнти відзначили, що пов’язують рецидив з похибками в харчуванні: зловживанні фастфудом, «швидкими» вуглеводами, а також з наявністю перегрівання або стресу.
У 7 пацієнтів, що впродовж року отримували себорегулюючу косметику та проходили косметологічну процедуру ексфоліації шкіри та екстракцію комедонів, за рік відзначалося загострення дерматозу. Вони не пред’являли скарг на множинні відкриті комедони, а відзначали періодичну появу поодиноких пустул без прогресування процесу.
* * *
У процесі статистичної обробки даних кількості елементів висипки у хворих на акне в різних групах було з’ясовано, що у випадку застосування системних ретиноїдів та топічної антибактеріальної терапії спостерігався більш пришвидшений регрес папуло-пустульозних елементів, що також у динаміці підтверджувалося мікробіологічними дослідженнями. Кількість вузлів зменшилася швидше при застосуванні комбінації системних антибіотиків та ретиноїдів, але на третьому місяці кількість вузлів ставала однаковою для всіх терапевтичних груп, що свідчить про те, що незалежно від виду комплексної терапії, але при наявності у ній системних ретиноїдів – спостерігався регрес гострозапальних елементів висипу. Регрес комедонів був поступовим та повільним у всіх групах спостереження, що свідчить про системну дію ретиноїдів на процеси салоутворення та саловиділення.
У ході дослідження також з’ясовано, що знижена комплаєнтність хворих може негативно впливати на ефективність терапії та провокувати ускладнення терапії. Вивчення психологічних проблем при спілкуванні з хворими на акне та дослідження рівня тривожності за методикою Спілбергера-Ханіна дозволило встановити, що лікування системними ретиноїдами позитивно впливає на психоемоційний стан пацієнта, а саме: нормалізує показники високого та низького рівня тривожності, що можуть бути ознаками психоемоційної лабільності або депресії у хворих на акне. Застосування косметологічного супроводу у хворих на акне в період ремісії діє позитивно на стан шкіри та мінімізує передумови появи акне.
Матеріали даного розділу опубліковані в наступних виданнях:
1. Кутасевич Я.Ф., Бронова И.М. Базовая и адъювантная терапия при тяжелых формах акне. Український журнал дерматології, венерології, косметології. 2015. № 2 (57). С. 74–79. [103].
2. Кутасевич Я.Ф., Бронова И.М. Акне: непростая задача в практике клинициста. Здоров‘я України 21 сторіччя. 2016. № 6 (379). С. 76–77 [102].
3. Бронова І.М. Оцінка ефективності лікування акне з урахуванням результатів обстеження за допомогою психометричної методики. Дерматологія та венерологія. 2016. № 2 (72). С. 56–62 [32].
4. Бронова І.М. Особливості динаміки регресу елементів висипки у хворих на акне, що отримували різні види патогенетичної терапії. Медицина сьогодні і завтра. 2017. № 2 (75). С.83–88 [29].
5. Бронова И.М. Проблемы общения с больными акне и пути их преодоления лечащим врачом. Дерматологія та венерологія. 2017. № 1 (75). С. 65–68 [33].
6. Бронова І.М. Особливості психосоматики у пацієнтів з акне, що знаходяться на різних видах комплексної терапії. ІІІ Міжнародний медичний конгрес «Впровадження сучасних досягнень медичної науки у практику охорони здоров’я України» : Матеріали конгресу, м. Київ, 15–17 квітня 2014 р. К., 2014. С. 85 [31].
7. Кутасевич Я.Ф., Бронова І.М. Сучасні аспекти лікування акне у жінок репродуктивного віку. Материалы научно-практической конференции с участием международных специалистов «Инновационные технологии в дерматовенерологии. Междисциплинарные связи», г. Харьков, 13-14 ноября 2015 г. Дерматологія та венерологія. 2015. № 3 (69). С. 78–79 [110].
8. Кутасевич Я.Ф., Бронова И.М. Вариабельность подхода к лечению подрывающего фолликулита. Матеріали науково-практичної конференції з міжнародною участю «Сучасні підходи до діагностики, профілактики та інноваційні технології лікування інфекцій, що передаються статевим шляхом, поширених дерматозів, основні організаційні задачі», 10-11 листопада 2017 р., м. Харків. Дерматологія та венерологія. 2017. № 3 (77). С. 104 [104].
9. Кутасевич Я.Ф. Бронова І.М. Комплексний підхід до лікування акне із застосуванням системних ретиноїдів та косметологічної методики екстракції комедонів. Тези доповідей науково-практичної конференції «Інноваційні досягнення в діагностиці інфекцій, що передаються статевим шляхом, інфекційних і грибкових захворювань та поширених дерматозів. Прогрес у лікуванні» у рамках VI Міжнародного медичного конгресу, м. Київ, 25 квітня 2017 р. К., 2017. С. 160 [107].
10. Кутасевич Я.Ф., Бронова И.М. Особенности коррекции сопутствующих явлений сухости слизистой губ у пациентов с акне, получавших системные ретиноиды. Сучасні проблеми дерматовенерології, косметології та управління охороною здоров’я : Збірник наукових праць. Вип. 14. Харків : Оберіг, 2017. С. 197 [109].
11. Пат. на корисну модель № 118999 UA, МПК А61К31/203, А61Р17/00, А61Р1/16, А61Q17/04. Спосіб лікування пацієнтів з акне середнього та тяжкого ступеня тяжкості / І.М. Бронова, Я.Ф. Кутасевич. № u201701391; заявл. 14.02.17; опубл. 11.09.17, Бюл. № 17 [137].
12. Кутасевич Я.Ф., Маштакова І.О., Бронова І.М. Клінічні рекомендації щодо лікування акне (посібник для лікарів). Харків : ДУ «Інститут дерматології та венерології НАМН України», 2017. 10 с. [106].
РОЗДІЛ 5
ДЕРМАТОСКОПІЧНЕ ДОСЛІДЖЕННЯ ДИНАМІКИ ЕЛЕМЕНТІВ ВИСИПКИ В ПРОЦЕСІ САНОГЕНЕЗУ У ХВОРИХ НА АКНЕ
Дерматоскопічне дослідження шкіри пацієнтам з акне середнього та тяжкого ступеня, які отримували системні ретиноїди, проводилося до початку, в процесі (через 1,5 місяці) і після закінчення терапії (через 5-7 місяців).
Аналіз 63 світлин, що відображували дерматоскопічну картину у хворих на акне, дозволив виділити наступні дерматоскопічні ознаки дерматозу:
1. Наявність розширених отворів сально-волосяних фолікулів з проявами посилення рельєфу тканини по периферії (фолікулярний гіперкератоз).
2. Наявність множинних відкритих і закритих комедонів.
3. Гіперемований фон, за рахунок запалення і розширення судин.
4. Набряк шкіри.
5. Осередки з включеннями світлих відтінків (мають ознаки формування сполучної тканини).
6. Посилення судинного рисунка шкіри по периферії пустули або відкритого комедону.
7. Наявність гнійних корок.
8. Білий віночок навколо розширених гирл сально-волосяних фолікулів (можливо спровокований компресією вмісту комедону або пустули).
9. Виражений неоднорідний рельєф шкіри.
10. Рубцеві елементи постакне з ознакою «мінус тканина».
Усі перераховані вище ознаки спостерігалися у всіх досліджуваних до початку терапії в себозалежних ділянках на обличчі та тулубі (рис. 5.1, 5.2, 5.3, 5.4).
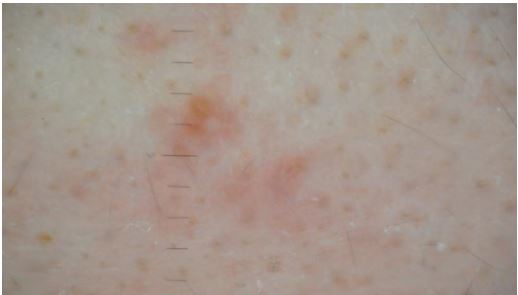
Рисунок 5.1 – Дерматоскопічна картина шкіри у пацієнта з акне до лікування себозалежної ділянки на тулубі (ділянка грудини).
Розширені гирла сально-волосяних фолікулів, посилений шкірний рисунок, відкриті комедони.
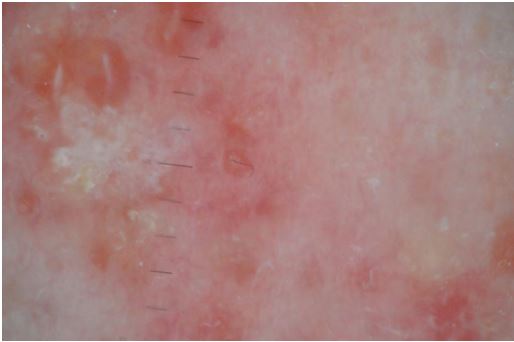
Рисунок 5.2 – Дерматоскопічна картина акне на шкірі обличчя до лікування –наявні ознаки: гіперемія, набряк, посилений судинний рисунок, ознаки формування сполучної тканини після регресу папуло-пустульозного елементу висипки, неоднорідність розподілу сполучної тканини, рубцеві елементи постакне з ознакою «мінус тканина».
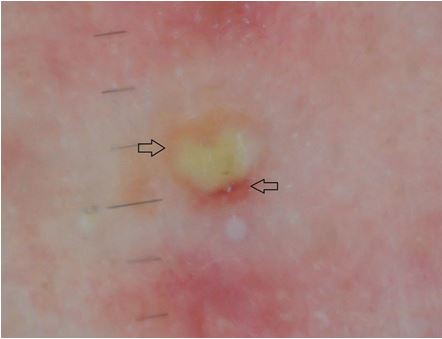
Рисунок 5.3 – Дерматоскопічна картина шкіри у пацієнта з акне до лікування:
Папуло-пустульозний елемент, який має гіперемований неоднорідний вінчик, який більш виражений у напряму найбільшого скупчення гною. Знімок зроблено, коли пацієнт знаходився у вертикальному положенні.
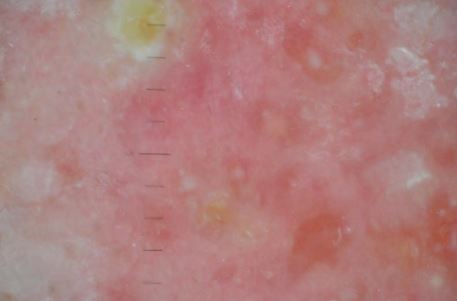
Рисунок 5.4 – Дерматоскопічна картина шкіри у пацієнта з акне до лікування в ділянці носо-губного трикутника центрофаціально. Наявні ознаки дерматозу: гіперемія, посилення шкірного та судинного малюнку, набряк, гіперкератоз, неоднорідність рельєфу, закриті комедони, серозна кірочка на елементі, що регресує з ознаками формування сполучної тканини.
При дослідженні дерматоскопічних знімків у процесі терапії (через 1,5 місяці) у всіх пацієнтів було виявлено наступне:
1. Зменшення інтенсивності гіперемії, часткова нормалізація кольору шкірних покривів в осередках висипу.
2. Фокальна гіперемія і посилення судинного рисунка навколо елементів, які регресують.
3. Відсутність гнійних корок.
4. Відкриті зяючі гирла сально-волосяних фолікулів без наявності комедонів.
5. Осередки з включеннями світлих відтінків, що мають ознаки формування рубцевої тканини.
6. Сухість шкіри, про що свідчить посилений відбиток світла при дерматоскопії.
7. Відсутність пустул (рис. 5.5, 5.6).
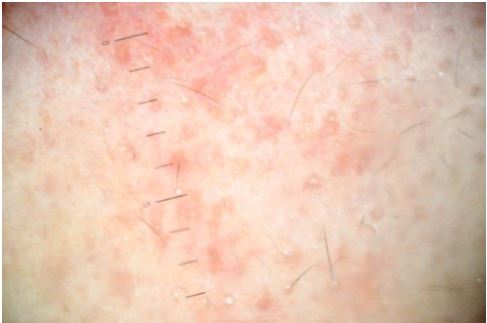
Рисунок 5.5 – Дерматоскопічна картина шкіри в процесі лікування у пацієнта з акне, що отримував системні ретиноїди. Знімок зроблено в себозалежній зоні тулуба. Наявні ознаки регресу дерматозу: відсутність тотальної гіперемії, фокальна гіперемія навколо гострозапальних елементів, що знаходяться в останній фазі регресу.
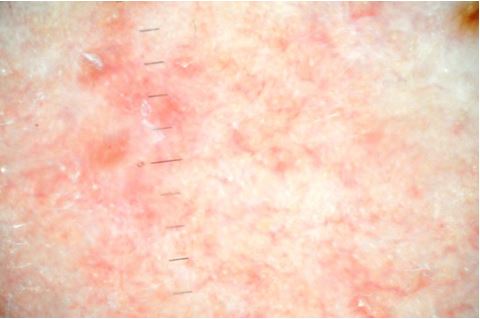
Рисунок 5.6 – Знімок ділянки шкіри щоки у пацієнтки з акне, що приймала системні ретиноіди, у процесі терапії (через 1,5 місяці після початку лікування). Наявна наступна динаміка регресу дерматозу та фармакологічного супутнього ефекту терапії: іритантність, сухість шкіри; відсутність набряку, посилений судинний рисунок, формування гіпотрофічних елементів постакне.
При оцінці дерматоскопічних знімків після проведеної терапії спостерігалася наступна динаміка змін шкіри в осередках висипу:
1. Нормалізація кольору шкіри.
2. Відсутність набряку.
3. Фокальна мала вираженість судинного рисунка навколо регресуючих елементів висипу.
4. Сухість, стоншеність епідермісу з елементами лущення.
5. Відсутність пустул та інших гострозапальних елементів висипу.
6. Неоднорідні ділянки формування свіжої сполучної тканини.
7. Відсутність відкритих і закритих комедонів.
8. Звуження усть сально-волосяних фолікулів (рис. 5.8, 5.9, 5.10).
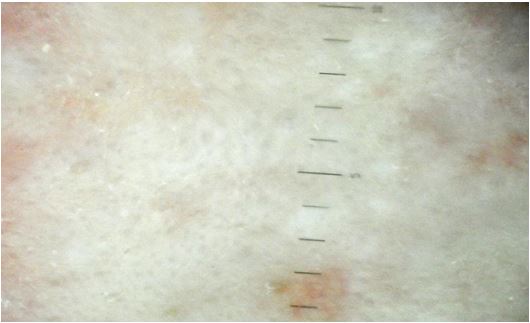
Рисунок 5.7 – Дерматоскопічні ознаки регресу акне у пацієнта, що отримував системні ретиноїди: відсутність набряку, фокальне посилення судинного рисунка біля ділянки, де формується свіжий рубцевий елемент постакне, ознаки гіперпігментації, пусті гирла сальноволосяних фолікулів, відсутність відкритих
та закритих комедонів, гострозапальних елементів, відсутні прояви гіперкератозу. Після лікування.
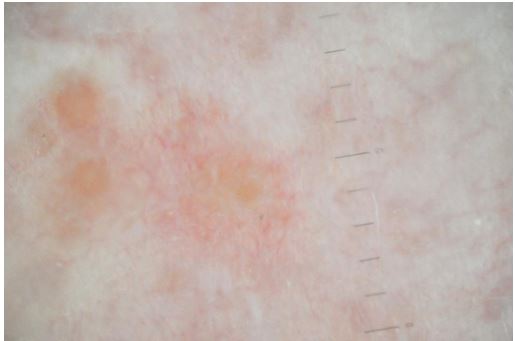
Рисунок 5.8 – Дерматоскопічна картина шкіри у пацієнтки з акне після лікування, яке проводилося системними ретиноїдами. Наявні ознаки: відсутність гострозапальних елементів та проявів дерматозу, майже непомітні гирла сально-волосяних фолікулів, у центрі регрес та заміщення сполучною тканиною папуло-пустули, рубцевий елемент має нормотрофічний характер. Шкіра суха, стоншена.
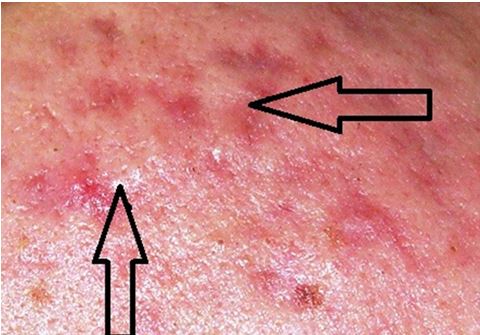
Рисунок 5.9 – Дерматоскопічна картина шкіри у пацієнта з акне, що не отримував системні ретиноїди, та формування рубцевої тканини, що має гіпертрофічний характер. Знімок ілюструє відмінність рельєфу та характеру формування рубцевої тканини без впливу системних ретиноїдів.
* * *
Дане дослідження дозволило визначити виражений запальний процес і його еволюцію на різних стадіях саногенезу та початок розвитку постакне-рубців. Після лікування дерматоскопічно спостерігалася нормалізація стану шкіри і зникнення запальних елементів, загальної гіперемії в осередках висипу, ознаки звуження сально-волосяних фолікулів, відсутність відкритих та закритих комедонів, а також свіжі атрофічні рубці на різних стадіях формування.
Таким чином, епілюмінесцентний метод дослідження доводить доцільність використання системних ретиноїдів для лікування хворих на акне середнього та тяжкого ступеня і вплив цих препаратів на усі ланки патогенезу.
Матеріали даного розділу опубліковані в наступних виданнях:
1. Дерматоскопические признаки регресса элементов акне в процессе саногенеза / Я.Ф. Кутасевич, В.А. Савоськина, Ю.В. Щербакова, С.Н. Джораева, И.М. Бронова. League medica. 2017. № 2. Р. 11–14 [55].
РОЗДІЛ 6
МІКРОБІОЛОГІЧНІ ДОСЛІДЖЕННЯ
Відомо, що на ділянках шкіри, які багаті сальними залозами, переважають пропіонібактерії, які утворюють асоціації з іншими мікроорганізмами (коринебактеріями, стафілококами). Сальна залоза формує майже позбавлену кисню нішу, заселену в ділянці дна такими факультативними анаеробами, як Propionibacterium spp., а в ділянці устя – ліпофільними аеробами, такими як Malassezia spp. Щільність заселення шкіри пропіонібактеріями на шкірі обличчя та голови може становити 1х105 КУО/см2. Щільність заселення пропіонібактеріями починає помітно зростати в пубертатному періоді та стабілізується до 25 років життя [72, 118, 138]. Сталість складу мікрофлори сальних залоз шкіри, поряд з доступністю тригліцеридів для переважаючих там пропіонібактерій, вважається характерним для шкіри людини [172]. Переважання гідрофільної грамнегативної мікробіоти та стафілококів з постійними змінами видового складу є характерним для ділянок шкіри, що багаті на сальні та потові залози [190]. Вважається, що на сальних ділянках шкіри, як середовище шкірного сала, так і діяльність пропіонібактерій, перешкоджають колонізації кокової флори [202, 219, 245, 247]. Саме тому, за мету дослідження було взято оцінку біотопу поверхні шкіри у хворих на акне як до лікування, так і в процесі саногенезу, враховуючи різні види патогенетичного лікування.
Для дослідження пацієнти були розділені на три групи: першу групу склали пацієнти, які отримували Акнетін і системні антибіотики, другу – Акнетін і зовнішню антибіотикотерапію – і третю – Акнетін у монотерапії.
Метою дослідження було дослідити вплив системних ретиноїдів у монотерапії на біоценоз шкіри та необхідність антибіотикотерапії з можливістю посилити антибактеріальний ефект.
Усім пацієнтам було триразово проведено бактеріологічне дослідження (до лікування, через 1,5 місяця після початку лікування і після лікування).
Першу групу хворих становили 20 пацієнтів, від яких було виділено 21 штам мікроорганізмів, що належали до 4 родів, у двох пацієнтів було виділено асоціацію бактерій.
При детальному розгляді мікроорганізми роду Staphylococcus склали 81,0 % (17 штамів), Corynebacterium – 9,4 %, Streptococcus – 4,8 %, Micrococcus – 4,8 %. Домінуючими видами виявилися S. epidermidis, S. haemolyticus (по 35,3 %) (рис. 6.1).
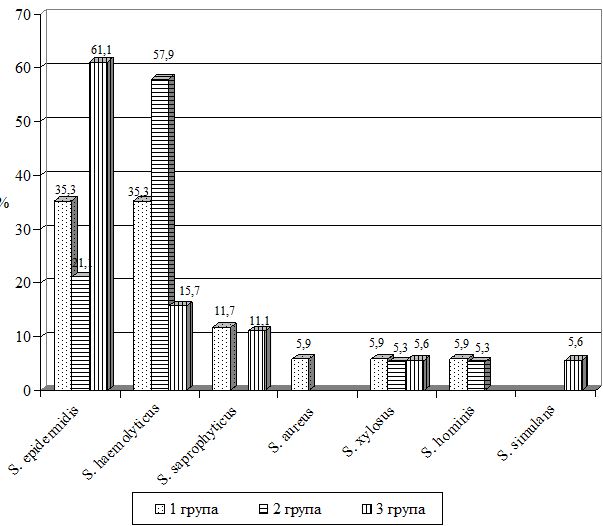
Рисунок 6.1 – Структура стафілококової мікрофлори, що була виділена у пацієнтів до лікування
У другу групу пацієнтів увійшло 20 осіб, від яких було виділено 19 штамів, що належали до роду Staphylococcus, у п’ятьох пацієнтів було виділено внутрішньовидову асоціацію бактерій. Домінуючими видами виявилися S. haemolyticus і S. epidermidis (57,9 % і 21,1 % відповідно).
У третю групу увійшов 21 пацієнт, від яких було виділено 23 штами, що належали до чотирьох родів, у чотирьох пацієнтів було виділено асоціацію бактерій. При детальному розгляді мікроорганізми роду Staphylococcus становили 78,3 % (18 штамів), Corynebacterium – 8,7 %, Streptococcus – 8,7 %, Micrococcus – 4,3 %. Найбільш часто у пацієнтів даної групи ізолювали S. epidermidis – 61,1 % (рис. 6.1).
У видовий структурі досліджуваної мікробіоти у всіх групах домінували коагулазонегативні представники роду – S. haemolyticus і S. epidermidis. Мікроценоз шкіри у всіх трьох групах не мав достовірних взаємозв’язків зі статтю і віком, клінічною формою і тяжкістю акне, наявністю рубцевих змін, зверненням до дерматолога або досвідом лікування антибіотиками і системними ретиноїдами в анамнезі.
Контрольна група: до групи увійшло 20 людей, від яких було виділено 26 штамів, які належали до трьох родів мікроорганізмів: Staphylococcus, Corynebacterium і Streptococcus. При цьому в складі шкірного біотопу домінували стафілококи (80,8 %), як самостійно, так і у складі асоціацій (26,9 %) (рис. 6.2).
Як видно з наведеного рисунка, у складі біотопу шкіри домінував комменсал – S. epidermidis (57,7 %) як самостійно, так і в асоціації з іншими коагулазонегативними представниками роду (71,4 %), стрептококами (14,3 %) і коринебактеріями (14,3 %).
На наступному етапі дослідження було проведено вивчення чутливості виділених лабораторних штамів стафілококів до антибактеріальних препаратів різних груп (рис. 6.3).
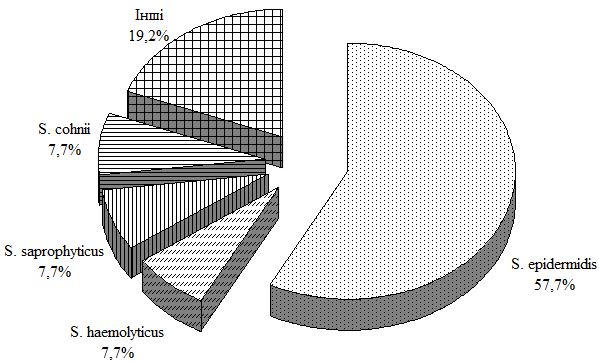
Рисунок 6.2 – Видовий склад виділеноі флори у людей з контрольноі групи
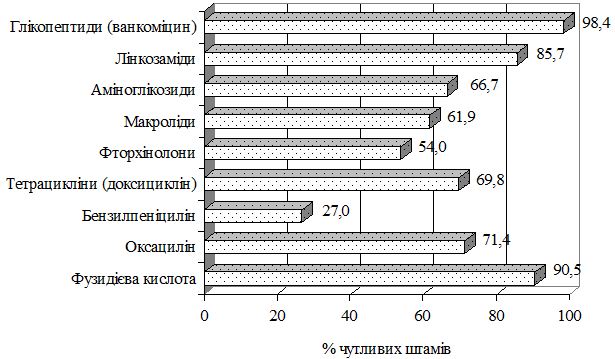
Рисунок 6.3 – Визначення чутливості до антибіотиків лабораторних штамів стафілококів, що були виділені від пацієнтів з акне
При визначенні чутливості до антибіотиків, більшість виділених штамів стафілококів демонструвало високу чутливість до фузидієвої кислоті, лінкозамідів і тетрацикліну (відсоток чутливих штамів становив 90,5 %, 86,0 % та 69,8 % відповідно).
Більшість штамів виявилася стійкими до β-лактамних антибіотиків групи пеніциліну, фторхінолонів і макролідів (73,0 %, 46,0 % і 38,1 % відповідно). 19,0 % (12 штамів) ізольованих лабораторних штамів стафілококів були визначені як полірезистентні, 3,4 % (2 штами) мали екстенсивну резистентність, полірезистентних штамів виявлено не було.
При вивченні взаємозв’язку між чутливістю стафілококів до антибіотиків і клінічною формою акне або наявністю рубців достовірних взаємозв’язків виявлено не було.
Від пацієнтів першої групи виділено 13 лабораторних штамів, що належали до роду Staphylococcus, серед виділених штамів були відсутні коагулозопозитивні представники роду з лідируючими позиціями S. epidermidis і S. haemolyticus (35,0 % і 20,0 % відповідно).
У процесі терапії та по досягненню клінічних змін пацієнтам трьох груп було проведено друге бактеріологічне дослідження (рис. 6.4).
При дослідженні матеріалу, отриманого від пацієнтів третьої групи (ізольовано 17 штамів), значних змін у складі шкірного ценозу не виявлено.
При порівнянні стану ценозу в досліджуваних групах на даному етапі лікування звертає на себе увагу той факт, що в першій і другій групах пацієнтів (Акнетін + системні антибіотики і Акнетін і зовнішня антибіотикотерапія) відзначено тенденцію до нормалізації складу ценозу. Так, кількість ізольованих штамів S. epidermidis збільшилася з 35,8 % до 53,8 % у першій групі і з 21,1 % до 52,9 % у другій групі обстежених, а кількість виділених штамів S. haemolyticus знизилася: в першій групі з 35,3 % до 30,8 %, а в другій групі з 57,9 % до 41,2 %, що відобразило більш позитивну динаміку нормалізації мікробіоценозу шкіри у групі, де застосовувалася терапія з використанням системних ретиноїдів та топічних антибактеріальних засобів, та дозволило обґрунтувати достатню тривалість антибіотикотерапії.
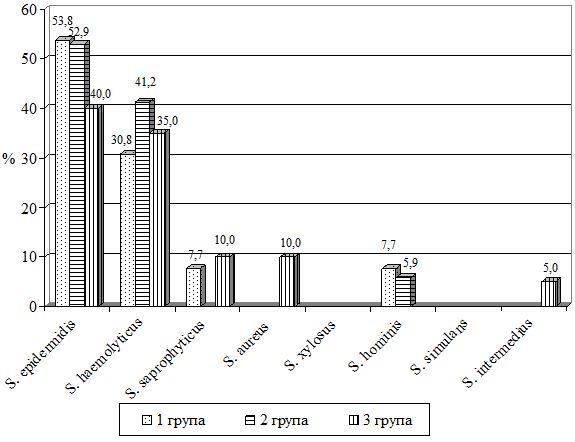
Рисунок 6.4 – Структура стафілококовоі мікрофлори, що була виділена у пацієнтів різних груп в процесі лікування
Від пацієнтів третьої групи було ізольовано 20 штамів стафілококів. Звертає на себе увагу виділення від цієї групи пацієнтів виділення представників роду з вираженим патогенним потенціалом – S. aureus і S. intermedius (10,0 % і 5,0 % відповідно), що свідчило про відсутність вираженої позитивної динаміки в цій групі пацієнтів на даному етапі терапії.
У третій групі пацієнтів спостерігалася зворотна тенденція: кількість ізольованих штамів S. epidermidis знизилася з 61,1 % до 40,0 %, у той час як відсоток виділення S. haemolyticus зріс з 16,7 % до 35,0 %, на тлі появи штамів з явним патогенним потенціалом S. aureus і S. intermedius (10,0 % і 5,0 % відповідно).
Після лікування пацієнтам цих груп також було проведено бактеріологічне дослідження. Отримані дані наведено на рисунку 6.5.
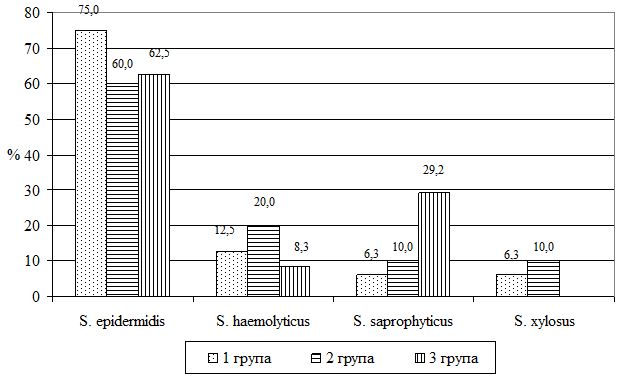
Рисунок 6.5 – Структура стафілококової мікрофлори, що була виділена у пацієнтів різних груп після лікування
Від першої групи пацієнтів було виділено 16 штамів, серед яких домінували представники нормальної резидентної мікрофлори шкіри – S. epidermidis (75,0 %) і S. saprophyticus (12,5 %), у другій групі (з 20 ізольованих штамів) – 60,0 % і 20,0 % відповідно, у третій групі обстежених (виділено 24 штами) дані показники склали 62,5 % і 29,2 % відповідно.
Аналізуючи наведену діаграму (рис. 6.5) встановлено, що після проведеного лікування шкірний мікробіоценоз характеризувався нормалізацією видового складу і зникненням видів з вираженим патогенним потенціалом (S. haemolyticus, S. aureus) і значним зниженням кількості S. haemolyticus до 12,5 % у першій, 8,3 % у другій та у 20,0 % у третій групах обстежених.
* * *
На підставі результатів проведеного дослідження, можна зробити висновки, що зміна показників мікробіоценозу в процесі саногенезу в групах з системними ретиноїдами та антибіотиками демонструвала повільну нормалізацію мікробіоценозу шкіри в ділянках висипу, а в групі, в якій пацієнти отримували системні ретиноїди в монотерапії, у процесі лікування спостерігалося збільшення видів з вираженим патогенним потенціалом.
Враховуючи показники мікробіоценозу шкіри після закінчення лікування, можна зробити висновки, що терапія акне середнього та тяжкого ступеня тяжкості системними ретиноїдами в монотерапії так само, як і комплексна із застосуванням антибіотикотерапії сприяє досягненню вираженого клінічного ефекту (регресу елементів висипу, реабілітації шкіри) та нормалізації мікробіоценозу шкіри, що характеризувався зникненням видів з вираженим патогенним потенціалом.
Подальшого поліпшення результатів лікування (зокрема нормалізації біоценозу шкіри) можливо досягти призначенням топічних антибактеріальних засобів додатково до терапії системними ретиноїдами.
Матеріали даного розділу опубліковані в наступних виданнях:
1. Кутасевич Я.Ф., Джораєва С.К., Бронова И.М. Акне: динамика изменений микробиоценоза в процессе саногенеза у пациентов, получающих системные ретиноиды. Дерматологія та венерологія. 2016. № 4 (74). С. 43–54 [101].
2. Особенности динамики изменений кожи в процессе саногенеза у больных акне / Я.Ф. Кутасевич, Г.И. Губина-Вакулик, С.Н. Джораева, И.А. Маштакова, И.М. Бронова. Proceedings of the International Scientific Conference «Topical Issues of Science and Education», Warsaw (Poland), July 17, 2017. Warsaw, 2017. Vol. 4. P. 25–30 [136].
РОЗДІЛ 7
ПАТОМОРФОЛОГІЧНІ ЗМІНИ ШКІРИ В ПРОЦЕСІ САНОГЕНЕЗУ
У ПАЦІЄНТІВ З АКНЕ, ЩО ОТРИМУВАЛИ СИСТЕМНІ РЕТИНОЇДИ
7.1 Дослідження біоптатів шкіри хворих на акне
Патоморфологічне дослідження проводилось у 5 пацієнтів та дало можливість оцінити динаміку елементів шкірного покриву в процесі лікування.
Перший біоптат у різних пацієнтів взяли в ділянці фолікулярної папули, що формувалася, фолікулярної пустули (папуло-пустули) і «квітучої» пустули (рис. 7.1).
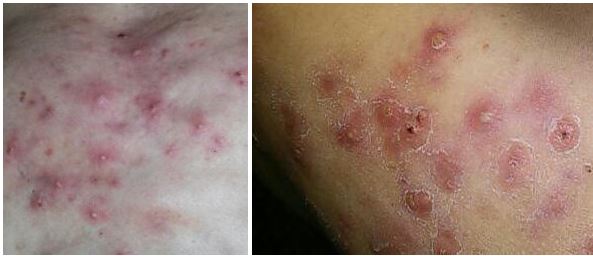
Рисунок 7.1 – Фото ділянки шкіри хворого на акне до лікування.
При вивченні матеріалу біопсії виявилося, що якщо біоптат узятий у ділянці фолікулярної папули, то мікроскопічно визначалося потовщення епітеліального шару в піхві волосяного фолікула, базальна мембрана місцями відсутня, а навколо волосяного фолікула сформований макрофагально-лімфоцитарний інфільтрат з проникненням окремих круглоядерних лейкоцитів в епітеліальний шар. Просвіт піхви волосяного фолікула в цій ділянці був дуже вузьким, точно відповідав діаметру волоса. Сальна залоза, сполучена з порожниною піхви волосяного фолікула в цій же середній ділянці, велика, з численними себоцитами, що мали велике еугетерохромне ядро і численні прозорі округлі вакуолі в цитоплазмі, які містять ліпіди (шкірне сало). Зустрічалися сальні залози з лейкоцитарним інфільтратом, подібним вище описаному, з наявністю ділянок відсутності базальної мембрани і проникненням лімфоцитів між себоцитами (рис. 7.2).
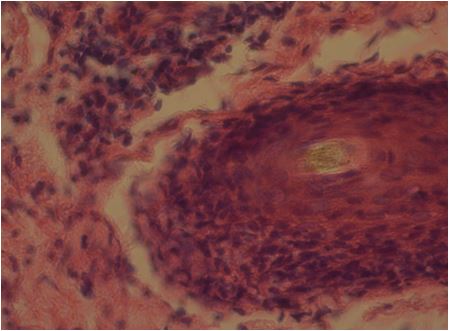
Рисунок 7.2 – Мікроскопічний зріз у середній частині піхви волосяного фолікула (біоптат до лікування з ділянки наявності папул). Шар проліферуючих епітеліоцитів щільно примикає до стрижня волосу. Навколо піхви волосяного фолікула густий лейкоцитарний інфільтрат при відсутності нейтрофілів. Забарвлення гематоксиліном та еозином. Збільшення х400.
Біопсія шкіри до лікування, взята в ділянці папуло-пустули, демонструвала початок гнійного запалення: епітелій піхви волосяного фолікула інфільтрований нейтрофілами, макрофагами, лімфоцитами, базальна мембрана відсутня взагалі. Розташована коло волосяного фолікула сальна залоза велика, з численними себоцитами.
Біопсія, що взята до лікування з ділянки пустули на тлі раніше згаданої гіперплазії поверхневих епідермоцитів, дозволила виявити наявність у дермі великого округлої форми осередку гнійного запалення з майже повним гістолізом елементів волосяного фолікула і сальної залози (рис. 7.3).
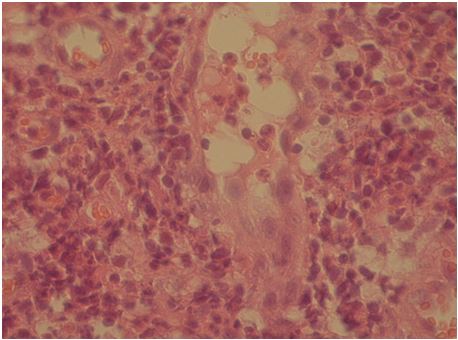
Рисунок 7.3 – Об’ємне гнійне запалення на місці волосяного фолікула обумовлює майже повний лізис волосяного фолікула зі збереженням кількох епітеліальних клітини (біоптат, взятий до лікування з ділянки наявності пустули). Забарвлення гематоксилін та еозином. Збільшення х400.
Таким чином, при вивченні гістологічної картини фолікулярної папули, папуло-пустули і пустули привертало увагу, що при цьому зміни були проявом провідних ознак захворювання – фолікулярного гіперкератозу (як результат гіперпроліферації епітеліоцитів) і запалення. Первинне запалення навколо середньої частини волосяного фолікула було не гнійним, а, можливо, імунним, оскільки інфільтрат представлений макрофагами і лімфоцитами з ознаками агресії щодо проліферируючих, незрілих епітеліоцитів, нездатних у зв’язку з цим здійснювати в достатній мірі фізіологічну регенерацію своєї базальної мембрани (рис. 7.4). А коли елементом висипу була папуло-пустула, то це вже більш виражена дезорганізація компонентів у середній частині піхви волосяного фолікула: проліферація епітеліоцитів та їх незрілість наростали, базальна мембрана відсутня, а поява ознак гнійного запалення, очевидно обумовлена активацією специфічної мікрофлори у зв’язку із затримкою виведення шкірного сала. Прогресування гнійного запалення призвело до лізису середньої частини піхви волосяного фолікула, сальної залози і навколишньої дерми.
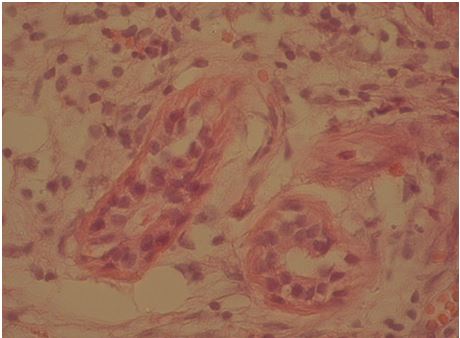
Рисунок 7.4 – Макрофагально-лімфоцитарний інфільтрат навколо потових залоз у хворого на акне тяжкого ступеня до початку лікування. Забарвлення гематоксиліном та еозином. Збільшення х100.
Цікаво, що і залозистий епітелій потових залоз, і поверхневий епідерміс у цих біоптатах також мав ознаки гіперпроліферації (рис. 7.5). Епідерміс потовщений, його поверхня нерівна, епідермально-дермальна межа мала хвилясті контури, тобто можна говорити про неглибокі та широкі акантолітичні вирости епідермісу. Поверхнева судинна мережа демонструвала наявність васкуліту і периваскуліту невеликої вираженості (рис. 7.6). Дерма була набряклою.
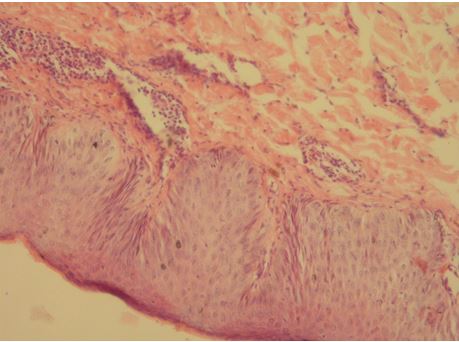
Рисунок 7.5 – Гіперплазований епідерміс до початку лікування. Забарвлення гематоксиліном та еозином. Збільшення х100.
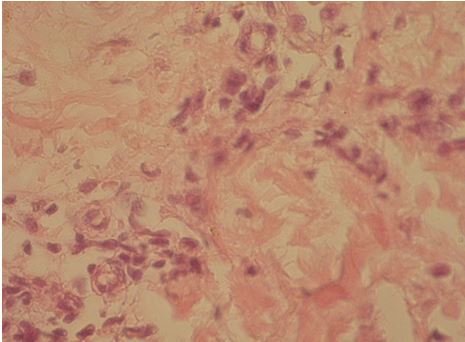
Рисунок 7.6 – Периваскуліт в субепідермальному шарі дерми у хворого до початку лікування. Набряк дерми. Забарвлення гематоксиліном та еозином. Збільшення х400.
Вже на 2-3-му тижні прийому системних ретиноїдів клінічно спостерігався регрес елементів висипки у всіх представників групи дослідження. Вони виявлялися в зниженні саловиділення, у тому числі в себозалежних зонах, наростаючою сухістю шкірних покривів і слизових оболонок. Наприкінці першого місяця відзначалося зниження кількості пустульозних елементів (рис. 7.7).
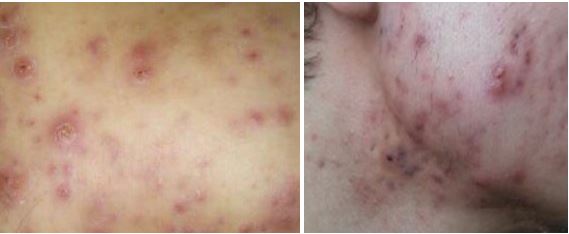
Рисунок 7.7 – Регрес пустульозних елементів.
Цікавим був той факт, що кількість дрібних пустул до кінця першого місяця значно зменшувалася, але відзначалася поява підшкірних, досить болісних інфільтратів або папул.
У матеріалі біопсій шкіри під час лікування можна було відзначити суттєве зменшення кількості епітеліоцитів в епідермісі, епідерміс став тоншим, більш вираженим був паракератоз, що свідчило про прискорення дозрівання молодих епідермоцитів, з’являлися апоптотичні тільця. Сальні залози меншого об’єму і з меншою кількістю себоцитів, ніж у біопсіях до лікування; зустрічалися різні варіанти: з фокусами гнійного ексудату, з макрофагально-лімфоцитарними інфільтратами навколо сальних залоз, а якщо в сальній залозі сформувалася щільна склерозована оболонка замість базальної мембрани, то ззовні до неї прилягала грануляційна тканина, інфільтрована макрофагами, лімфоцитами, нейтрофілами (рис. 7.8, 7.9, 7.10).
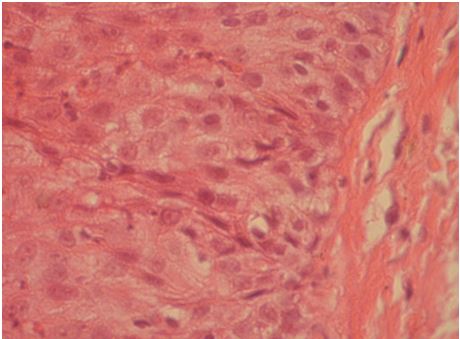
Рисунок 7.8 – Біопсія, взята в процесі лікування. Виражене зменшення кількості епідермоцитів у базальному шарі епідермісу, але загалом епідерміс товстий. Забарвлення гематоксиліном та еозином. Збільшення х100.
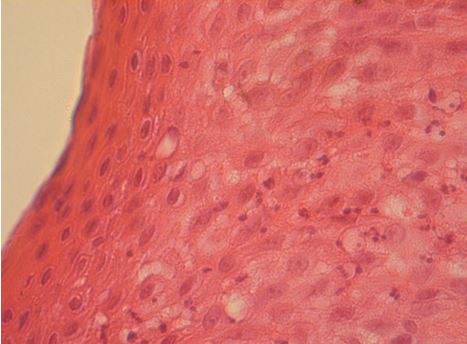
Рисунок 7.9 – Біопсія, взята в процесі лікування. Поверхневий епідерміс
з паракератозом у зовнішньому шарі і з численними апоптотичними тільцями в шарі шипуватих епідермоцитів. Забарвлення гематоксиліном та еозином. Збільшення х400.
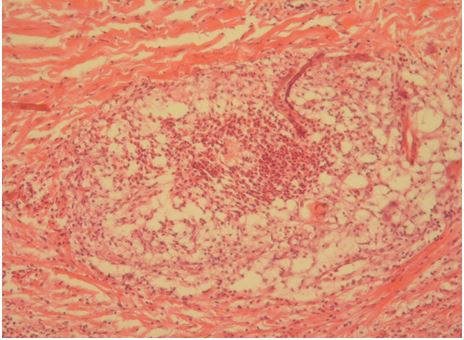
Рисунок 7.10 – Біопсія, що була взята в процесі лікування. Сальна залоза з невеликим гнійним запаленням у центрі. Забарвлення гематоксиліном та еозином. Збільшення х100.
Аналогічна грануляційна тканина формувалася навколо середньої частини піхви волосяного фолікула одночасно зі склерозуванням межі між епітелієм і дермою і зі зменшенням кількості епітеліоцитів, що вистилали стінку піхви волосяного фолікула. Васкуліт у дермі зберігся.
Таким чином, через 1,5 місяця системного лікування хворих на тяжку форму акне в біоптатах шкіри спостерігалися такі зміни, які можна трактувати як результат більш швидкого проходження диференціювання епітеліоцитів, що «знімає» таку патогенетичну ланку важкого акне, як потовщення епітеліального шару піхви волосяного фолікула з гіперкератозом. Прохідність піхви волосяного фолікула для шкірного сала, імовірно, відновлюється.
На четвертому місяці терапії у 2 пацієнтів тривало формування підшкірних болісних елементів. Їх клінічна характеристика була відмінною від таких при акне без терапії. Ці елементи мали тенденцію завмирати і мимовільно регресувати, без формування гнійного стрижня, запального віночка і зміни кольору шкірного покриву над ними. Можливо, гістологічно виявлені округлі ділянки грануляційної тканини, інфільтрованої лейкоцитами, і являють собою ці підшкірні, досить болісні елементи, що визначалися клінічно (рис. 7.11).
Рисунок 7.11 – Біоптат, взятий на 4-му місяці з початку лікування. Наявність у дермі великих округлих осередків, представлених
грануляційною тканиною з макрофагально-лімфоцитарною інфільтрацією. Забарвлення гематоксиліном та еозином. Збільшення х100.
Взяття біоптатів у цей термін (через 4-5 місяців після початку системного лікування ретиноїдами) у інших хворих дало можливість продемонструвати практично повне завершення запалення в шкірі, що можна спостерігати як макроскопічно (рис. 7.12), так і мікроскопічно: відсутність у матеріалі біоптату скупчення лейкоцитів, зникнення або значне зменшення ознак васкуліту, розвиток рубцевої тканини в дермі, відсутність волосяних фолікулів (або наявність редукованих) та сальних залоз із одночасним стоншенням епідермісу і атрофією потових залоз або завершенням хронічного інтерстиціального запалення потових залоз (рис. 7.13, 7.14, 7.15).
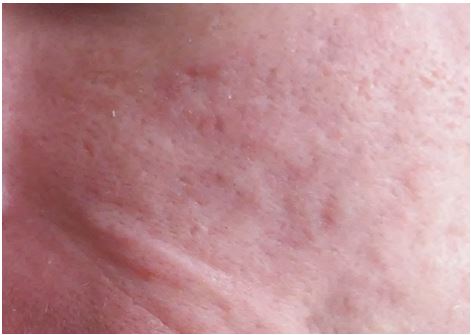
Рисунок 7.12 – Макроскопічна картина шкіри після лікування, що демонструє повний регрес запальних елементів акне.
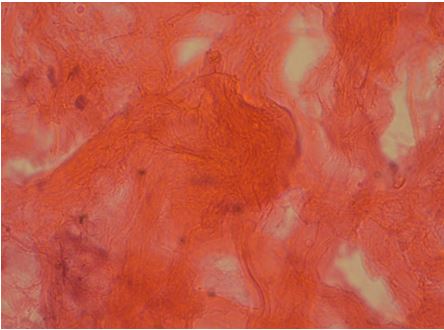
Рисунок 7.13 – Біоптат шкіри узятий через 5 місяців після початку лікування. Ознаки рубцювання в дермі. Забарвлення гематоксіліном та еозином. Збільшення х400.
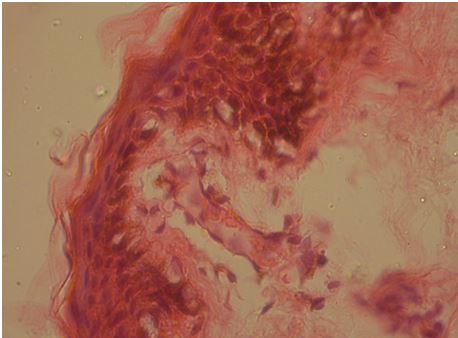
Рисунок 7.14 – Атрофія епідермісу через 4 міс. лікування. Забарвлення гематоксиліном та еозином. Збільшення х400.
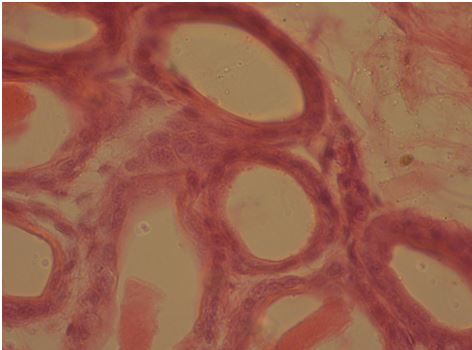
Рисунок 7.15 – Завершення хронічного інтерстиціального запалення потових залоз. Атрофічний стан гландулярного епітелію. Забарвлення гематоксиліном та еозином. Збільшення х400.
Підсумовуючи результати патогістологічного дослідження біоптатів шкіри при лікуванні системними ретиноїдами тяжкого акне, було складено таблицю 7.1, в якій демонструється поступове зменшення ознак гіперпроліферації епітелію шкіри та запалення, появу ознак атрофії епітелію та накопичення колагену в дермі.
Таблиця 7.1 – Узагальнення наявності патогістологічних змін у результаті проведених досліджень у процесі саногенезу
| Ознака | Наявність ознак до лікування | Наявність ознак у процесі лікування |
Наявність ознак після лікування |
| 1. Потовщення епідермісу та епітелію піхви волосяного фолікула | ++ | + | – |
| 2. Набряклість дерми | ++ | + | – |
| 3. Фрагментація колагену | + | +/– | – |
| 4. Судини з периваскулярним інфільтратом | + | +/– | – |
| 5. У пустулах нейтрофільна інфільтрація | + | – | – |
| 6. Лізис сальної залози | + | – | – |
| 7. Наявність грануляційної тканини з макрофагально-лімфоцитарною інфільтрацією | – | ++ | – |
| 8. Велика кількість фібробластів і фіброцитів у дермі | – | + | + |
| 9. Накопичення колагену в дермі | – | + | ++ |
| 10. Атрофія епідермісу, волосяних фолікулів та потових залоз | – | +/– | + |
Примітка:
1. + – наявність ознаки у всіх пацієнтів з групи дослідження.
2. +\– – ознака була присутня не у всіх пацієнтів з групи дослідження.
