Державна установа
«Інститут дерматології та венерології НАМН України»
Федорич Павло Володимирович
УДК [616.64+618.15]:616.993.1]-07-084-085
ПОПЕРЕДЖЕННЯ МЕДИКО–СОЦІАЛЬНИХ НАСЛІДКІВ
ІНВАЗІЙ СЕЧОСТАТЕВОЇ СИСТЕМИ, СПРИЧИНЕНИХ
ТРИХОМОНАДАМИ ТА ЛЯМБЛІЯМИ – ДІАГНОСТИКА, КОМПЛЕКСНА ТЕРАПІЯ, ПРОФІЛАКТИКА
14.01.20 – шкірні та венеричні хвороби
Автореферат
дисертації на здобуття наукового ступеня
доктора медичних наук
Харків — 2021
Дисертацією є рукопис.
Робота виконана в Українській військово-медичній академії.
Науковий консультант:
доктор медичних наук, професор
Мавров Геннадій Іванович,
Державна установа «Інститут дерматології та венерології НАМН України»,
завідувач сектора вивчення впливу епідемії ВІЛ на проблему інфекцій,
що передаються статевим шляхом.
Офіційні опоненти:
доктор медичних наук, професор
Дюдюн Анатолій Дмитрович,
Дніпровський державний медичний університет МОЗ України, завідувач кафедри
шкірних та венеричних хвороб;
доктор медичних наук, професор
Бондар Сергій Анатолійович,
Вінницький національний медичний університет імені М. І. Пирогова,
завідувач кафедри шкірних та венеричних хвороб;
доктор медичних наук
Запольський Максим Едуардович,
Одеський національний медичний університет МОЗ України, доцент кафедри дерматології та венерології.
Захист відбудеться «28» квітня 2021 року об 11:00 годині на засіданні спеціалізованої вченої ради Д 64.603.01 при ДУ «Інститут дерматології та венерології НАМН України», за адресою: 61057, м. Харків, вул. Чернишевська, 7/9.
З дисертацією можна ознайомитись у бібліотеці ДУ «Інститут дерматології та венерології НАМН України» (61057, м. Харків, вул. Чернишевська, 7/9).
Автореферат розісланий «25» березня 2021 р.
Вчений секретар
спеціалізованої вченої ради,
к. мед. н. Т. В. Губенко
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність теми. За останні декілька десятиліть змінилась патогенність мікроорганізмів, що є паразитами сечостатевої системи (ССС) людини (В.І. Степаненко та ін., 2015). Giardia lamblia, Trichomonas tenax, Pentatrichomonas hominis могли зазнати патоморфозу і колонізувати ССС хворих на інфекції, що передаються переважно статевим шляхом (ІПСШ) (E.S. Roointan et al., 2013; A.K. Mehr et al., 2015). На сучасному етапі важливим є впровадження нових методів діагностики протозойних інвазій ССС, які мають високу чутливість, специфічність, клінічну інформативність, а також доступні для лабораторних служб (А.Н. Григорьев, 2013; Г.М. Бондаренко та ін., 2016). В Україні дотепер не проводилося визначення Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia в ССС людини, також не проводилося генотипування Trichomonas vaginalis (S.C. Masha et al., 2017). Питання щодо патогенності різних морфотипів цього мікроорганізму залишається відкритим. Разом з тим, визначення виду найпростіших, імовірно, має вирішальну роль у запобіганні рецидивів і реінфекцій з урахуванням поєднаної генітальної та екстрагенітальної інвазії. Крім того, для успішного лікування відповідних хворих слід враховувати стан їх імунної системи, а також склад патогенних мікробних асоціацій (МА) найпростіших із бактеріями (А.Д. Дюдюн и др., 2016). Тому виникла потреба в ретельному вивченні окремих представників типу найпростіших, як чинників перебігу ІПСШ для запобігання тяжких медичних і соціальних наслідків, що впливають на здоров’я нації, таких як безплідність, порушення статевої функції, втрата працездатності. Необхідно суттєво поліпшити надання медичної допомоги хворим на сечостатевий трихомоноз і лямбліоз шляхом впровадження нових підходів до діагностики, лікування та профілактики зазначених інвазій.
Зв’язок роботи з науковими програмами, планами, темами. Робота виконана в рамках науково-дослідної роботи Державної установи «Інститут дерматології та венерології Національної академії медичних наук України» на тему «Удосконалити заходи щодо діагностики, лікування, профілактики інфекцій, що передаються статевим шляхом, та ВІЛ-інфекції серед споживачів психоактивних речовин» (№ держреєстрації 0117U000984) та Української військово-медичної академії (УВМА) Міністерства оборони України на тему «Особливості клінічного перебігу, діагностики, лікування коморбідної соматичної патології у військовослужбовців та працівників Збройних Сил України, обумовленої факторами професійної діяльності» (№ держреєстрації 0114U003803). Здобувач є співвиконавцем теми. Дисертантом особисто виконано основні фрагменти наукових робіт з епідеміологічних, клінічних, імунологічних, мікробіологічних, молекулярно-біологічних, гістологічних, електронномікроскопічних досліджень, а також розробку медикаментозних та функціональних методів терапії й напрацювання алгоритмів надання спеціалізованої медичної допомоги.
Мета та задачі дослідження.
Мета роботи – підвищити ефективність діагностики, лікування, профілактики інвазій сечостатевої системи, спричинених Trichomonas vaginalis та іншими представниками типу найпростіших на підставі даних про їх епідеміологію, клініку, властивості збудників, морфоімунопатогенез, а також про наявність супутньої колонізації умовно-патогенними збудниками
Для досягнення поставленої мети були поставлені такі задачі:
- Провести бібліосемантичний аналіз і метааналіз наукових публікацій, статистичних звітів і медичних баз даних для виявлення невирішених наукових і практичних питань з проблеми діагностики, лікування та профілактики сексуально трансмісивних захворювань, спричинених Trichomonas vaginalis та іншими збудниками протозойних інвазій ССС.
- Розробити оригінальні праймери для виявлення ДНК Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia методом полімеразної ланцюгової реакції (ПЛР). Провести визначення їх специфічності за допомогою метода секвенування біологічного матеріалу. Порівняти ефективність розробленого ПЛР тесту з традиційними методами лабораторної діагностики.
- Оцінити поширеність Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia серед пацієнтів, хворих на ІПСШ. Встановити епідеміологічні закономірності розповсюдження трихомонадної інвазії сечостатевого тракту.
- Провести електронно-мікроскопічне дослідження біологічного матеріалу для визначення патогенезу змішаної трихомонадної інвазії та патогенності різних морфотипів Trichomonas vaginalis.
- Провести молекулярне типування Trichomonas vaginalis, що циркулюють в Україні, на основі поліморфізму гена актину.
- Виявити імунні порушення при колонізації сечостатевого тракту Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia та обґрунтувати призначення імуномодулюючого препарату в комплексі лікування.
- Визначити мікробні асоціації збудників, в тому числі, анаеробні та мікроаерофільні бактерії, що супроводжують протозойні інвазії ССС.
- Обґрунтувати і розробити методи комбінованого лікування хворих на урогенітальний трихомоноз і лямбліоз з урахуванням наявності супутнього інфікування анаеробними та мікроаерофільними бактеріями та імунних порушень.
- Розробити і впровадити алгоритм організації надання медичної допомоги хворим на урогенітальний трихомоноз і лямбліоз для запобігання виникнення медичних і соціальних наслідків цих інвазій.
Об’єкт дослідження – паразитарні інвазії сечостатевої системи.
Предмет дослідження – патогенетичні та клінічні особливості паразитарних інвазій ССС; лабораторні показники досліджень хворих на інфекції урогенітального тракту, їх зміни під впливом проведеної терапії; діагностика, лікування попередження медико-соціальних наслідків інвазій ССС.
Методи дослідження: бібліосемантичний аналіз; метааналіз; загальні клінічні (з’ясування скарг, анамнезу захворювання та життя, аналіз суб’єктивних і об’єктивних даних обстеження, постановка діагнозу, контроль ефективності лікування) та лабораторні (клінічні аналізи крові, сечі, калу, біохімічні та серологічні аналізи крові); мікробіологічні (мікроскопічні та культуральні дослідження мікробіоти ССС); імунологічні (показники імунограм); методи епідеміологічного аналізу; молекулярно-генетичні (ПЛР, секвенування); ультраструктурні (електронна мікроскопія); методи біометричної та медичної статистики.
Наукова новизна отриманих результатів. Наукова новизна полягає у тому, що у хворих на протозойні інвазії ССС виявлено декілька збудників інвазії, а саме: Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia. Вперше показано значну розповсюдженність уражень, спричинених Giardia lamblia, Trichomonas tenax та Pentatrichomonas hominis, ССС хворих на ІПСШ з хронічним перебігом.
Доведено важливу роль Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia в перебігу та патогенезі хронічних ІПСШ на сучасному етапі.
Доведено необхідність розробки праймерів для виявлення ДНК Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia у біологічних рідинах та обґрунтовано методики їх отримання.
Встановлено епідеміологічні закономірності трихомонадної інвазії сечостатевого тракту, а саме – поширеність Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia, а також чинники їх розповсюдження, проаналізовано особливості сексуальної поведінки хворих на ІПСШ та їх партнерів для встановлення можливих шляхів та локусів статевого зараження.
Визначено особливості клінічного перебігу сечостатевого трихомонозу в сучасних умовах, а саме – наявність генітальних і екстрагенітальних осередків, частота рецидивів, залежно від додаткової колонізації сечостатевих шляхів Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia, а також умовно-патогенними, переважно, анаеробними та мікроаерофільними бактеріями.
Проведено порівняння мікроскопічної, культуральної діагностики та ПЛР при виявленні трихомонад у ССС хворих на ІПСШ.
Вперше виявлено зв’язок імунодефіцитних станів з наявністю протозойних інвазій ССС людини.
Вперше показано взаємозв’язок протозойних інвазій ССС із наявністю бактеріального вагінозу (БВ) у жінок та еквіваленту цього стану у чоловіків (анаеробного та мікроаерофільного дисбактеріозу ССС).
Вперше проведено молекулярне типування Trichomonas vaginalis, що циркулюють в Україні, на основі поліморфізму гена актину.
Проведено електронно-мікроскопічне дослідження уражених тканин хворих на трихомоноз та охарактеризовано ультраструктурні особливості атипових трихомонад та супутньої бактеріальної флори. При цьому вперше отримано клініко-лабораторні дані щодо патогенності овального морфотипу Trichomonas vaginalis.
Науково обґрунтовано застосування нових комплексних методів лікування хворих на протозойні інвазії ССС (спричинені Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia), в тому числі із призначенням імунопатогенетичної і антипротозойної терапії та доведено їх ефективність.
Практичне значення отриманих результатів. Вперше впроваджено сучасний алгоритм надання медичної допомоги хворим на сечостатевий трихомоноз із застосуванням лікувально-профілактичних та організаційних підходів, що дозволяють елімінувати різні види трихомонад, а також лямблії з урогенітального тракту для запобігання ускладнень, що призводять до негативних медичних і соціальних наслідків. Розроблено, науково обґрунтовано та впроваджено в практичну охорону здоров’я нові методи комбінованого лікування хворих на протозойні інвазії ССС, спричинені як Trichomonas vaginalis, так і іншими збудниками протозойних інвазій, а саме Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia, в тому числі при поєднаних ураженнях із мікрофлорою, що є асоційованою з БВ (анаеробною та мікроаерофільною), а також на тлі порушень з боку імунної системи (патент України на корисну модель № 103397 від 10.12.2015; патент України на корисну модель № 109257 від 25.08.2016).
Вперше в Україні розроблено та отримано праймери для виявлення ДНК Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia у біологічних рідинах (патент України на винахід № 107910 від 25.02.2015; патент України на винахід № 110759 від 10.02.2016; патент України на винахід № 110767 від 10.02.2016). Відповідність праймерів до видоспецифічних ділянок ДНК зазначених мікроорганізмів було підтверджено за допомогою методу секвенування.
Запропоновано системну концепцію і програму профілактичних та організаційних заходів з боротьби із сечостатевими інвазіями, що спричинені трихомонадами і лямбліями. Створено рекомендації для індивідуальної профілактики протозойних реінвазій ССС, спричинених не Trichomonas vaginalis.
Основні положення дисертації впроваджено в практику роботи: клініки шкірних та венеричних хвороб КНП Харківської обласної ради «Обласний клінічний шкірно-венерологічний диспансер № 1»; КУ «Запорізький обласний шкірно-венерологічний диспансер» Запорізької обласної ради; Полтавського обласного клінічного шкірно-венерологічного диспансеру; КНП «Одеський обласний шкірно-венерологічний диспансер» Одеської обласної ради; КЗ «Рівненський обласний шкірно-венерологічний диспансер» Рівненської обласної ради; КНП «Міський клінічний шкірно-венерологічний диспансер № 5» Харківської міської ради; ДУ «Інститут дерматології та венерології НАМН України». Теоретичні положення дослідження і практичні рекомендації впроваджено в практику навчання студентів обох факультетів УВМА Міністерства оборони України, кафедри дерматовенерології та ВІЛ/СНІДу Харківської медичної академії післядипломної освіти; кафедри дерматовенерології та косметології з курсом дерматовенерології і естетичної медицини факультету післядипломної освіти Запорізького державного медичного університету.
Особистий внесок здобувача. Ідея дисертаційного дослідження належить автору разом із науковим консультантом. Автором розроблений план дослідження, визначені мета та завдання. Особисто автором проведені: бібліосемантичний пошук та аналіз літературних джерел, патентної ситуації, визначення актуальних питань проблеми, що вивчається. Клінічне обстеження, анкетування, лікування пацієнтів проведено здобувачем.
Дисертантом самостійно проведено комплексне клініко-лабораторне обстеження та лікування 1037 хворих на ІПСШ, облік і статистичну обробку показників результатів загальних клініко-лабораторних і спеціальних обстежень, особисто написано всі розділи дисертації. Особисто сформульовано всі наукові узагальнення, положення, результати, висновки та рекомендації.
Усі опубліковані наукові праці, в яких викладено основні положення і зміст дисертації, є авторськими. З наукових праць, опублікованих у співавторстві, в дисертації використано лише ті ідеї, положення і висновки, які є результатом особистої роботи здобувача і становлять його індивідуальний науковий внесок. Конфлікту інтересів немає.
Апробація результатів дисертації. Основні положення та результати роботи представлені здобувачем під час доповідей на з’їздах науково-практичних конференціях різного рівня: науково-практичній конференції Національної медичної академії післядипломної освіти (НМАПО) ім. П.Л. Шупика «Проблеми захворювань шкіри та інфекцій, що передаються переважно статевим шляхом, у дітей та підлітків» (Київ, 2015), 13th EADV Spring Symposium (Athens, 2016); науково-практичному семінарі І Збори військових дерматологів (Вінниця, 2016); ІІІ (Х) з’їзді Української асоціації лікарів-дерматовенерологів та косметологів (УАЛДВК) (Львів, 2017); науково-практичній конференції НМАПО ім. П.Л. Шупика «Місце дерматовенерології в міждисциплінарному вирішенні питань діагностики та лікування хронічних захворювань», (Київ, 2017); науково-практичній конференції з міжнародною участю НМАПО ім. П.Л. Шупика «Дерматовенерологія в розробках молодих науковців», (Київ, 2018); Всеукраїнській науково-практичній конференції УАЛДВК з міжнародною участю «Особливості надання дерматовенерологічної допомоги населенню України в умовах медичної реформи» (Івано-Франківськ, 2018); науково-практичній конференції з міжнародною участю НМАПО ім. П.Л. Шупика «Дерматовенерологія в розробках молодих науковців» (Київ, 2019); Всеукраїнській науково-практичній конференції з міжнародною участю «Досягнення та перспективи в сучасній дерматовенерології: Європейський та український досвід, взаємодія науки та практики» (Харків 2019).
Публікації. За результатами дослідження опубліковано 49 праць. З них: 6 статей у наукових фахових виданнях України (3 – у моноавторстві), 16 статей у фахових виданнях, акредитованих ДАК України, що входять до наукометричних баз (5 написані у моноавторстві); 10 статей у наукових виданнях інших держав (4 – англійською мовою, 3 – у моноавторстві), що входять до наукометричних баз Index Copernicus, Googlе Scholar, РІНЦ та інших; 7 статей у інших наукових виданнях України та 4 – у матеріалах наукових форумів різного рівня, включаючи міжнародні. Отримано 2 патенти України на корисну модель, та 3 патенти України на винахід. Опубліковано 1 методичні рекомендації. 4 із наведених вище статей входять до міжнародних наукометричних баз Scopus (3) та Web of Science (1).
Структура та обсяг дисертації. Дисертаційна робота викладена українською мовою на 308 сторінках машинописного тексту. Складається зі вступу, огляду літератури, характеристики матеріалів і методів дослідження, 4 розділів власних досліджень, обговорення результатів дослідження з аналізом та узагальненням отриманих даних, висновків, рекомендацій та списку використаної літератури. Робота ілюстрована 34 рисунками та містить 21 таблицю. Бібліографічний список містить 281 джерело, з них 162 – кирилицею і 119 – латиницею.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Матеріали та методи досліджень. Застосовувався бібліосемантичний та метааналіз; загальні клінічні та лабораторні данні, також проводилися мікробіологічні, імунологічні, епідеміологічні, молекулярно-генетичні, ультраструктурні дослідження. Для визначення поширеності ІПСШ було проаналізовано дані 607 хворих з Олександрійської клінічної лікарні м. Києва. Для вивчення сексуальної поведінки проведено анкетування 100 молодих людей (50 чоловіків та 50 жінок, віком (21 ± 1) рік). З метою детекції анаеробної мікрофлори досліджено 30 чоловіків з використанням набору реагентів Фемофлор-16. Для визначення поширеності Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia проведене дослідження 452 осіб. Для порівняння культурального метода та полімеразної ланцюгової реакції в реальному часі (ПЛР-РЧ) використано матеріал від 97 пацієнтів. Апробацію оригінальних праймерiв для Pentatrichomonas hominis проведено у 37 хворих. Молекулярне типування Trichomonas vaginalis проведено у 29 пацієнтів. Здійснено секвенування 62 зразків із ССС хворих. Вивчено дію суміші α- і ß-дефенсинів у 62 хворих на ІПСШ з імунною недостатністю. Електронну мікроскопію проведено зі зразками від 52 хворих. Порівняння виявлення Trichomonas vaginalis методами мікроскопії, культуральним та ПЛР проведено у 377 пацієнтів. Епідеміологічні дані щодо трихомонозу в Україні за 2011-2018 рр. складено зі статистичних даних по областях. Клініко-епідеміологічну характеристику трихомонозу вивчено у 241 хворого. Проліковано за розробленими схемами 165 хворих із Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia. З них 56 хворих із супутньою мікрофлорою, асоційованою з БВ. Для дослідження імунної системи визначалися в сироватці крові кількість Т-лімфоцитів (CD3+), Т-хелперів (CD4+), Т-цитотоксичних лімфоцитів (CD8+); імунорегуляторний індекс Тх/Тс; активних Т-лімфоцитів, В-лімфоцитів (CD22+), лімфоцитів-кілерів (CD18+), 0-лімфоцитів; реакцію бласттрансформації з фітогемаглютиніном, фагоцитарний індекс, фагоцитарний показник, НСТ-тест, а також рівні Ig А, G, М (К.С. Камышева, 2016). Діагностика трихомонадної інвазії: виявлення трихомонад у мазках та культуральне дослідження у середовищі М 305 (Індія) та СВТ (Російська Федерація). Використовувалися також ПЛР та ПЛР-РЧ в ампліфікаторі ДТ-96 (Російська Федерація) згідно модифікованого протоколу. Для виявлення Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia застосовувались оригінальні праймери (П.В. Федорич, С.Б. Зелений, 2015; 2016). Використовувався також праймер для Trichomonas vaginalis ДНК-Технологія (Російська Федерація). Авторські праймери підбиралися за допомогою програми Vector NTI. Послідовності для відповідних видів отримані з бази даних GenBank (NCBI). Для перевірки унікальності використовувалася програма BLAST (NCBI). Для перевірки продуктів ПЛР за допомогою підібраних праймерів використовувався пакет програм Bioinformatics tools (США). Для електронної мікроскопії зрізи, отримані на ультрамікротомі УМТП-7, контрастувались уранілацетатом і цитратом свинцю. Ультраструктура клітин досліджувалася за допомогою електронного мікроскопа ПЕМ-125К при пришвидшеній напрузі 75 kV, забезпеченого системою аналізу зображення САІ – 01А SELMI (Україна) з використанням CCD камери DX 2 і пакету програм KAPPA (Німеччина). Типування T. vaginalis проводилося за поліморфізмом гена актину, який ампліфікувався гніздовим методом на термоциклері Терцик (Російська Федерація) з використанням двох пар праймерів – зовнішніх: Tv8S (5`‑TCTGGAATGGCTGAAGAAGACG-3`) і Tv9R (5`‑CAGGGTACATCGTATTGGTC-3`); та внутрішніх: Tv10S (5`‑CAGACACTCGTTATCG-3`) і Tv11R (5`‑CGGTGAACGATGGATG-3`). При аналізі електрофореграм враховувався характерний для кожного генотипу спектр фрагментів ДНК, що утворюються при рестрикції, відповідно до схеми [T. Crucitti et al., 2008]. Секвенування проводилося з використанням приладу «Applied Biosystems» SOLIDTM System 5500xl (USA), який використовує емульсійну ПЛР і твердофазне лігування. Продукти ПЛР екстрагувалися з 2 % агарозного гелю за допомогою DEAE Cellulose Menbrane (0,45μm) (Serva, Germany), використовуючи стандартну методику очищення (Б. Альбертс и др., 2018). Нуклеотидні послідовності порівнювалися з відомими за допомогою SOLIDTM System 5500xl (USA), а також бази даних GenBank. Визначення мікроорганізмів, асоційованих із БВ, проводилося за допомогою методу ПЛР-РЧ на ампліфікаторі ДТ-96 за допомогою набору реагентів ФЕМОФЛОР®-16 (НПО «ДНК-технология», РФ). Вивчення сексуальної поведінки проводилося шляхом анкетування. Запитували про сексуальні та супутні феномени – лібідо, ерекцію, еякуляцію, любрикацію, оргазм, біль, відчуття задоволення (R.G. Rogers et al., 2018; F. Montorsi et al., 2010). Оцінка мікробіологічної та клінічної ефективності запропонованої комбінованої терапії (специфічна + імунна) проводилася шляхом порівняння відповідних клініко-терапевтичних груп щодо елімінації збудників протозойних інвазій та їх патогенних мікробних асоціацій. Статистичне опрацювання результатів проведено з використанням пакету програм STATISTICA 9.0. (StatSoft). Для параметричного аналізу даних використовувалася програма MS Excel 2010. Визначено М – середню арифметичну величину, m – її похибку, Р –достовірність різниці середніх величин. Достовірність результатів оцінювалася згідно критерію Стьюдента (А.И. Кобзарь, 2012).
Результати досліджень та їх обговорення.
Локальним дослідженням у місті Києві визначено поширеність інфікування на збудники, що є найбільш клінічно значимими для хворих на ІПСШ. Chlamydia trachomatis було виявлено у 159 (26,2 %) із 607 обстежених пацієнтів – 85 чоловіків та 74 жінок. Mycoplasma hominis було виявлено у 122 з 585 (21,1 %) обстежених пацієнтів – 64 чоловіків та 58 жінок. Mycoplasma genitalium, відповідно, у 17 (6,6 %) із 258 пацієнтів – 6 чоловіків та 11 жінок. Ureaplasma urealyticum знайдено у найбільшої кількості пацієнтів (305 осіб, тобто у 48,8 % з 601 обстеженого пацієнта) – 157 чоловіків та 148 жінок. Trichomonas vaginalis було ідентифіковано у 28 (5,2 %) з 535 пацієнтів – 15 чоловіків та 13 жінок. Human papillomavirus мав місце у 158 з 297 обстежених (53,2 %) пацієнтів – 88 чоловіків та 70 жінок. Neisseria gonorrhoeae було виявлено у 33 з 297 (8,5 %) пацієнтів – 8 чоловіків та 25 жінок. Таким чином, найбільш розповсюдженими були Human papillomavirus, Ureaplasma urealyticum, Chlamydia trachomatis та Mycoplasma hominis. Тому дослідження на ці мікроорганізми у вказаному регіоні є найбільш доцільним при проведенні діагностичних обстежень. Кількість випадків трихомонозу на 100000 населення в цілому по Україні повільно знижується, залишаючись, проте, на досить високому рівні: всього – 97,6; чоловіки – 42,7; жінки – 145,0. Офіційні статистичні дані не відображають справжню поширеність трихомонозу в Україні. Про це свідчить вкрай нерівномірний розподіл по регіонах та суттєві гендерні відмінності. У Житомирській, Полтавській та Чернівецькій областях співвідношення чоловіків і жінок найбільш відрізнялося – більш ніж 1 до 30. В інших областях – Хмельницькій, Херсонській, Кіровоградській та Дніпропетровській кількість жінок із трихомонозом перевищувала кількість чоловіків із трихомонозом не більше ніж у два рази. При аналізі статевих і вікових відмінностей в захворюваності на трихомоноз спостерігалися суттєві відмінності в окремих областях України. У кожній області є свої особливості, очевидно, пов’язані з економічними і соціальними чинниками поширення трихомонозу (табл. 1).
Таблиця 1 – Захворюваність на сечостатевий трихомоноз чоловіків і жінок різного віку (на 100 000 відповідного населення) у 2018 і 2010 рр.
| Чоловіки | Жінки | |||||||
| 15-19 років | 20-29 років | 30-39 років | 40-59 років | 15-19 років | 20-29 років | 30-39 років | 40-59 років | |
| Україна (2018) | 36,7 | 122,1 | 89,0 | 25,3 | 152,7 | 433,7 | 339,5 | 115,1 |
| Україна (2010) | 59,8 | 242,8 | 186,6 | 44,6 | 336,3 | 814,0 | 723,1 | 204,7 |
| Львівська (2018) | 81,3 | 125,7 | 65,4 | 8,4 | 136,6 | 496,5 | 393,9 | 78,4 |
| Львівська (2010) | 89,9 | 172,1 | 129,6 | 21,9 | 312,0 | 889,9 | 836,9 | 94,2 |
| Київська (2018) | 22,1 | 108,4 | 71,3 | 20,9 | 192,2 | 640,6 | 554,3 | 104,3 |
| Київська (2010) | 35,9 | 79,4 | 72,0 | 10,7 | 310,7 | 824,9 | 961,0 | 136,8 |
| Харківська (2018) | 29,7 | 121,2 | 128,1 | 37,2 | 91,5 | 364,9 | 330,9 | 101,4 |
| Харківська (2010) | 50,9 | 269,0 | 208,7 | 36,2 | 330,9 | 1143,5 | 1092,4 | 201,6 |
| Дніпропетровська (2018) | 160,3 | 340,6 | 219,6 | 67,0 | 354,1 | 703,1 | 483,0 | 155,7 |
| Дніпропетровська (2010) | 130,8 | 508,2 | 433,8 | 116,2 | 531,8 | 1118,4 | 885,1 | 274,4 |
Співвідношення міського і сільського населення серед нововиявлених випадків трихомонозу в Україні в 2018 році: 111,5 – сільське і 91,3 – міське. Таким чином, на сьогоднішній день захворюваність на селі трохи вища. Трихомоноз «йде» в сільську місцевість, де пацієнти менш доступні для проведення диспансерних заходів. Отримані дані дозволяють говорити про новий підхід до вивчення епідеміології ІПСШ із позицій малих соціальних груп – осіб різного віку і статі, що мешкають на окремих територіях, а також мають певні особливості статевої поведінки.
У 241 хворого на трихомоноз, виявлена супутня мікрофлора: хламідіоз – у 116 ([48,1 ± 3,2] %), мікоплазмоз – у 87 ([36,1 ± 3,1] %), гарднерельоз – у 40 ([16,6 ± 2,4] %) хворих. Також у 123 (77,2 %) хворих діагностовано безсимптомну вірусну інфекцію: вірус простого герпесу 1 і 2 типу – у 118 ([49,0 ± 3,2] %), цитомегаловірус – у 19 ([7,9 ± 1,7] %) і вірус Епштейна-Барр – у 8 ([3,3 ± 1,2] %) хворих. При підтвердженні діагнозу трихомоноз найбільш чутливим виявився метод ПЛР – до 95 %. Він дещо гірше виявляв безсимптомні форми (до 90 %). Метод культури виявився оптимальним при різних клінічних формах. Він мав чутливість 84,6 %, а специфічність – до 100 % (табл. 2).
Таблиця 2 – Лабораторні маркери трихомонадної інвазії при різних клінічних формах сечостатевого трихомонозу
| Клініка | Кіль-кість | ПЛР + | Нативний мазок + | Культура + | ||||
| Кіль-кість | % | Кіль-кість | % | Кіль-кість | % | |||
| Неускладнені форми
(уретрит, баланопостит, вульвовагініт, цервіцит, ерозія шийки матки) |
124 | 118 | 95,2 ± 1,9 | 86 | 69,4 ± 4,1 | 108 | 87,1 ± 3,0 | |
| Ускладнені форми
(простатит, епідидиміт, аднексит, цистит, сексуальні розлади, безпліддя) |
77 | 72 | 93,5 ± 4,7 | 48 | 62,3 ± 5,5 | 67 | 87,0 ± 3,8 | |
| Безсимптомна форма | 40 | 33 | 82,5 ± 6,5 | 23 | 57,5 ± 7,8 | 29 | 72,5 ± 7,1 | |
| УСЬОГО | 241 | 223 | 92,5 ± 2,7 | 157 | 65,1 ± 3,1 | 204 | 84,6 ± 2,3 | |
При аналізі клінічних проявів у 26 чоловіків (17 %) виявлено безсимптомний перебіг. Провідним клінічним синдромом у 58 (38 %) хворих було виявлено уретрит, у 21 (14 %) – простатит, у 11 (7 %) – епідидиміт, у 23 (23 %) баланопостит. Копулятивні і репродуктивні розлади мали місце у 12 чоловіків, що склало 8 %. Серед 90 жінок у 76 (74 %) зустрічалася патологія як нижніх, так і верхніх поверхів урогенітального тракту. Цистит виявлено у 8 (9 %) жінок, вульвовагініт – у 17 (19 %), цервіцит – у 9 (10 %), ерозії шийки матки – у 17 (19 %), аднексит – у 14 (15,6 %). У 14 жінок (16 %) спостерігався безсимптомний перебіг трихомонадної інвазії. Порушення менструального циклу, безпліддя і сексуальні розлади як основний клінічний синдром був у 11 жінок, що склало 12 %. Отже, особливості клінічних проявів УТ у поєднанні з мікст-інфекціями, що передаються статевим шляхом, характеризуються або малосимптомним перебігом захворювання, або багатофокусністю ураження, наявністю супутніх мікроорганізмів. Трихомоноз зазнав клінічного патоморфозу. Збільшилася частота атипових і резистентних до лікування форм.
Об’єктом електронно-мікроскопічного дослідження слугували 5–9 добових культур трихомонад, виділених від 52 хворих. Були виділені два морфотипи вірулентних форм T. vaginalis: грушовидні і овальні, при цьому, останній морфотип переважав у хворих на хронічний трихомоноз – 67 %. Ультраструктурні особливості T. vaginalis овального морфотипу дозволяє віднести їх до вірулентних форм, а не дегенеративних (рис. 1, 2).
 Рисунок 1 – T. vaginalis округлої форми. Ядро неправильної форми по центру клітини. Цитолема і каріолеми цілісні. У цитоплазмі
Рисунок 1 – T. vaginalis округлої форми. Ядро неправильної форми по центру клітини. Цитолема і каріолеми цілісні. У цитоплазмі
виявляються одиничні гідрогеносоми (Г), численні електронно-щільні везикули. Каріоплазма значно просвітлена. Гетерохроматин дифузно
розподілений по ядру і вздовж внутрішньої ядерної мембрани. У цитоплазмі виявляються травні вакуолі (В)
 Рисунок 2 – Фрагмент T. vaginalis. Цитолемма не скрізь чітко проглядається. Мікроворсини відсутні. Контур ядерної мембрани
Рисунок 2 – Фрагмент T. vaginalis. Цитолемма не скрізь чітко проглядається. Мікроворсини відсутні. Контур ядерної мембрани
звивистий. Гідрогеносоми (Г) мають рівномірну гомогенну структуру. В цитоплазмі спостерігаються везикули, травна вакуоль (В),
а також електронносвітлі порожнини, що не окреслені елементарною мембраною
У зразках, узятих з цервікального каналу, піхви і уретри, визначалася велика кількість супутніх мікроорганізмів, які перебували між клітинами епітелію, – коки, хламідії, гриби роду Сandida у вигляді бластоспор (рис. 3, 4).
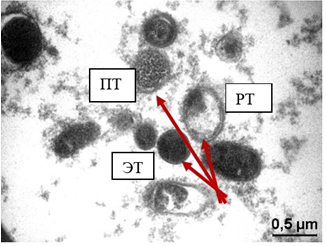 Рисунок 3 – Стрілками показані хламідії (C. trachomatis) на різних стадіях розвитку: ЕТ – елементарне тільце, ПТ – проміжне
Рисунок 3 – Стрілками показані хламідії (C. trachomatis) на різних стадіях розвитку: ЕТ – елементарне тільце, ПТ – проміжне
тільце, РТ – ретикулярне тільце
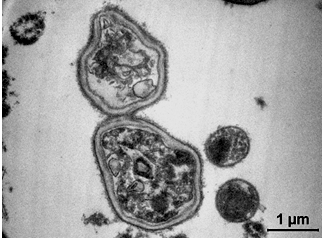 Рисунок 4 – Гриби роду Candida, що утворюють бруньки
Рисунок 4 – Гриби роду Candida, що утворюють бруньки
Для генотипування використано 49 зразків, отриманих від хворих, в яких методом ПЛР було виявлено ДНК T. vaginalis. Провести генотипування вдалося у 29 клінічних зразках – 14 зразків було отримано від пацієнтів в м. Харкові та 15 – у м. Києві. За гендером було 11 (37,9 %) чоловіків та 18 (62,1 %) жінок, середній вік їх склав (31,2 ± 3,5) року. У зразку на рис. 5 водночас із типовою картиною, характерною для генотипу Е, відзначається додаткова полоса довжиною 519 п.н. після дії рестриктази MseI, що є характерним для генотипу А, що стало підґрунтям для висновку про присутність двох генотипів – А та Е.
Зразки з північно-східного (Харків) та центрального (Київ) регіонів України, практично не відрізнялися. В українській популяції домінував генотип Е (69,0 %) при меншій частоті виявлення генотипів G (21,4 %), H (14,3 %) та А (3,5 %). Не вдалося виявити зв’язок будь-яких особливостей клінічної картини трихомонозу з генотипом Trichomonas vaginalis.
При вивченні статевої поведінки молодих осіб ([23 ± 1] рік), що мали вищу освіту та гетеросексуальну орієнтацію, показано, що 90 % з них є неодруженими. Майже всі з респондентів (98 %) мали більше одного статевого партнера за життя (у середньому 12 осіб у чоловіків та 5 – у жінок). Анальний секс регулярно використовували 33 % досліджуваних осіб. Оральний секс регулярно використовували 74 % досліджуваних осіб. Сексуальне спілкування з випадковими сексуальними партнерами мали 64 % з анкетованих. При цьому використовували бар’єрні засоби при традиційних статевих стосунках 92 % респондентів, у той час, як при анальних зносинах – 79 %, а при оральному сексі – 16,3 %. Низький рівень застосування презервативів є свідченням того, що оральний та анальний секс практично не сприймається як можливість отримання чи передачі статевих інфекцій. Існуючий стереотип сексуальної поведінки позначається на характері перебігу ІПСШ, зокрема виникненні генітально-екстрагенітальних інвазій різними видами трихомонад та лямбліями.
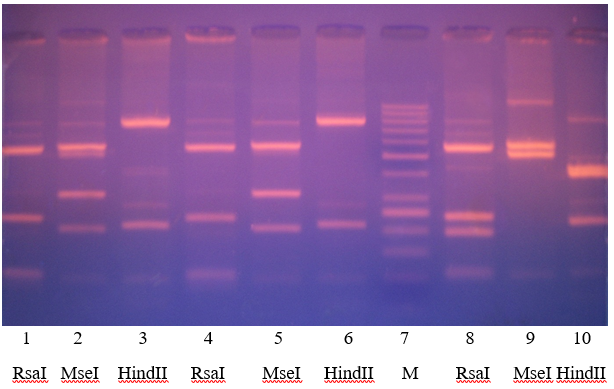 Рисунок 5 – Електрофореграма фрагментів ДНК, отриманих після рестрикції амплікону гена актину T. vaginalis. 1-3 полоси – зразок 1, генотипи А+Е; 4-6 полоси – зразок 2, генотип Е; полоса 7– маркери молекулярної маси 50 – 1000 п.н. (M); полоси 8-10 – зразок 3, генотип G. 1, 4, 8 полоси – рестриктаза RsaI; 2, 5, 9 полоси – рестриктаза MseI; 3, 6, 10 полоси – рестриктаза HindII
Рисунок 5 – Електрофореграма фрагментів ДНК, отриманих після рестрикції амплікону гена актину T. vaginalis. 1-3 полоси – зразок 1, генотипи А+Е; 4-6 полоси – зразок 2, генотип Е; полоса 7– маркери молекулярної маси 50 – 1000 п.н. (M); полоси 8-10 – зразок 3, генотип G. 1, 4, 8 полоси – рестриктаза RsaI; 2, 5, 9 полоси – рестриктаза MseI; 3, 6, 10 полоси – рестриктаза HindII
При порівнянні лабораторних методів діагностики при виявленні різних видів трихомонад Trichomonas vaginalis за допомогою культурального методу була ідентифікована у 15 ([15,5 ± 3,7] %) з 97 досліджуваних пацієнтів. Разом з тим, за допомогою методу ПЛР-РЧ Trichomonas vaginalis було виявлено у 6 ([6,2 ± 2,4] %) осіб. Trichomonas tenax виявлено, відповідно, у 9 ([9,3 ± 2,9] %) осіб, а Pentatrichomonas hominis – у 12 ([12,4 ± 3,3] %). При засівах за Trichomonas vaginalis помилково приймають Trichomonas tenax та Pentatrichomonas hominis. Trichomonas tenax – мікроорганізм, що існує в ротовій порожнині, а Pentatrichomonas hominis – у кишківнику людини. А відтак, не може бути виключена можливість реінфекції трихомонозу при практиці “альтернативного сексу”. Одночасне використання праймерів для виявлення Trichomonas vaginalis, Trichomonas tenax та Pentatrichomonas hominis за допомогою методу ПЛР-РЧ є більш ефективним ([27,9 ± 9,6] %), ніж за допомогою культурального методу.
Щоб довести специфічність оригінальних праймерів, було проведене секвенування ампліконів, отриманих від 62 пацієнтів. Нуклеотидні послідовності, що були секвеновані, абсолютно співпадали з нуклеотидними послідовностями саме Trichomonas tenax, Pentatrichomonas hominis або Gіardia lamblia (рис. 6).
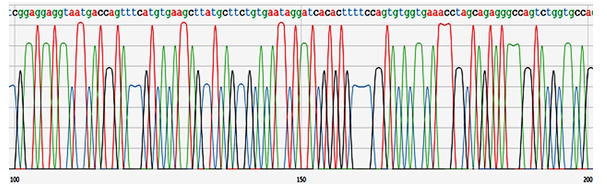 Рисунок 6 – Приклад результатів секвенування генетичного матеріалу, визначеного за допомогою авторського праймеру як Pentatrichomonas hominis. Таким чином, показана можливість використання в медичній практиці авторських праймерів
Рисунок 6 – Приклад результатів секвенування генетичного матеріалу, визначеного за допомогою авторського праймеру як Pentatrichomonas hominis. Таким чином, показана можливість використання в медичній практиці авторських праймерів
для виявлення ДНК Trichomonas tenax, Pentatrichomonas hominis і Giardia lamblia.
Було вивчено можливість одночасної інвазії ССС трихомонадами різних видів. Трихомонадну інвазію було виявлено більше ніж у третини (38,9 %) зі 198 обстежених пацієнтів, хворих на ІПСШ із хронічним перебігом. «Trichomonas non vaginalis» було виявлено у 69 (34,8 %). Причому, у 41 (20,7 %) було діагностовано Trichomonas tenax, а у 28 (14,1 %) – Pentatrichomonas hominis. Рівень діагностування Trichomonas vaginalis у досліджуваній групі хворих склав лише 4 %. Таким чином, більшість випадків трихомонадної інвазії ССС (34,9 %) у обстежених пацієнтів була викликана «Trichomonas non vaginalis». При цьому встановлено існування явища антибіозу у формі конкуренції при трихомонадній інвазії ССС.
Детальне обстеження асоціації умовно-патогенних бактерій та збудників протозойних інвазій було проведено у 71 пацієнта, у яких попередньо були виявлені мікроорганізми, що асоційовані з БВ. Група складалася з 45 чоловіків (63,4 %) та 26 жінок (36,6 %). У 13 пацієнтів (18,3 %) було діагностовано Trichomonas tenax, у 10 чоловіків (22,2 % із усіх чоловіків) та у 3 жінок (11,5 % із усіх жінок). У 48 пацієнтів (67,6 %) було діагностовано Pentatrichomonas hominis – у 29 чоловіків (64,4 %) та 19 жінок (73,1 %). Trichomonas vaginalis – у 1 пацієнта, жінки (3,8 %). Giardia lamblia було виявлено у 9 пацієнтів (12,7 %), 6 чоловіків (13,3 %) та 3 жінок (11,5 %). Показники виявлення мікроорганізмів, асоційованих з БВ наведені в табл. 3.
Таблиця 3 – Виявлення мікроорганізмів, асоційованих із БВ, у ССС пацієнтів (n = 71)
| Види, таксономічні групи | Кількість хворих з позитивним результатом | |||||
| Загальна вибірка | Чоловіки | Жінки | ||||
| Абс. | % | Абс. | % | Абс. | % | |
| Enterobacteriaceae * | 13 | 18,3 ± 4,6 | 10 | 22,2 ± 6,2 | 3 | 11,5 ± 6,3 |
| Streptococcus spp. * | 11 | 15,5 ± 4,3 | 11 | 24,4 ± 6,4 | 0 | 0 |
| Staphylococcus spp. * | 8 | 11,3 ± 3,8 | 8 | 17,8 ± 5,7 | 0 | 0 |
| Gardnerella vaginalis/
Prevotella bivia / Porphyromonas spp. |
24 | 33,8 ± 5,6 | 17 | 37,8 ± 7,2 | 7 | 26,9 ± 8,7 |
| Eubacterium spp. * | 38 | 53,5 ± 5,9 | 29 | 64,4 ± 7,1 | 9 | 34,6 ± 9,3 |
| Sneathia spp./ Leptotrihia spp./ Fusobacterium spp. * | 4 | 5,6 ± 2,7 | 4 | 8,9 ± 4,2 | 0 | 0 |
| Megasphaera spp./
Veilonella spp. /Dialister spp. |
14 | 19,7 ± 4,7 | 10 | 22,2 ± 6,2 | 4 | 15,4 ± 7,1 |
| Lachnobacterium spp./
Clostridium spp. |
13 | 18,3 ± 4,6 | 9 | 20,0 ± 6,0 | 4 | 15,4 ± 7,1 |
| Mobiluncus spp./
Corynebacterium spp. * |
37 | 52,1 ± 5,9 | 35 | 77,8 ± 6,2 | 2 | 7,7 ± 5,2 |
| Peptostreptococcus spp. | 20 | 28,2 ± 5,3 | 16 | 35,6 ± 7,1 | 4 | 15,4 ± 7,1 |
| Atopobium vaginae | 4 | 5,6 ± 2,7 | 1 | 2,2 ± 2,2 | 3 | 11,5 ± 6,3 |
| Candida spp. | 49 | 69,0 ± 5,5 | 35 | 77,8 ± 6,2 | 14 | 53,8 ± 9,8 |
| Mycoplasma hominis | 1 | 1,4 ± 1,4 | 1 | 2,2 ± 2,2 | 0 | 0 |
| Ureaplasma (urealyticum + parvum) | 15 | 21,1 ± 4,8 | 8 | 17,8 ± 5,7 | 7 | 26,9 ± 8,7 |
| Mycoplasma genitalium | 1 | 1,4 ± 1,4 | 1 | 2,2 ± 2,2 | 0 | 0 |
| Всього ** | 71 | 100 | 45 | 100 | 26 | 100 |
Примітка. * – Процент виявлення відрізняється у чоловіків та жінок (p < 0,05); ** – у більшості хворих (61) були виявлені два і більше (до 9) досліджуваних збудників.
У жінок, що мають протозойні інвазії ССС, до складу МА найчастіше входять, як показало дослідження: Candida spp., Eubacterium spp., Mobiluncus spp./Corynebacterium spp., Gardnerella vaginalis/Prevotella bivia/ Porphyromonas spp. Має місце значна перевага частоти виявлення у чоловіків деяких мікроорганізмів, асоційованих з БВ, а саме: Enterobacteriaceae, Streptococcus spp., Staphylococcus spp,. Gardnerella vaginalis/Prevotella bivia/Porphyromonas spp., Eubacterium spp., Sneathia spp./Leptotrihia spp./Fusobacterium spp., Mobiluncus spp./Corynebacterium spp., Peptostreptococcus spp. Гендерні відмінності в частоті виявлення вказаних мікроорганізмів можуть вказувати на їх пристосування до ССС чоловіків.
При розробці метода лікування протозойних інвазій ССС були проаналізовані дані обстежень 106 хворих, серед них 45 (42,5 %) чоловіків, середній вік яких становив (39,8 ± 3,3) року, та 61 жінка (57,5 %); середній вік жінок становив (28,4 ± 4,7) року. З цих хворих були сформовані основна група (77 пацієнтів) та група порівняння (29 пацієнтів). Хворим основної групи застосовувалися послідовно: секнідазол по 2,0 г 1 раз на добу протягом 5 днів; препарат, що містить 0,5 г орнідазолу та 0,5 г ципрофлоксацину, – по 1 таблетці 3 рази на день при вазі більше 70 кг (або 2 рази на день при вазі менше 70 кг) протягом 10 днів. Група порівняння отримувала метронідазол по 500 мг два рази на добу протягом 7–10 днів на тлі традиційної патогенетичної терапії згідно з існуючими протоколами лікування МОЗ та Європейського союзу.
В основній групі (77 пацієнтів) клінічний ефект (повне завершення клінічних проявів – болі, свербіння, виділення з геніталій) спостерігався у 71 (92,2 %) хворих. Клінічні прояви зберігалися у 6 пацієнтів, хоча вираженість симптомів істотно зменшилася. Позитивний мікробіологічний ефект лікування отримано у 74 (96,1 %) хворих основної групи. У трьох пацієнтів були знову виявлені трихомонади та/або гіардії. Усі вони заперечували статеві зв’язки після лікування. У групі порівняння (29 пацієнтів) клінічний і мікробіологічний ефект був, відповідно, 23 (79,3 %) і 24 (82,8 %) (табл. 4).
Таблиця 4 – Клінічний і мікробіологічний ефект лікування протозойних інвазій ССС
| Групи обстеження | Усього | Зникнення симптомів | P. hominis, T. tenax, G. lamblia не виявлені | |||
| Абс. | % | Абс. | % | Абс. | % | |
| Основна група (секнідазол + орнідазол + ципрофлоксацин) | 77 | 100 | 71 | 92,2 ± 3,1 | 74 | 96,1 ± 2,2 |
| Група порівняння (традиційна терапія) | 29 | 100 | 23 | 79,3 ± 7,5 | 24 | 82,8 ± 7,0 |
| t-критерій (р) | t = 2,57 (р = 0,012) | t = 2,10 (р = 0,038) | ||||
Запропонований оригінальний метод лікування є ефективним, має задовільну переносимість та може бути рекомендованим для емпіричної терапії уражень ССС, спричинених протозойними інвазіями T. tenax, P. hominis та G. lamblia.
Для врахування чутливості мікроорганізмів, що є асоційованими з БВ, до антибактеріальних препаратів у осіб із колонізацією сечостатевого тракту Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia використовувався структурно-логічний аналіз спеціальних літературних джерел. Отримані дані були оформлені у вигляді графічної інформаційної панелі даних відносно чутливості складових БВ до окремих антибактеріальних препаратів. Для перевірки ефективності використання графічної панелі при лікуванні хворих на ІПСШ було відібрано 128 осіб: 46 чоловіків (35,9 %) та 82 жінки (64,1 %), які у складі мікробіоти ССС мали мікроорганізми, що асоційовані з БВ. Середній вік пацієнтів становив (34 ± 2,5) року. Визначення якісного і кількісного складу мікроорганізмів, що асоційовані з БВ, виконувалося за допомогою методу ПЛР-РЧ та набору реагентів Фемофлор‑16. Після проведення індивідуалізованого лікування, що враховувало чутливість мікроорганізмів згідно даних панелі, погіршення стану мікробіоти ССС не реєструвалося в жодного з досліджуваних пацієнтів. Стан мікробіоти ССС (щодо анаеробних та мікроаерофільних мікроорганізмів) залишився без змін у 2 пацієнтів (1,6 %). Незначне покращення з боку ССС спостерігалось у 15 пацієнтів (11,7 %), 4 з яких були чоловіки (8,7 %) та 11 (13,4 %) – жінки. Значне покращення ССС відбулося після лікування у 37 пацієнтів (28,9 %), з них було 12 чоловіків (26,1 %) та 25 жінок (30,5 %). Повна нормалізація мікробіоти ССС відбулась у 74 осіб (57,8 %), з них було 30 чоловіків (65,2 %) та 44 жінки (53,7 %). Показано, що використання графічної інформаційної панелі при терапії хворих на ІПСШ, які в складі супутньої мікробіоти мали мікроорганізми, що асоційовані з БВ, підвищує ефективність лікування.
Для розробки лікування хворих на поєднанні протозойно-бактеріальні інфекції відібрано групу з 56 хворих на ІПСШ хронічного перебігу, 17 (30,4 %) чоловіків та 39 (69,6 %) жінок. Застосовувалися послідовно секнідазол (секнідокс), а також комбінація 0,5 г орнідазолу і 0,5 г ципрофлоксацину (орципол). Секнідокс призначався по 2,0 г 1 раз на добу протягом перших 5 днів лікування, орципол – з 6-го по 15-й день лікування по 1 таблетці 3 рази на день при масі тіла > 70 кг та 2 рази на день при масі тіла < 70 кг протягом 10 днів. У жінок лікування починалося відразу після припинення mensis. Вони отримували щоденно вагінальні спринцювання та піхвові таблетки з ніфуротелем і ністатином або одним з препаратів групи нітроімідазолів, а також піхвові свічки з хлоргексидином послідовно протягом 5–10 та 10 днів відповідно. За запропонованою схемою проліковано 56 хворих на ІПСШ. Забір матеріалу із ССС проводився через 1 місяць після припинення антибактеріальної терапії. У результаті лікування досягнуто елімінації трихомонад у 54 ([96,4 ± 2,5] %) осіб дослідної групи. Повної нормалізації рівня мікрофлори, асоційованої з БВ, досягнуто у 31 ([57,4 ± 6,6] %) хворих. Значне зменшення кількості цієї мікрофлори виявлено у решти 24 ([42,6 ± 6,6] %) пацієнтів. Запропонований оригінальний метод лікування досить ефективний, відносно задовільно переноситься хворими і його можна рекомендувати для емпіричної терапії поєднаних уражень ССС, спричинених трихомонадами та мікроорганізмами, асоційованими з БВ.
Ефективність лікування хворих на хронічні ІПСШ з використанням в якості імуномодулюючого препарату суміші α- і ß-дефенсинів вивчалась у 62 осіб, хворих на ІПСШ, на тлі імунодефіциту. У 32 з них (41,6 %) були виявлені протозойні інвазії. В дослідній групі було 22 (68,8 %) жінки та 10 чоловіків (31,2 %), віком від 20 до 48 років. Середній вік складав (32 ± 2,5) року. Усі хворі мали хронічний перебіг ураження ССС. Trichomonas tenax було виявлено у 12 пацієнтів дослідної групи (37,5 %), Pentatrichomonas hominis – у 18 (56,3 %), Trichomonas vaginalis – у 2 (6,2 %). Препарат уводився по 2 мл 1 раз на добу протягом 10 діб або 1 раз на 2 доби протягом 20 діб. Як видно з таблиці 5, у пацієнтів були змінені середньостатистичні показники імунограм. Етіотропну терапію було проведено з послідовним внутрішнім застосуванням орнідазолу та ніфуротелю, по 10 діб кожний. Повна елімінація збудників трихомонадної інвазії досягнута у 31 (96,9 %) особи. Вдалося добитися повної або часткової нормалізації показників імунограми. Тобто запропонований метод лікування є ефективним та може бути рекомендованим для емпіричної терапії уражень ССС, спричиненими протозойними інвазіями на тлі імунодефіциту.
Таблиця 5 – Показники імунограм досліджуваних пацієнтів до та після лікування (n = 32)
| Показник імунограми | Результат до лікування |
Результат після лікування | Референтні
значення |
| Абсолютна кількість лімфоцитів, х10 | *3,00 ± 0,45 | 2,3 ± 0,42 | 1,5 – 2,4 |
| Т-лімфоцити (CD3+), % | 45 ± 5,1 | 45 ± 5,3 | 40 – 67 |
| Т-хелпери (CD4+), % | 33 ± 4,4 | 33 ± 4,7 | 23 – 48 |
| Т-цитотоксичні лімфоцити (CD8+), % | *12 ± 1,7 | **18 ± 1,6 | 17 – 25 |
| Імунорегуляторний індекс Тх/Тс | *2,7 ± 0,81 | 2,0 ± 0,75 | 1,1 – 2,2 |
| Активні Т-лімфоцити, % | *13,1 ± 3,1 | **23 ± 2,2 | 22 – 39 |
| В-лімфоцити (CD22+), % | 30,2 ± 6,0 | 30 ± 6,1 | 15 – 35 |
| Лімфоцити-кілери (CD18+), % | 17,3 ± 3,6 | 17 ± 3,5 | 15 – 20 |
| 0-лімфоцити, % | *25,2 ± 4,3 | **18 ± 1,9 | 15 – 20 |
| Реакція бласттрансформації лімфоцитів з фітогемаглютиніном, % | 78,4 ± 10,1 | 78 ± 10 | 70 – 82 |
| IgG, г/л | 12,3 ± 1,9 | 13,2 ± 1,8 | 7,5 – 15,45 |
| IgА, г/л | 2,1 ± 0,2 | 2,1 ± 0,3 | 1,75 – 2,5 |
| IgМ, г/л | 0,9 ± 0,2 | 0,9 ± 0,2 | 0,65 – 1,65 |
| Фагоцитарний індекс, % | 64 ± 11 | 60 ± 11 | 40 – 80 |
| Фагоцитарний показник | 5,2 ± 0,7 | 5,8 ± 0,4 | 4 – 8 |
| НСТ-тест | 17,2 ± 3,2 | 17 ± 1,8 | 10 – 30 |
Примітка:
* – достовірність різниці показників відносно даних контрольної групи здорових осіб (p < 0,05); ** – достовірність різниці показників після лікування відносно даних до лікування (p < 0,05); n – кількість обстежених
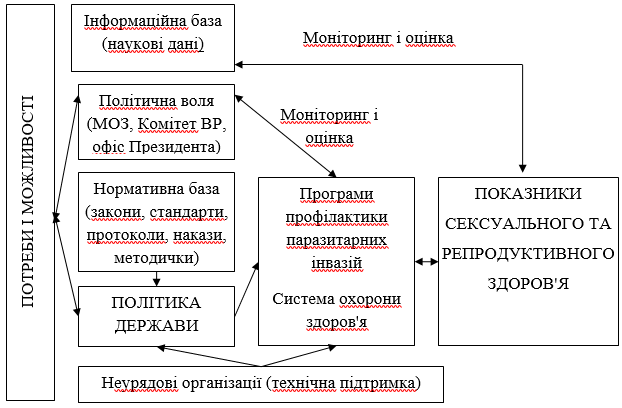
Для суспільної і особистої профілактики протозойних інвазій пропонується системна концепція і програма організаційних заходів з боротьби з сечостатевими інвазіями, що спричинені трихомонадами і лямбліями. Враховані рекомендації Глобальної стратегії ВООЗ з профілактики ІПСШ на 2015-2021 рр. Суттю стратегії є надання якісної допомоги хворим в рамках першого і другого рівнів медико-санітарної допомоги, а також спеціалізованих служб (третій і четвертий рівень). Якість медичної допомоги повинна оцінюватися в контексті системи охорони здоров’я в цілому. Увага до динамічної взаємодії між елементами структури визначає прийняття рішень протягом усіх етапів здійснення (рис. 7).
Рисунок 7 – Концепція профілактики генітальних паразитарних інвазій Trіchomonas vagіnalіs, а також Trichomonas tenax, Pentatrichomonas hominis і Gіardia lamblia
Створено рекомендації для індивідуальної профілактики протозойних реінвазій ССС, викликаних не Trichomonas vaginalis. А саме: проведення адекватної ерадикації збудників; санація власних екстрагенітальних осередків; санація генітальних та/або екстрагенітальних осередків у статевого партнера (партнерів); тривала відмова від сексуальних контактів без використання засобів бар’єрної контрацепції; нормалізація стану імунної системи. Для закладів охорони здоров¢я був рекомендований алгоритм (рис. 8) ведення пацієнтів при обстеженні їх на наявність статевої протозойної інвазії (Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Gіardia lamblia), а також алгоритм (рис. 9) маршруту пацієнтів ЛПЗ гінекологічного та урологічного профілю при наданні спеціалізованої допомоги з приводу статевої протозойної інвазії.
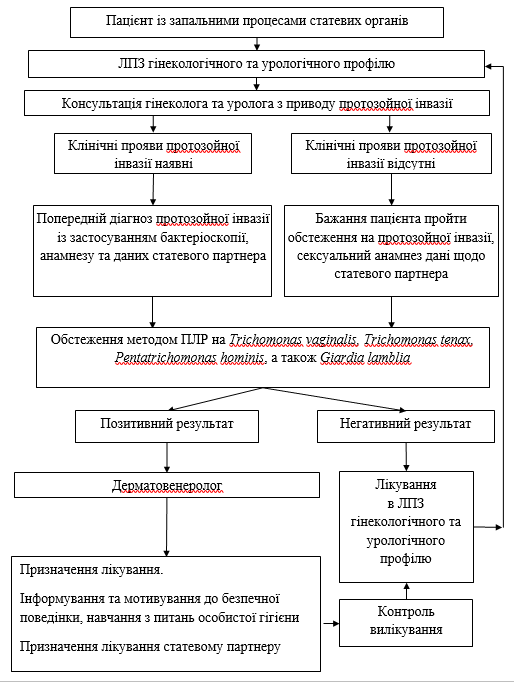
Рисунок 8 – Алгоритм (блок-схема) ведення пацієнтів при обстеженні їх на наявність статевої протозойної інвазії
Рисунок 9 – Алгоритм (блок-схема) маршруту пацієнтів лікувально-профілактичних закладів (ЛПЗ) гінекологічного та урологічного профілю при наданні спеціалізованої допомоги з приводу статевої протозойної інвазії.
ВИСНОВКИ
Запропоновано теоретичне обґрунтування та нове вирішення актуальної наукової і практичної проблеми сучасної дерматовенерології, що полягає в підвищенні ефективності діагностики, лікування, профілактики інвазій сечостатевої системи, спричинених Trichomonas vaginalis та іншими представниками типу найпростіших на підставі даних про їх епідеміологію, клініку, біологічні властивості збудників, морфопатогенез, а також про наявність супутньої колонізації умовно-патогенними збудниками.
- Значна поширеність, хронічний, рецидивуючий характер перебігу з можливістю виникнення тяжких ускладнень, недостатня вивченість механізмів патогенезу, негативні соціальні наслідки, а також недоліки в наданні медичної допомоги роблять проблему діагностики, лікування і профілактики протозойних інвазій сечостатевої системи актуальною для науки і практики та обумовлють необхідність її всебічного вивчення.
- Розроблено оригінальні праймери для виявлення Trichomonas tenax, Pentatrichomonas hominis і Giardia lamblia методом полімеразної ланцюгової реакції в модифікації «у реальному часі». Секвенування біологічного матеріалу, взятого від 62 пацієнтів, у яких було виявлено ДНК цих найпростіших показало відповідність оригінальних праймерів названим мікроорганізмам – тобто їх високу специфічність. Використання цих праймерів дозволяє виявляти протозойні інвазії сечостатевої системи удвічі ефективніше, ніж застосування культурального методу.
- Протозойні інвазії трапляються у 29 – 40% пацієнтів, з хронічним перебігом інфекцій, що передаються статевим шляхом. Поширеність Trichomonas tenax, Pentatrichomonas hominis та Gіardia lamblia залежить від груп обстежуваних пацієнтів, і становить, відповідно, 9,3 – 32%; 12,4 – 16,4% і 4,2 – 6%. Має місце тенденція до зниження реєстрації трихомонозу, але темпи зниження варіюють, залежно від місця проживання, вікового та гендерного складу популяції. Захворюваність є більшою серед жінок, особливо, у молодому віці. В ряді регіонів серед молоді 15-20 років, захворюваність знижується досить повільно. Статистичні дані щодо трихомонадної інфекції не відображають її поширеності внаслідок неповної реєстрації.
- Ультраструктурні особливості трихомонад та супутніх бактерій в хворих на трихомоноз свідчать про те, що округлі форми vaginalis є однією з вірулентних, а не дегенеративних форм, оскільки вони мають необхідну морфологічну організацію і здатні спричиняти патогенний вплив на макроорганізм. Структурні зміни, що спостерігаються в цитоплазмі округлих форм, вказують на зниження їх фізіологічної активності внаслідок несприятливих факторів.
- Розподіл генотипів vaginalis за поліморфізмом гена актину в українській популяції характеризується домінуванням генотипу Е (69,0 %) при порівняно низькій частоті виявлення генотипів G (21,4 %), H (14,3 %) та А (3,5 %). При цьому не було виявлено достовірної різниці у розподілі генотипів T. vaginalis у центральному та північно-східному регіонах України.
- Клініко-імунологічні показники пацієнтів хворих на інфекції, що передаються статевим шляхом з хронічним перебігом, вказують на імунну недостатність клітинної ланки імунітету в 41,6 %. Це слугує підґрунтям для призначення імуномодулюючої терапії, зокрема препарату суміші дефензинів, призначення якого призводить до часткової нормалізації показників імунограм.
- Протозойні інвазії сечостатевої системи в 92% випадків супроводжують мікроорганізми, асоційовані з бактеріальним вагінозом. У жінок це частіше: Candida spp., Eubacterium spp., Mobiluncus spp./Corynebacterium spp., Gardnerella vaginalis/Prevotella bivia/ Porphyromonas spp. У чоловіків переважають наступні мікроорганізми: Enterobacteriaceae, Streptococcus spp., Staphylococcus spp,. Gardnerella vaginalis/Prevotella bivia/Porphyromonas spp., Eubacterium spp., Sneathia spp./Leptotrihia spp./Fusobacterium spp., Mobiluncus spp./Corynebacterium spp., Peptostreptococcus spp. Гендерні відмінності в частоті виявлення вказаних мікроорганізмів вказують на їх пристосування до сечостатевої системи чоловіків. Тому можна розглядати Pentatrichomonas hominis, Trichomonas tenax і Giardia lamblia в якості важливих чинників бактеріального вагінозу в жінок, а також відповідного анаеробного та мікроаерофільного дисбіозу в чоловіків.
- Запропоновано метод комплексного лікування уражень сечостатевої системи, спричинених трихомонадами та лямбліями, в тому числі, при супутньому інфікуванні анаеробними та мікроаерофільними мікроорганізмами за рахунок послідовного призначення секнідазолу та препарату, що містить 0,5 орнідазолу та 0,5 ципрофлоксацину. Клінічне одужання наступило в 93 % випадків, бактеріологічна санація – в 97 %. За наявності імунодефіцитних станів запропоновано курс лікування з подовженим (до 20 діб) строком послідовного прийому двох протистоцидних препаратів різних фармакологічних груп – ніфуротелю та орнідазолу. Разом з тим, з метою імунокорекції, одночасно призначається препарат суміші α і ß-дефенсинів. Бактеріологічна санація досягається в 96,9 %.
- Розроблено і впроваджено сучасні алгоритми надання та організації надання медичної допомоги хворим на сечостатевий трихомоноз з урахуванням можливості виявлення різних видів трихомонад та лямблії для запобігання тяжких медичних і соціальних наслідків хронічного перебігу інвазії. Запропоновано комплекс дій для суспільної та індивідуальної профілактики реінвазій.
РЕКОМЕНДАЦІЇ
Для покращення ранньої діагностики інвазій Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis і Gіardia lamblia слід проводити інформаційно-роз’яснювальну роботу в групах ризику, доцільно використовувати молекулярно-біологічні методи (ПЛР) для виявлення означених збудників. Необхідно забезпечити реєстрацію відповідних хворих із зазначенням віку, статі, провідного синдрому і етіологічних даних, як у загальній популяції, так і серед окремих груп населення.
Слід дотримуватись алгоритму ведення хворих, що мають ризик розвитку ускладнень, рецидивів та реінфекцій. При наявності показань до лікування застосовувати розроблені методи лікування. В якості етіотропних засобів доцільно послідовно використовуватит секнідазол по 2 г 1 раз на день протягом 5 днів, потім 500 мг ципрофлоксацину + 500 мг орнідазолу 2-3 рази (залежно від маси тіла) в день протягом 10 днів. При хронічних, повторних випадках змішаної трихомонадної інвазії, а також з метою імунокорекції вводиться суміш α- і ß-дефенсинів внутрішньом’язово по схемі – 2 мл через день впродовж 20 днів, одночасно з курсом специфічної терапії протозойних інвазій. А саме, внутрішньо призначається орнідазол по 1,5 г на добу. Препарат приймається по 0,5 г тричі на добу після їди на протягом 10 діб. У перший день лікування добова доза орнідазолу вживається за один прийом під час вечері. Наступні 10 днів хворі мають отримувати по 400 мг ніфуротелю тричі на добу, незалежно від прийому їди. У разі необхідності, через 5 днів після початку специфічної антипротозойної терапії, призначаються додаткові антибактеріальні препарати з метою елімінації з урогенітальної системи інших збудників ІПСШ, не чутливих до ніфуротелю та орнідазолу. Крім того, чоловіки, у разі потреби, мають отримувати пальцьовий масаж передміхурової залози та ректальні протизапальні свічки. Жінкам рекомендовані щоденні вагінальні спринцювання та піхвові таблетки з ніфуротелем та ністатином, а також свічки з хлоргексидином послідовно протягом 8 та 10 днів, відповідно. Під час лікування пацієнтам заборонено мати сексуальні контакти, а в контрольний період – лише із застосуванням презервативів. Запропоновано комплекс рекомендацій для індивідуальної профілактики відповідних реінвазій: проведення адекватної ерадикації збудників протозойних інвазій сечостатевої системи; санація власних екстрагенітальних осередків протозойних інвазій; санація генітальних та/або екстрагенітальних осередків протозойних інвазій у статевих партнерів; тривала відмова від сексуальних контактів, включно з оральними та анальними, без використання засобів бар’єрної контрацепції; нормалізація стану імунної системи.
Скринінг і обстеження на паразитарну патологію, а також профілактична терапія нітроімідазолами та антибіотиками є важливими елементами, як індивідуальної профілактики рецидивів, так і суспільної профілактики ІПСШ в цілому.
СПИСОК ОПУБЛІКОВАНИХ ПРАЦЬ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
- Федорич П.В., Мавров Г.І. Поширеність протозойних інвазій при загостреннях хронічного запалення сечостатевої системи. Журнал дерматовенерології та косметології ім. М.О. Торсуєва. 2018.№2(40).С.37-42.
- Федорич П.В., Мавров Г.І., Зелений С.Б. Можливість використання авторських праймерів для детекції, Pentatrichomonas hominis, Trichomonas tenax, Giardia lamblia в біологічному матеріалі. Журнал дерматовенерології та косметології імені М.О. Торсуєва. 2019. № 2 (42). С. 7–11. (Здобувачем доведено можливість використання авторських праймерів для детекції, Pentatrichomonas hominis, Trichomonas tenax, Giardia lamblia в біологічному матеріалі, підготовлено статтю до друку).
- Федорич П.В. Трихомоніаз. Патоморфоз трихомонад. Військова медицина України. Т. 14, № 1. С. 62–67.
- Федорич П.В., Мавров Г.І., Зелений С.Б. Виявлення Pentatrichomonas hominis в сечостатевій системі людини методом полімеразної ланцюгової реакції. Військова медицина України. 2018. Т. 18, № 4. С. 49–54. (Здобувачем проведено аналіз визначення Pentatrichomonas hominis в сечостатевій системі пацієнтів, підготовлено статтю до друку).
- Федорич П.В. Індивідуальна профілактика протозойних реінвазій сечостатевої системи, викликаних не Trichomonas Vaginalis. Військова медицина України. 2019. Т. 19 (2). С. 66–68.
- Федорич П.В. Обґрунтування та апробація оригінального способу взяття біологічного матеріалу з метою адаптації діагностикума Фемофлор-16 для кількісної детекції анаеробної та мікроаерофільної мікрофлори сечостатевої системи чоловіків. Український науково-медичний молодіжний журнал. 2012. № 2. С. 155–158.
- Mavrov H.I., Osinska T.V., Fedorych P.V. Clinical and epidemiological characteristics and morphological peculiarities of urogenital trichomoniasis nowadays. Pathologia. 2020. Vol. 17, № 1 (48). P. 52–59. (Здобувачем проаналізовано літературні джерела, підготовлено статтю до друку).
- Федорич П.В. Урогенітальний трихомоноз: новий погляд на проблему. Дерматологія та венерологія. 2017. № 4 (78). С. 12–16.
- Федорич П.В. Виявлення Pentatrichomonas hominis при кольпоцервіциті та сальпінгоофориті. Дерматологія та венерологія. 2018. № 3 (81). С. 77–79.
- Ультраструктурные особенности морфотипов Trichomonas vaginalis, выделенных от больных с хронической трихомонадной инвазией / П.В. Федорич, Г.И. Мавров, С.К. Джораева, Т.В. Осинская. Дерматологія та венерологія. 2018. № 4 (82). С. 17–22. (Здобувачем здійснено відбір дослідної групи пацієнтів та забір біологічного матеріалу, аналіз отриманих даних, підготовлено статтю до друку).
- Молекулярное типирование Trichomonas vaginalis, циркулирующих в Украине,на основании полиморфизма гена актина / А.П. Белозоров, П.В. Федорич, Г.И. Мавров, А.Д. Зеленская, Е.Н. Горобчишина. Дерматологія та венерологія. 2019. № 1. С. 8–12. (Здобувачем здійснено відбір дослідної групи пацієнтів та забір біологічного матеріалу, аналіз отриманих даних, підготовлено статтю до друку).
- Сучасні епідеміологічні аспекти трихомонозу в Україні / П.В. Федорич, Г.І. Мавров, Т.В. Осінська, Л.В. Іващенко. Дерматологія та венерологія. 2020. № 1 (87). С. 44–51. (Здобувачем проаналізовано дані щодо епідеміологічних аспектів трихомонозу в Україні за 8 років, підготовлено статтю до друку).
- Федорич П.В., Мавров Г.І. Лікування генітальних інвазій, спричинених Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia. Дерматовенерологія. Косметологія. Сексопатологія. 2019. № 1–2. С. 5–10.
- Федорич П.В. Протозойні інвазії сечостатевої системи у поєднанні зі збудниками бактеріального вагінозу у жінок фертильного віку та їхніх статевих партнерів. Здоровье женщины. 2018. № 7 (133). С. 11–16.
- Федорич П.В., Мавров Г.І. Сучасна клініко-епідеміологічна характеристика хворих на сечостатевий трихомоноз в Україні. Український журнал дерматології, венерології, косметології. 2020. № 1. С. 15–23.
- Федорич П.В., Мавров Г.І. Випадок хронічного уретропростатиту при виявленні Chlamydia trachomatis та Trichomonas tenax. Здоров’я чоловіка. 2018. № 3 (66). С. 107–108.
- Визначення деяких найпростіших (Trichomonas tenax, Trichomonas hominis, Giardia lamblia, Entamoeba histolytica, Enthamoeba gingivalis) у пацієнтів, хворих на урогенітальні інфекції методом ПЛР в реальному часі / П.В. Федорич, С.Б. Зелений, Л.С. Зайцева, О.В. Мазій. Український журнал дерматології, венерології, косметології. 2012. № 4 (47). С. 5–10. (Здобувачем проаналізовано результати досліджень, підготовлено статтю до друку).
- Федорич П.В., Примак А.В., Коновалова Т.С. Бактеріальний вагіноз: сучасний погляд на проблему. Раціональна терапія та реабілітаційні заходи щодо способу життя пацієнток. Український журнал дерматології, венерології, косметології. 2013. № 3 (50). С. 86–94. (Здобувачем проаналізовано літературні дані, результати лікування, підготовлено статтю до друку).
- Федорич П.В. Кількісне визначення мікрофлори, асоційованої з бактеріальним вагінозом, у сечостатевій системі чоловіків. Український журнал дерматології, венерології, косметології. 2014. № 3 (54). С. 57–62.
- Визначення поширеності інфікування Giardia lamblia сечостатевої системи хворих з інфекціями, що передаються переважно статевим шляхом / П.В. Федорич, С.Б. Зелений, Л.Я. Федорич, Х.І. Шеховцова. Український журнал дерматології, венерології, косметології. 2015. № 2 (57). С. 67–70. (Здобувачем з¢ясовано поширеності інфікування Giardia lamblia в сечостатевій системі, підготовлено статтю до друку).
- Порівняння ефективності діагностики трихомоніазу за культуральним методом та методом полімеразної ланцюгової реакції з використанням праймерів для виявлення Trichomonas vaginalis, Trichomonas tenax та Pentatrichomonas hominis / П.В. Федорич, С.Б. Зелений, О.А. Садовська, К.В. Дудікова. Український журнал дерматології, венерології, косметології. 2017. № 1 (64). С. 65–69. (Здобувачем проведене порівняння різних діагностичних методик при підозрі на протозойну інвазію сечостатевої системи, підготовлено статтю до друку).
- Федорич П.В. Випадок хронічного баланопоститу при виявленні Pentatrichomonas hominis. Український журнал дерматології, венерології, косметології. 2018. № 4 (70). С. 136–138.
- Protozoan genital invasions caused by the representatives of Trichomonas and Giardia / P.V. Fedorych, G.I. Mavrov, T.V. Osinska, Y.V. Shcherbakova. Wiadomości Lekarskie. Vol. 73, Iss. 2. P. 380–383. (Здобувачем проаналізовано результати лікування, підготовлено до друку).
- Клинический случай инвазии Trichomonas vaginalis беременной женщины и ее новорожденной / Г.И. Мавров, Т.В. Осинская, П.В. Федорич, Л.В. Гречанская. Georgian Medical News. 2019. № 12 (297). С. 41–46. (Здобувачем проаналізовано результати лікування, підготовлено до друку).
- FedorychDiagnostics and treatment of genital invasion caused by Trichomonas vaginalis and possibly other related species (Pentatrichomonas hominis and Trichomonas tenax) in patients with immunodeficiency. Georgian Medical News. 2020. No 12 (309). P. 81–85.
- Fedorych P.V., Mavrov G.I. The role of protozoal infestations in chronic inflammation exacerbations in patients with genitourinary pathology. EURYKA: Health Science. No. 5. P. 28–33.
- Fedorych P.V., Mavrov G.I. Incidence of Sexually Transmitted Infections: Local Study in Ukraine. World Science. Vol. 2, Iss. 8 (36). P.4–7.
- Федорич П.В., Мацас Е.Ю., Мулькина Е.И. Применение диагностикума Фемофлор для исследования микрофлоры мочеполовой системы у пар половых партнёров при наличии воспаления. Уральский медицинский журнал. 2011. № 3 (81). С. 26–32. (Здобувачем виконано взяття біологічного матеріалу із сечостатевої системи хворих та проаналізовано результати дослідження, написано частину статті).
- Федорич П.В., Зеленый С.Б. Трихомониаз. Явление существования Trichomonas tenax в мочеполовой системе человека. Уральский медицинский журнал. № 1 (115). С. 93–97. (Здобувачем виконано взяття біологічного матеріалу із сечостатевої системи хворих та проаналізовано результати дослідження, написано статтю).
- Федорич П.В., Зеленый С.Б. Трихомониаз. Явление существования Trichomonas hominis в мочеполовой системе человека. Медицинская панорама. 2014. № 1 (145). С. 59–61. (Здобувачем виконано взяття біологічного матеріалу із сечостатевої системи хворих та проаналізовано результати дослідження, написано статтю).
- Федорич П.В. Вопросы рациональной методологии и диагностики урогенитальных инфекций у мужчин. Дерматовенерология и эстетическая медицина. 2014. № 2 (22). С. 56–59.
- Федорич П.В. Определение микрофлоры, ассоциированной с бактериальным вагинозом, в мочеполовой системе мужчин методом полимеразной цепной реакции в реальном времени. Военная медицина. 2015. №1. С. 57–60.
- Федорич П.В., Корнієнко А.О., Федорич Л.Я. Бактеріальний вагіноз. Огляд літературних джерел. Український журнал дерматології, венерології, косметології. 2008. № 3 (30). С. 102–105. (Здобувачем проаналізовано літературні джерела, підготовлено статтю до друку).
- Федорич П.В., Зеленый С.Б. Трихомониаз. Выявление Trichomonas tenax и Pentatrichomonas hominis в мочеполовой системе женщин репродуктивного возраста, больных инфекциями, передающимися преимущественно половым путем. Здоровье женщины. 2014. № 3 (89). С. 167–170. (Здобувачем проведено визначення трихомонад різних видів в сечостатевій системі жінок фертильного віку, підготовлено до друку).
- Федорич П.В. Діагностика та лікування поєднаних уражень сечостатевої системи трихомонадами різних видів і мікроорганізмами, асоційованими з бактеріальним вагінозом. Лікарська справа. 2018. № 5–6. С. 100–111.
- Федорич П.В. Явище антибіозу при трихомонадній інвазії сечостатевої системи. Медичні аспекти здоров’я чоловіка. 2018. № 2 (29). С. 19–21.
- Аналіз сексуальної поведінки сучасних молодих осіб із вищою освітою / П.В. Федорич, В.П. Філіпішин, Л.Я Федорич., І.Г. Миколюк, Мехмет Бюлент Багчі. Сучасні аспекти військової медицини. Збірник наукових праць. К., 2013. Вип. 20. С. 328–334. (Здобувачем розроблено анкету, проаналізовано особливості сексуальної поведінки молоді, підготовлено статтю до друку).
- Федорич П.В., Мавров Г.І., Осінська Т.В. Лікування протозойних інвазій сечостатевої системи викликаних Pentatrichomonas hominis, Trichomonas tenax та Giardia lamblia. Проблеми військової охорони здоров¢я: Збірник наукових праць Української військово-медичної академії 2019. № 52. С. 290–298. (Здобувачем обґрунтовано та успішно використано новий метод лікування уражень сечостатевої системи збудниками протозойних інвазій, підготовлено статтю до друку).
- Федорич П.В. Особливості інфекцій, що передаються статевим шляхом, в Україні. Український медичний вісник. 2013. № 7–8 (82). С. 62–63.
- Fedorych P.V. Study of incidence ofmainly sexually transmitted infections in Ukraine. 13th EADV Spring Symposium. Athens, Greece, 19–22 may 2016. P. 0774.
- Федорич П.В. К вопросу о возможности колонизации мочеполовой системы человека Trichomonas tenax и Pentatrichomonas hominis. Матеріали Науково-практичної конференції НМАПО ім. П.Л. Шупика «Місце дерматовенерології в міждисциплінарному вирішенні питань діагностики та лікування хронічних захворювань», м. Київ, 20–21 березня 2017 р. С. 117–118.
- Типування Trichomonas vaginalis в Україні, на підставі поліморфізму гена актину /А.П. Белозоров, П.В. Федорич, Г.І. Мавров, А.Д. Зеленська. Матеріали Всеукраїнської науково-практичної конференції з міжнародною участю «Досягнення та перспективи в сучасній дерматовенерології: Європейський та український досвід, взаємодія науки та практики», 21–22 листопада 2019 р., м. Харків. Дерматологія та венерологія. 2019. № 3 (85). С. 51–52. (Здобувачем відібрано групу та взято матеріал для проведення дослідження).
- Федорич П.В., Мавров Г.І., Зелений С.Б. Апробація праймерів для виявлення Pentatrichomonas hominis в сечостатевій системі людини методом ПЛР. Матеріали науково-практичної конференції з міжнародною участю НМАПО ім. П.Л. Шупика «Дерматовенерологія в розробках молодих науковців», м. Київ, 22 листопада 2018 р. С. 44-45. (Здобувачем виконано взяття біологічного матеріалу із сечостатевої системи хворих та проаналізовано результати дослідження, написано тези).
- Пат. на винахід 107910 Україна, МПК С12/Q 1/68 (2006.01), С12/Q 1/04 (2006.01), С12/N15/11 (2006.01). Спосіб визначення присутності Trichomonas tenax у досліджуваному зразку та набір праймерів для його здійснення / Федорич П.В., Зелений С.Б. – заявники та патентовласники. – а201407161; заявл. 25.06.2014; опубл. 25.02.15, Бюл. № 4.
- Пат. на корисну модель. 103397 Україна, МПК А61К 31/345 (2006.01),А61К 31/7080 (2006.01),А61/Р 17/04 (2006.01). Спосіб лікування хронічного трихомоніазу / Федорич П.В. – заявник та патентовласник. – u201506813; заявл. 09.07.2015; опубл. 10.12.15, Бюл. №23.
- Пат. на винахід 110759 Україна, МПК С12/Q 1/68 (2006.01),С12/Q 1/04 (2006.01),С12/N15/11 (2006.01), С12/R 1/90(2006.01). Спосіб визначення присутності Pentatrichomonas hominis у досліджуваному зразку та набір праймерів для його здійснення / Федорич П.В., Зелений С.Б. – заявники та патентовласники. – а201501255; заявл. 16.02.2015; опубл. 10.02.16, Бюл. №3.
- Пат. на винахід 110767 Україна, МПК С12/Q 1/68 (2006.01),С12/Q 1/04 (2006.01),С12/N15/11 (2006.01), С12/R 1/90(2006.01). Спосіб визначення присутності Giardia lamblia у досліджуваному зразку та набір праймерів для його здійснення / Федорич П.В., Зелений С.Б. – заявники та патентовласники. – а201505750; заявл. 11.06.2015 ; опубл. 10.02.16, Бюл. №3.
- Пат. на корисну модель 109257 Україна, МПК А61К (2016.01),А61Р (2016.01). Спосіб лікування хронічного трихомоніазу сечостатевої системи, викликаного Trichomonas tenax або Pentatrichomonas hominis / Федорич П.В. – заявник та патентовласник. – u20151294; заявл. 21.12.2015; опубл. 25.08.16, Бюл. №16.
- Подольський Вл.В., Подольский В.В., Федорич П.В. Оптимізація лікування хронічних запальних захворювань статевих органів у жінок фертильного віку з урахуванням міжнародного досвіду: метод. рек. (№ 94/2017). К., 2018. 12 с.
АНОТАЦІЯ
Федорич П.В. Попередження медико-соціальних наслідків інвазій сечостатевої системи, спричинених трихомонадами та лямбліями – діагностика, комплексна терапія, профілактика. – Кваліфікаційна наукова праця на правах рукопису.
Дисертація на здобуття наукового ступеня доктора медичних наук за спеціальністю 14.01.20 — шкірні та венеричні хвороби. — Державна установа «Інститут дерматології та венерології НАМН України», Харків, 2021.
Виявлення Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia дозволяє проводити діагностику і лікування трихомонозу та других протозойних інвазій в сечостатевій системі. Враховуються також морфологічні, серологічні та ультраструктурні особливості цих найпростіших та інших учасників патологічних мікробних асоціацій, що ними утворюються. Це призводить до збільшення ефективності лікування і дозволяє проводити профілактику й зменшувати медико-соціальні наслідки відповідних патологій.
Ключові слова: трихомоноз, протозойні інвазії, сечостатева система,Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis,Giardia lamblia, діагностика, лікування, профілактика.
АННОТАЦИЯ
Федорич П.В. Предупреждение медико-социальных последствий инвазий мочеполовой системы, вызванных трихомонадами и лямблиями – диагностика, комплексная терапия, профилактика. – Квалификационный научный труд на правах рукописи.
Диссертация на соискание ученой степени доктора медицинских наук по специальности 14.01.20 — кожные и венерические болезни. — Государственное учреждение «Институт дерматологии и венерологии НАМН Украины», Харьков, 2021.
Выявление Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia позволяет проводить диагностику и лечение трихомоноза и других протозойных инвазий в мочеполовой системе. Учитываются также морфологические, серологические и ультраструктурные особенности этих простейших и других участников патологических микробных ассоциаций, образуемых ими. Это приводит к увеличению эффективности лечения и, как следствие, позволяет проводить профилактику и уменьшать медико-социальные последствия соответствующих патологий.
Ключевые слова: трихомоноз, протозойные инвазии, мочеполовая система, Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia, диагностика, лечение, профилактика.
ABSTRACT
Fedorych P.V. Prevention of Medical and Social Consequences Caused with Genitourinary Invasions by Trichomonas and Lamblias: Diagnostics, Comprehensive Therapy, Prevention. – Qualifying scientific work as the manuscript.
Thesis for a Scientific Degree of the Doctor of Medical Science by specialty 14.01.20 – Skin and Venereal Diseases. – State Establishment «Institute of Dermatology and Venereology of NAMS of Ukraine», Kharkiv, 2021.
The scientific novelty lies in the fact that today the patients with protozoan genitourinary invasions have several pathogens, namely: Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia. Significant prevalence of Giardia lamblia, Trichomonas tenax, and especially Pentatrichomonas hominis in the genitourinary system of patients with chronic sexually transmitted diseases (STDs) has been shown for the first time ever. It has been proved that Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia play an important role in the course and pathogenesis of chronic STDs at the present stage. Primers for the DNA detection of Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia in biological fluids have been developed and obtained in Ukraine for the first time. The correspondence of the primers to individual parts of the genome of the corresponding microorganisms has been confirmed by sequencing. Epidemiological patterns of Trichomonas genitourinary invasion, namely, the prevalence of Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis and Gardia lamblia, as well as their distribution factors have been established; the characteristics of sexual behavior of patients with STDs and their partners have been analyzed to identify the anatomical loci of infection. Peculiarities of the clinical course of venereal trichomoniasis in modern conditions are described, namely, the availability of genital and extragenital foci, the frequency of recurrences, depending on additional colonization of the urogenital tract with Trichomonas tenax, Pentatrichomonas hominis and Giardia lamblia, and with opportunistic, mainly anaerobic and microaerogenic bacteria. Microscopic, culture diagnostics and polymerase chain reaction have been compared in the context of Trichomonas detection in genitourinary system of patients with STDs. Relation between certain immune status disorders and presence of some protozoal invasions in human urogenital system has been revealed for the first time. For the first time, relation between protozoal genitourinary invasions and presence of bacterial vaginosis in women and dysbiotic (anaerobic and microaerophilic dysbacteriosis of genitourinary system) condition in men has been demonstrated. For the first time, molecular typing of Trichomonas vaginalis circulating in Ukraine has been performed on the basis of actin gene polymorphism. An electronic microscopy of affected tissues of the patients with trichomoniasis has been carried out. For the first time, clinical and laboratory data on pathogenicity of the oval morphotype Trichomonas vaginalis have been obtained. For the first time, a comprehensive method of treating the patients with protozoal genitourinary invasions (caused by Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia) has been scientifically substantiated and its efficacy has been proved. For the first time, a modern algorithm for medical care to patients with urogenital trichomoniasis has been introduced, taking into account the methods that allow to detect and eliminate various types of Trichomonas and Lamblias from urogenital tract to prevent medical and social consequences of this invasion. The practical significance of the obtained results is the original primers developed and offered for DNA detection of Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia (current pathogens of protozoal genitourinary invasions) by real time PCR for general medical practice. New methods of combined treatment of patients with protozoal genitourinary invasions caused by both Trichomonas vaginalis and other agents of protozoal invasions, namely, Trichomonas tenax, Pentatrichomonas laminia, Giardia lamblia, including in combined lesions with the microflora associated with bacterial vaginosis (anaerobic and microaerophilic), and on the background of immune disorders, have been developed, scientifically substantiated and introduced into the general medical practice. A system-based concept and a program of preventive and organizational measures to combat genitourinary invasions caused by Trichomonas and Lamblias have been offered. Recommendations for individual prophylaxis of protozoal genitourinary reinvasions caused by non–Trichomonas vaginalis have been developed.
Keywords: trichomoniasis, protozoal invasions, genitourinary system, Trichomonas vaginalis, Trichomonas tenax, Pentatrichomonas hominis, Giardia lamblia, diagnostics, therapy, prevention.