Державна установа «Інститут дерматології та венерології
Національної академії медичних наук України»
Кваліфікаційна наукова
праця на правах рукопису
Бронова Ірина Михайлівна
УДК 616.53-002-036.87-092-035-085
ДИСЕРТАЦІЯ
ОПТИМІЗАЦІЯ ТЕРАПЕВТИЧНИХ КОМПЛЕКСІВ ХВОРИХ НА АКНЕ
З УРАХУВАННЯМ КЛІНІЧНИХ ПРОЯВІВ, ДИНАМІКИ МОРФОФУНКЦІОНАЛЬНОГО СТАНУ І МІКРОБІОЦЕНОЗУ ШКІРИ
14.01.20 – шкірні та венеричні хвороби
Подається на здобуття наукового ступеня кандидата медичних наук
Дисертація містить результати власних досліджень. Використання ідей, результатів і текстів інших авторів мають посилання на відповідне джерело
__________________________________________________________________
(підпис, ініціали та прізвище здобувача)
Науковий керівник: Кутасевич Яніна Францівна, доктор медичних наук, професор
Харків – 2018
АНОТАЦІЯ
Бронова І.М. Оптимізація терапевтичних комплексів хворих на акне з урахуванням клінічних проявів, динаміки морфофункціонального стану і мікробіоценозу шкіри. – Кваліфікаційна наукова праця на правах рукопису.
Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 14.01.20 «Шкірні та венеричні хвороби». – Державна установа «Інститут дерматології та венерології НАМН України», Харків, 2018.
Наукова робота присвячена підвищенню ефективності лікування пацієнтів з акне середнього та тяжкого ступеня шляхом уточнення показань до призначення системних ретиноїдів, поєднання їх із системними і топічними антибактеріальними засобами, а також засобами профілактики очікуваних побічних ефектів на підставі поглибленого вивчення механізмів дії системних ретиноїдів.
Задачами дослідження було: вивчити сучасні клініко-епідеміологічні особливості акне, динаміку регресу клінічних ознак захворювання, комплаєнтність хворих на акне та її вплив на ефективність терапії, динаміку регресу дерматоскопічних ознак дерматозу, особливості психоемоційних порушень та дослідити вплив терапії системними ретиноїдами на психічний стан хворих на акне, дослідити динаміку мікробіоценозу шкіри у хворих на акне до, впродовж та після закінчення терапії системними ретиноїдами та комбінацією з системними та топічними антибактеріальними засобами і розробити оптимальні терапевтичні комплекси та режими їх застосування залежно від клінічної форми та ступеня тяжкості дерматозу, а також комплекс косметологічного супроводу хворих на акне в процесі терапії та під час ремісії; вивчити патогістологічні зміни у шкірі хворих на акне, а саме процеси проліферації та апоптозу епітеліоцитів і визначити морфометричні особливості епідермоцитів у процесі саногенезу.
Було застосовано наступні методи дослідження: клінічні (постановка діагнозу, визначення ступеня тяжкості перебігу дерматозу, контроль ефективності лікування); мікробіологічні (комплексна мікроскопічна та культуральна оцінка мікробіоценозу шкіри); імуногістохімічні та патоморфологічні (вивчення змін патогістологічної картини шкіри у процесі саногенезу), клініко-інструментальні: дерматоскопія (вивчення дерматоскопічних ознак дерматозу), психометричні (вивчення ступеня тривожності у пацієнтів з акне); статистичні.
У зв’язку зі значною поширеністю акне, збільшенням тяжких форм захворювання, невизначеністю окремих ланок патогенезу, що веде до певної емпіричності вибору терапевтичних комплексів та режимів їх проведення, актуальним залишається вивчення морфофункціональних особливостей змін у шкірі на різних етапах розвитку захворювання, а також розробка комплексних методів лікування хворих, особливо на тяжкі форми акне, методів оцінки його ефективності, створення програми косметологічного супроводу лікування та вторинної профілактики захворювання і його ускладнень.
Особливістю середньотяжких та тяжких форм акне є те, що вони досить часто (40,1 %) спостерігаються у віці старше 23 років та превалюють серед чоловіків (67,2 %). Тривале попереднє лікування цих хворих здебільшого включало використання лише антибактеріальних засобів чи системних ретиноїдів занадто короткими курсами, що не приводило до одержання стійкого терапевтичного ефекту.
При вивченні динаміки регресу елементів висипки доведено доцільність при наявності вузлів додавання системних антибіотиків до системних ретиноїдів. При наявності значної кількості пустульозних елементів, але відсутності вузлів, достатньо додавати топічні антибіотики, а при непереносимості, довготривалому використанні, неефективності на попередніх етапах лікування антибіотиками системні ретиноїди здатні забезпечити як клінічний, так і мікробіологічний ефект, але більш повільними темпами.
Застосування епілюмінесцентного методу дослідження дозволяє встановити дерматоскопічні ознаки захворювання та демонструє можливості виявлення навіть незначних проявів запалення за відсутності виражених клінічних ознак, що об’єктивізує оцінку ефективності лікування та в певних випадках аргументує необхідність підтримуючої терапії або навіть продовження основного курсу лікування.
Встановлено наявність психоемоційних порушень у хворих на акне. При цьому мають місце гендерні відмінності: у чоловіків превалював низький (на 5,9 % більше, ніж у жінок), тоді як у жінок – високий і надвисокий рівні тривожності (більше на 23,9 %). Наявність психоемоційних зрушень є аргументом на користь необхідності призначення більш інтенсивного (із залученням системних ретиноїдів) лікування цієї категорії хворих. Недостатню комплаєнтність констатовано у 57,3 % хворих на тяжкі форми акне, що обумовило появу таких побічних ефектів терапії, як: ретиноїдний дерматит та ангуліт.
Встановлено особливості біоценозу поверхні шкіри хворих на акне, зокрема видовий склад стафілококової флори, який був до лікування представлений значною кількістю патогенних штамів (S. haemolyticus – до 57,9 %, S. aureus – до 5,9 %). Після лікування біоценоз характеризувався практичним зникненням патогенних штамів. Визначено високу чутливість виділених штамів до фузидієвої кислоти, лінкозамідів та тетрацикліну (відсоток чутливих штамів становив 90,5 %, 86,0 % та 69,8 % відповідно). Доведено, що у всіх досліджуваних групах у результаті лікування біоценоз поверхні шкіри нормалізувався. Якщо не використовувалися додаткові антибактеріальні засоби (ІІІ група), нормалізація наставала пізніше – після вилучення провідних патогенетичних ланок захворювання (фолікулярного гіперкератозу, гіперпроліферації епітелію, піхви волосяних фолікулів).
Дослідженням доведено, що показанням до залучення системних ретиноїдів до лікування хворих на акне є не тільки середньотяжкі та тяжкі форми захворювання, а й неефективність лікування лише антибактеріальними засобами, непереносимість топічних ретиноїдів, ознаки швидкого розвитку деформуючих рубцевих проявів, значні психоемоційні порушення, що призводять до розвитку депресивних станів, порушення комунікативних властивостей, погіршення соціалізації хворих.
При вивченні морфологічної характеристики шкіри хворих на акне встановлено, що на етапі папульозної висипки лімфоцитарний інфільтрат не містить нейтрофілів, тобто на цьому етапі відсутнє гнійне запалення. Інфільтрат здебільшого представлений CD8-лімфоцитами (Т-лімфоцити-супресори/цитолітики), що дозволяє розглядати його як автоімунний процес. Присутність CD8-лімфоцитів не дає розвитися процесу згідно зі «сценарієм гострого гнійного запалення». Гіперпроліферація епітелію, у першу чергу піхви волосяних фолікулів, виявляється значною кількістю епітеліоцитів, мічених Ki‑67 і є морфологічною ознакою патогномонічного клінічного симптому – фолікулярного гіперкератозу. Наявність цієї ознаки навіть через 6–8 тижнів лікування системними ретиноїдами, а також прояви апоптозу, лише через 3–5 місяців від початку лікування є аргументом необхідності тривалої терапії у хворих на тяжкі форми акне.
Вперше було вивчено динаміку морфологічних та імуногістохімічних змін шкіри та її придатків у процесі саногенезу у пацієнтів з акне, що отримували системні ретиноїди, визначено дерматоскопічні ознаки захворювання та їх динаміку в процесі лікування, уточнено показання до призначення системних ретиноїдів, визначено оптимальні режими їх використання, зокрема підтримуючої терапії, обґрунтовано необхідність таргетного косметологічного супроводу лікування хворих на середньотяжкі та тяжкі форми акне, надано оцінку ступеня тривожності хворих до та після лікування, дано оцінку динаміки біоти шкіри залежно від вживання системних ретиноїдів без чи із системними антибактеріальними препаратами або препаратами зовнішньої дії.
Розроблено, клінічно апробовано та впроваджено в практику спосіб лікування пацієнтів з акне середнього та тяжкого ступеня тяжкості, який включає призначення системних ретиноїдів та антибактеріальних препаратів системної чи зовнішньої дії та засобів, що запобігають розвитку побічних ефектів лікування системними ретиноїдами. Розширено показання до лікування системними ретиноїдами. Розроблено програму таргетного косметологічного супроводу лікування хворих на акне, рекомендації щодо проведення підтримуючої терапії системними ретиноїдами. Оцінено вплив порушень комплаєнтності на ефективність лікування.
Ключові слова: акне, системні ретиноіди, системні антибіотики, топічні антибіотики, мікробіоценоз, каспаза-3, Ki-67,CD4, CD8.
ABSTRACT
Bronova I.M. Optimisation of therapeutic complexes for acne patients with regard to clinical aspects, dynamics of morphofunctional state and microbiocenosis of skin. – Qualification research work as a manuscript.
Thesis for the Degree of Candidate of Medical Science on specialty 14.01.20 “Skin and Venereal Deseases”. – State Establishment “Institute of Dermatology and Venereology of NAMS of Ukraine”, Kharkiv, 2018.
This research work is dedicated to enhancement of treatment efficiency for moderate and severe acne patients whereby indications were elaborated to prescribe systemic retinoids, their combination with systemic and topical antibacterial agents, as well as preventive means against presumable side effects and maintenance therapy on the basis of in-depth study of modes of action of systemic retinoids.
Research tasks were: to study modern clinical and epidemiological features of acne, retrogressive dynamics of clinical signs of disease, acne patients’ compliance and its influence on therapy efficiency, retrogressive dynamics of dermatoscopic signs of dermatosis, distinctive features of psychoemotional derangements, and to investigate influence of therapy treatment with systemic retinoids on acne patients’ mental condition, to study dynamics of microbiocenosis of acne patients’ skin prior to, in the process of and after the termination of therapy treatment with systemic retinoids and their combination with systemic and topical antibacterial agents, and to develop optimal therapeutic complexes and modes of their application in relation to the clinical form and the severity level of dermatosis, as well as a complex of cosmetological support for acne patients in the process of the therapy treatment and during the remission; to study pathohistological changes in acne patients’ skin, in particular, the processes of proliferation and apoptosis of epitheliocytes and to identify the morphometric features of epidermal cells in the sanogenesis process.
The following research methods were applied: clinical (diagnosis, identification of dermatosis severity, monitoring of treatment efficiency); microbiological (comprehensive microscopic and cultural evaluation of skin microbiocenosis); immunohistochemical and pathomorphological (study of changes in the pathohistological state of the skin in the sanogenesis process), clinical and instrumental: dermatoscopy (study of dermatoscopic signs of dermatosis), psychometric (study of acne patients’ anxiety level); statistical.
In connection with abundance of acne cases, increase of severe forms of the disease, uncertainty of separate areas of pathogenesis which leads to certain empiricalness in the choice of therapeutic complexes and modes of their implementation, it still remains an important issue to study morphofunctional aspects of changes within the skin at different stages of the disease progression, as well as to develop comprehensive methods of patients’ treatment, especially in cases of severe forms of acne, methods of evaluation of the treatment efficiency, to create a program of cosmetological support for the treatment and that of secondary prevention of the disease and its complications.
One of the features of moderate-to-severe and severe forms of acne is that they are observed frequently enough (40,1 %) at the age of over 23 and prevail amongst males (67,2 %). Long-term prior treatment of such patients substantially included the use of only antibacterial agents or systemic retinoids within short-term courses which did not produce a stabile therapeutic effect.
The study of rash elements’ regression dynamics shows the expediency, in case of papules, to add systemic antibiotics to the treatment with systemic retinoids. In case of a significant amount of pustular elements but absence of papules, it would be sufficient to add topical antibiotics, and in case of intolerance, extended use, inefficiency of antibiotics at previous stages of treatment, systemic retinoids are capable of ensuring both clinical and microbiological effects but at slower rates.
The use of the epiluminescent research method for studying the dynamics of the disease symptoms found with the said method shows a possibility to detect even minor inflammations in the absence of obvious clinical signs which objectifies the assessment of the treatment efficiency and, in certain cases, justifies the necessity of the supportive therapy or even the continuation of the main course of treatment.
Psychoemotional disorders were found amongst acne patients, this being the case of gender differences: a low level of anxiety prevailed amongst males (5.9 % higher than that amongst females), whereas females showed high and extra-high levels of anxiety (23.9 % higher). The presence of the said psychoemotional disorders is a compelling argument in favour of sufficiently intensive treatment (that includes the use of systemic retinoids) of the above category of patients. The patients’ inadequate compliance was found in 57.3% of patients with severe forms of acne, which caused the onset of such complications of therapy as retinoid dermatitis and angulitis
Specific features were determined with regard to biocenosis of acne patients’ skin surface, in particular, species composition of staphylococcal flora which, prior to treatment, contained a significant amount of pathogenic strains (Staphylococcus haemolyticus up to 57.9 %, Staphylococcus aureus up to 5.9 %). After the treatment the biocenosis was characterised with practical disappearance of pathogenic strains. Antibiotic susceptibility of isolated strains was studied whereby high sensitivity to fusidic acid, lincosamides and tetracycline was shown (the percentages of resistant strains were 9.5, 14.0 and 30.2 respectively).
It was proven that in all the groups under study, the biocenose of skin surface became normalized. If no additional antibacterial agents (Group 3) were used, normalization occurred later, after the removal of major pathogenetic areas of the disease (follicular hyperkeratosis, hyperproliferation of epithelium, vagina of hair follicles).
The study has proven that the indications for using systemic retinoids for treatment of acne patients result not only from moderate and severe forms of the disease, but also from the ineffectiveness of treatment only with antibacterial agents, the intolerance to topical retinoids, the signs of rapid development of deforming scar appearances, the significant psychoemotional disorders that lead to the development of depression, affect sociability, socialization of patients.
While studying morphological characteristics of acne, it has been found that at the stage of the papular rash, the lymphocytic infiltrate does not contain neutrophils, i.e. at this stage purulent inflammation does not occur. And the fact that the infiltrate is mainly represented by CD8-lymphocytes (T-lymphocytes-suppressors/cytolytics), allows to consider it as an autoimmune process. Besides, the presence of CD8-lymphocytes probably prevents the development of the process (in acute purulent inflammation “scenario”). The hyperproliferation of epithelium, primarily the vagina of hair follicles, which is shown by the number of epitheliocytes marked as Ki-67, is a morphological sign of the pathognomonic clinical symptom – the follicular hyperkeratosis. This symptom persists for over 6 to 8 weeks of treatment with systemic retinoids, which is a compelling argument for the necessity of extended therapy as the signs of apoptosis (histochemical reaction to caspase-3) are seen at a later stage (in 3 to 5 months after the start of the treatment) and coincide with the period of clinical remission achievement.
For the first time dynamics of morphological and immunohistochemical changes in the skin and its appendages was studied in the process of sanogenesis amongst acne patients treated with systemic retinoids, dermatoscopic signs of the disease along with their dynamics in the course of treatment were identified, indications for the prescription of systemic retinoids were determined, optimal regimens were defined for their use, in particular, the supporting therapy, the necessity of the targeted cosmetological support for the treatment of moderate and severe acne patients is justified, the levels of anxiety of patients before and after the treatment were assessed, the dynamics of skin biota in relation to the use of systemic retinoids without or with systemic antibacterial drugs or quasi drugs was evaluated.
A method of treating patients suffering from moderate-to-severe acne was developed, clinically tested and practically implemented which includes administration of systemic retinoids and antibacterial agents of systemic or external action and means preventing the development of side effects of treatment with systemic retinoids. Indications for treatment with systemic retinoids were enlarged. A program of target cosmetological support for acne patients’ treatment was developed, recommendations for maintenance therapy with systemic retinoids were elaborated. Patients’ non-compliance was assessed in respect of the treatment efficiency.
Key words: acne, systemic retinoids, systemic antibiotics, topical antibiotics, microbiocenosis, caspase-3, Ki-67,CD4, CD8.
СПИСОК ОПУБЛІКОВАНИХ ПРАЦЬ ЗА ТЕМОЮ ДИСЕРТАЦІЇ
1. Бронова И.М. Акне, индуцированное приемом анаболических стероидов. Дерматологія та венерологія. 2015. № 1 (67). С. 89–92.
2. Кутасевич Я.Ф., Бронова И.М. Базовая и адъювантная терапия при тяжелых формах акне. Український журнал дерматології, венерології, косметології. 2015. № 2 (57). С. 74–79.
3. Губіна-Вакулик Г.И., Бронова И.М. Патогенетическая терапия акне и патоморфологические аспекты изменений кожи в процессе саногенеза. Актуальні проблеми сучасної медицини. 2017. Т. 17, вип. 2 (58). С. 98–108. (Здобувачем особисто сформульовано мету та завдання дослідження, проведено аналіз даних та їх узагальнення)
4. Імуногістохімічні особливості патогенезу акне та динаміка змін шкіри при застосуванні системних ретиноїдів у пацієнтів з тяжкими формами дерматозу / Г.І. Губіна-Вакулік, Я.Ф. Кутасевич, Р.В. Сидоренко, І.М. Бронова. Дерматологія та венерологія. 2018. № 1 (79). С. 22–26. (Здобувачем особисто сформульовано мету та завдання дослідження, проведено аналіз даних та їх узагальнення)
5. Бронова І.М. Особливості динаміки регресу елементів висипки у хворих на акне, що отримували різні види патогенетичної терапії. Медицина сьогодні і завтра. 2017. № 2 (75). С.83–88.
6. Бронова І.М. Оцінка ефективності лікування акне з урахуванням результатів обстеження за допомогою психометричної методики. Дерматологія та венерологія. 2016. № 2 (72). С. 56–62.
7. Кутасевич Я.Ф., Джораєва С.К., Бронова И.М. Акне: динамика изменений микробиоценоза в процессе саногенеза у пациентов, получающих системные ретиноиды. Дерматологія та венерологія. 2016. № 4 (74). С. 43–54. (Здобувачем проведено збір, статистичну обробку та підготовку статті до друку)
8. Бронова И.М. Проблемы общения с больными акне и пути их преодоления лечащим врачом. Дерматологія та венерологія. 2017. № 1 (75). С. 65–68.
9. Бронова И.М., Хатем С.М. Редкие нозологии: клинический случай синдрома Фавра-Ракушо. Дерматологія та венерологія. 2017. № 2 (76). С. 53–55. (Здобувачем проведено збір та обробку літературних даних, підготовку статті до друку)
10. Дерматоскопические признаки регресса элементов акне в процессе саногенеза / Я.Ф. Кутасевич, В.А. Савоськина, Ю.В. Щербакова, С.Н. Джораева, И.М. Бронова. League medica. 2017. № 2. Р. 11–14. (Здобувачем особисто проведено збір та обробку даних, сформульовано мету і проведена підготовка статті до друку)
11. Особенности динамики изменений кожи в процессе саногенеза у больных акне / Я.Ф. Кутасевич, Г.И. Губина-Вакулик, С.Н. Джораева, И.А. Маштакова, И.М. Бронова. Proceedings of the International Scientific Conference «Topical Issues of Science and Education», Warsaw (Poland), July 17, 2017. Warsaw, 2017. Vol. 4. P. 25–30. (Здобувачем особисто проведено збір та обробку даних, сформульовано висновки, зроблено підготовку статті до друку)
12. Кутасевич Я.Ф., Бронова И.М. Акне: непростая задача в практике клинициста. Здоров‘я України 21 сторіччя. 2016. № 6 (379). С. 76–77.
13. Пат. на корисну модель № 118999 UA, МПК А61К31/203, А61Р17/00, А61Р1/16, А61Q17/04. Спосіб лікування пацієнтів з акне середнього та тяжкого ступеня тяжкості / І.М. Бронова, Я.Ф. Кутасевич. № u201701391; заявл. 14.02.17; опубл. 11.09.17, Бюл. № 17.
14. Кутасевич Я.Ф., Маштакова І.О., Бронова І.М. Клінічні рекомендації щодо лікування акне (посібник для лікарів). Харків : ДУ «Інститут дерматології та венерології НАМН України», 2017. 10 с. (Здобувачем зроблено обробку літературних даних та підготовлено рекомендації до друку)
15. Бронова І.М. Особливості психосоматики у пацієнтів з акне, що знаходяться на різних видах комплексної терапії. ІІІ Міжнародний медичний конгрес «Впровадження сучасних досягнень медичної науки у практику охорони здоров’я України» : Матеріали конгресу, м. Київ, 15–17 квітня 2014 р. К., 2014. С. 85.
16. Коморбидная патология у группы пациентов со средней степенью тяжести акне / Я.Ф. Кутасевич, И.А. Олейник, И.А. Маштакова, В.Ю. Мангушева, И.М. Бронова. Матеріали Всеукраїнської наук.-практ. конф. за участю міжнародних спеціалістів «Сучасні технології в рішенні організаційних, епідеміологічних, клінічних та діагностичних задач дерматовенерології», яка присвячена 80-річчю кафедри дерматовенерології Донецького національного медичного університету ім. М. Горького, 13 червня 2014 р., м. Донецьк. Журнал дерматовенерології та косметології ім. М. О. Торсуєва. 2014. № 1–2 (32). С. 133. ( Здобувачем зроблено обробку даних, сформульовано мету, підготовано тези до друку)
17. Кутасевич Я.Ф., Бронова І.М. Сучасні аспекти лікування акне у жінок репродуктивного віку. Материалы научно-практической конференции с участием международных специалистов «Инновационные технологии в дерматовенерологии. Междисциплинарные связи», г. Харьков, 13-14 ноября 2015 г. Дерматологія та венерологія. 2015. № 3 (69). С. 78–79.
18. Бронова І.М. Вплив ендокринологічних та психологічних чинників на епідеміологію акне у жінок. Збірник робіт за матеріалами науково-практичної конференції «Дерматовенерологія в розробках молодих науковців», 19-20 листопада 2015 року, м. Київ. Дерматовенерологія. Косметологія і сексопатологія. 2015. № 3–4. С. 108.
19. Кутасевич Я.Ф., Бронова И.М. Гендерные особенности течения акне. Научные труды первой научно-практической международной конференции Ассоциации дерматовенерологов Армении «Ереванские дерматовенерологические чтения» (Ереван, 2015). Научно-медицинский журнал. 2015. № 10. С. 94.
20. Бронова І.М. Особливості загострень акне у пацієнтів, що отримували різні види патогенетичної терапії. V Ювілейний міжнародний медичний конгрес «Впровадження сучасних досягнень медичної науки у практику охорони здоров’я» : Матеріали конгресу, м. Київ, 19–21 квітня 2016 р. К., 2016. С. 84.
21. Губина-Вакулик Г.И., Бронова И.М., Мещерякова Н.В. К вопросу о патологической морфологии угревой болезни. Збірник матеріалів заочної науково-практичної конференції з міжнародною участю, присвяченої 150-річчю з дня народження професора М.Ф. Мельникова-Разведенкова «Сучасні аспекти морфології людини: успіхи, проблеми та перспективи». Харків, 2016. С. 55–57. (Здобувачем зроблено аналіз даних та сформульовано мету)
22. Кутасевич Я.Ф. Бронова І.М. Комплексний підхід до лікування акне із застосуванням системних ретиноїдів та косметологічної методики екстракції комедонів. Тези доповідей науково-практичної конференції «Інноваційні досягнення в діагностиці інфекцій, що передаються статевим шляхом, інфекційних і грибкових захворювань та поширених дерматозів. Прогрес у лікуванні» у рамках VI Міжнародного медичного конгресу, м. Київ, 25 квітня 2017 р. К., 2017. С. 160.
23. Кутасевич Я.Ф., Бронова И.М. Вариабельность подхода к лечению подрывающего фолликулита. Матеріали науково-практичної конференції з міжнародною участю «Сучасні підходи до діагностики, профілактики та інноваційні технології лікування інфекцій, що передаються статевим шляхом, поширених дерматозів, основні організаційні задачі», 10-11 листопада 2017 р., м. Харків. Дерматологія та венерологія. 2017. № 3 (77). С. 104.
24. Кутасевич Я.Ф., Бронова И.М. Особенности коррекции сопутствующих явлений сухости слизистой губ у пациентов с акне, получавших системные ретиноиды. Сучасні проблеми дерматовенерології, косметології та управління охороною здоров’я : Збірник наукових праць. Вип. 14. Харків : Оберіг, 2017. С. 197.
ЗМІСТ
| Вступ | 17 |
| Розділ 1 Огляд літератури | 23 |
| 1.1 Епідеміологія та етіопатогенез акне | 23 |
| 1.2 Особливості мікробіоценозу шкіри хворих на акне | 29 |
| 1.3 Патогістологічні характеристики шкіри хворих на акне | 35 |
| 1.4 Сучасні неінвазивні методи діагностики акне | 36 |
| 1.5 Оцінка стану психоемоційної сфери у хворих на акне | 38 |
| 1.6 Сучасні методи терапії акне | 43 |
| Розділ 2 Матеріали та методи | 53 |
| 2.1 Клінічні методи | 53 |
| 2.2 Мікробіологічні методи | 53 |
| 2.3 Морфологічні методи | 54 |
| 2.4 Інструментальні методи | 56 |
| 2.5 Методи анкетування | 56 |
| 2.6 Статистичні методи | 56 |
| Розділ 3 Клінічна характеристика хворих на акне | 58 |
| Розділ 4 Лікування хворих на акне | 77 |
| 4.1 Методика лікування | 77 |
| 4.2 Динаміка регресу клінічних проявів дерматозу | 78 |
| 4.3 Клінічні випадки з груп спостереження | 83 |
| 4.4 Підтримуюча терапія хворих на акне | 92 |
| 4.5 Косметологічний супровід хворих на акне під час терапії системними ретиноїдами | 92 |
|
4.6 Комплаєнтність хворих на акне та її взаємозв’язок з ускладненнями та ефективністю терапії
|
94 |
| 4.7 Дослідження рівня тривожності у пацієнтів з акне до та після проведеної терапії | 99 |
| 4.8 Косметологічний супровід хворих на акне в період ремісії | 102 |
| Розділ 5 Дерматоскопічне дослідження динаміки елементів висипки в процесі саногенезу у хворих на акне | 107 |
| Розділ 6 Мікробіологічні дослідження | 116 |
| Розділ 7 Морфофункціональні зміни шкіри у процесі саногенезу у пацієнтів, що отримували системні ретиноїди | 124 |
| 7.1 Дослідження біоптатів шкіри хворих на акне | 124 |
| 7.2 Результати каріометрії епітеліоцитів шкіри хворих на акне | 136 |
| 7.3 Імуногістохімічні дослідження біоптатів шкіри хворих на акне | 137 |
| Розділ 8 Аналіз та узагальнення результатів досліджень | 150 |
| Висновки | 169 |
| Рекомендації172 | 172 |
| Список використаних джерел | 174 |
| Додаток А Акти впровадження | 202 |
| Додаток Б Список публікацій здобувача за темою дисертації та відомості про апробацію результатів дисертації | 212 |
| 4.5 Косметологічний супровід хворих на акне під час терапії системними ретиноїдами |
ВСТУП
Актуальність теми. Акне – це широко розповсюджене хронічне захворювання шкіри зі складним мультифакторним патогенезом, що вимагає тривалої комбінованої терапії. Більшість вітчизняних і закордонних авторів розглядають акне як порушення функціонування всього організму [150, 156]. На акне страждає 9,4 % світового населення, що робить його восьмим за поширеністю захворюванням у всьому світі. Акне посідає перше місце у структурі косметологічної патології і третє – за частотою звернення хворих до дерматологічних закладів [2].
Клінічні прояви акне являють проблему для пацієнтів та лікарів через велику поширеність, тривалий перебіг, стійкість до терапії та можливі післявугрові зміни шкіри.
На сучасному етапі простежується тенденція до зростання рівня захворюваності на вугрову хворобу акне, що вказує на важливе медичне та медико-соціальне значення проблеми.
У зв’язку з тим, що акне належить до хронічних, рецидивуючих дерматозів, локалізується, як правило, на відкритих ділянках шкіри, найбільш значущих для комунікативного спілкування, воно є постійним стресовим чинником, що призводить до психоемоційних реакцій, обмежень у всіх сферах життя [48, 49]. Акне має виражений вплив на якість життя пацієнтів, включаючи фізичну, емоційну та соціальну складові [50, 53, 79, 146]. За даними ряду авторів, вугрова хвороба завдає душевні страждання хворим, спричиняє занепокоєння, депресію, міжособистісні проблеми. Ряд зарубіжних дерматологів рекомендують обстежити всіх пацієнтів з акне молодого та юного віку на наявність депресії і пропонують відносити хворих на акне до групи суїцидального ризику [173, 200, 206].
Таким чином, можна сказати, що акне є психоемоційним дерматозом, для якого є характерною наявність психовегетативних порушень, перебування пацієнтів у стані хронічного стресу, соціальної дезадаптації [222]. У зв’язку з наявністю у хворих шкірних проявів, постійних психотравмуючих ситуацій, виникає фіксація на своєму захворюванні, що нерідко ускладнює терапію [240]. При виборі терапії пацієнтів з акне у кожному конкретному випадку слід враховувати швидкість настання ефекту з метою мінімізації психічних розладів [184]. Серед напрямків лікування акне можливо відокремити такі основні фармакологічні групи, як антибіотики, ретиноїди та зовнішня терапія [51]. Незавжди різне комбінування препаратів цих груп дає стійкий ефект або тривалий період між рецидивами. Так, серед пацієнтів з акне дуже часто спостерігається ефект поліпрагмазії, коли пацієнти отримували багато препаратів, що не впливають на етіопатогенез захворювання, впливають на матеріальний стан пацієнта, але не дають очікуваного ефекту від терапії.
Таким чином, особливої значущості набуває розкриття нових імуногістохімічних та мікробіологічних аспектів патогенезу акне, дерматоскопічних та патогістологічних ознак регресу дерматозу, пошук комплексної етапної терапії акне з урахуванням біоценозу шкіри, розробка методів протирецидивної дії, вивчення психологічного впливу акне на пацієнтів до та під час лікування, що підвищить ефективність лікування хворих.
Зв’язок роботи з науковими програмами, планами, темами. Дослідження виконувалися відповідно до основних наукових напрямів ДУ «Інститут дерматології та венерології НАМН України» і є фрагментом комплексних науково-дослідних робіт «Вивчити роль мутацій філагрину в порушенні епідермального бар’єру у хворих на хронічні дерматози та розробити методи корекції виявлених розладів» (№ держреєстрації 0117U000982), в якій дисертантом виконано розділ, що стосується вивчення динаміки біоценозу поверхні шкіри хворих на акне в процесі саногенезу; «Дослідити деякі аутозапальні механізми хронічних дерматозів» (№ держреєстрації 0115U000578), в якій дисертантом з’ясовано імуноморфологічні зміни, інтенсивність проліферації та апоптозу в шкірі хворих на тяжкі форми акне.
Мета та задачі дослідження. Мета – підвищити ефективність лікування пацієнтів з акне середнього та тяжкого ступеня шляхом уточнення показань до призначення системних ретиноїдів, поєднання їх із системними і топічними антибактеріальними засобами, а також засобами профілактики очікуваних побічних ефектів на підставі поглибленого вивчення механізмів дії системних ретиноїдів.
Для досягнення поставленої мети були поставлені такі задачі:
1. Дослідити сучасні клініко-епідеміологічні особливості акне.
2. Вивчити динаміку регресу клінічних ознак захворювання в процесі лікування.
3. Вивчити динаміку регресу дерматоскопічних ознак дерматозу.
4. Вивчити комплаєнтність хворих на акне та її вплив на ефективність терапії.
5. Вивчити особливості психоемоційних порушень та дослідити вплив терапії системними ретиноїдами на психічний стан хворих на акне.
6. Вивчити патогістологічні зміни у шкірі хворих на акне, а саме процеси проліферації та апоптозу епітеліоцитів. Визначити морфометричні особливості епідермоцитів у процесі саногенезу.
7. Дослідити динаміку мікробіоценозу шкіри у хворих на акне до, впродовж та після закінчення терапії системними ретиноїдами та комбінацією з системними і топічними антибактеріальними засобами та розробити оптимальні терапевтичні комплекси та режими їх застосування залежно від клінічної форми і ступеня тяжкості дерматозу, а також комплекс косметологічного супроводу хворих на акне у процесі терапії та під час ремісії.
Об’єкт дослідження: акне.
Предмет дослідження: стан мікробіоценозу, патогістологічних, дерматоскопічних, психоемоційних, біохімічних показників у пацієнтів з акне у процесі саногенезу та ефективність розробленого комплексу терапії та протирецидивних заходів.
Методи дослідження: клінічні (постановка діагнозу, визначення ступеня тяжкості перебігу дерматозу, контроль ефективності лікування); мікробіологічні (комплексна мікроскопічна та культуральна оцінка мікробіоценозу шкіри); імуногістохімічні та патоморфологічні (вивчення змін патогістологічної картини шкіри у процесі саногенезу), клініко-інструментальні: дерматоскопія (вивчення дерматоскопічних ознак дерматозу), психометричні (вивчення ступеня тривожності у пацієнтів з акне); статистичні.
Наукова новизна одержаних результатів. Вперше вивчено динаміку морфологічних та імуногістохімічних змін шкіри та її придатків у процесі саногенезу у пацієнтів з акне, що отримували системні ретиноїди.
Вперше визначено дерматоскопічні ознаки захворювання та їх динаміку в процесі лікування.
Вперше дано оцінку динаміки біоти шкіри залежно від вживання системних ретиноїдів без/або із системними антибактеріальними препаратами або препаратами зовнішньої дії.
Уточнено показання до призначення системних ретиноїдів, визначено оптимальні режими їх використання, зокрема підтримуючої терапії. Обґрунтовано необхідність таргетного косметологічного супроводу лікування хворих на середньотяжкі та тяжкі форми акне.
Надано оцінку ступеня тривожності хворих до та після терапії.
Практичне значення отриманих результатів. Розроблено, клінічно апробовано та впроваджено в практику спосіб лікування пацієнтів з акне середнього та тяжкого ступеня тяжкості, який включає призначення системних ретиноїдів і антибактеріальних препаратів системної чи зовнішньої дії та засобів, що запобігають розвитку побічних ефектів лікування системними ретиноїдами (патент України на корисну модель № 118999 від 11.09.2017р.).
Розширено показання до лікування системними ретиноїдами.
Розроблено програму таргетного косметологічного супроводу лікування хворих на акне.
Розроблено рекомендації щодо проведення підтримуючої терапії системними ретиноїдами.
Основні положення дисертації впроваджено в практичну роботу КЗОЗ «Харківський міський шкірно-венерологічний диспансер № 1», КЗОЗ «Харківський міський шкірно-венерологічний диспансер № 2», КМУ «Чернівецький обласний шкірно-венерологічний диспансер», ДУ «Інститут дерматології та венерології НАМН України», КЗОЗ Обласний клінічний шкірно-венерологічний диспансер № 1 (м. Харків), КЗОЗ «Харківський міський шкірно-венерологічний № 4», КЗ «Обласний шкірно-венерологічний диспансер» (м. Дніпро), а також у навчальний процес кафедри дерматології, венерології Львівського національного медичного університету ім. Данила Галицького.
Особистий внесок здобувача. Дисертантом проведено інформаційно-патентний аналіз літературних даних, обґрунтовано мету та завдання дослідження, зроблено висновки. Проведено клініко-лабораторне обстеження та лікування 142 хворих на акне різного ступеня тяжкості. Здобувачем самостійно здійснено кількісну обробку і наукову інтерпретацію отриманих результатів.
Усі опубліковані наукові праці, в яких викладено основні положення і зміст дисертації, авторські. З наукових праць, опублікованих у співавторстві, в дисертації використано лише ті ідеї, положення і висновки, які є результатом особистої роботи здобувача і становлять його індивідуальний науковий внесок. Дисертантом не були використані результати та ідеї співавторів публікацій. Конфлікту інтересів немає.
Апробація результатів дисертації. Матеріали дисертації доповідалися на науково-практичних конференціях і з’їздах: «Молоді науковці – майбутнє української дерматовенерології» (Київ, 2014), «Традиції та інновації у дерматології та венерології» (Харків, 2014), IV Міжнародний медичний конгрес «Впровадження сучасних досягнень медичної науки у практику охорони здоров’я України» (Київ, 2015), «Школа нових методів діагностики, лікування та профілактики в дерматовенерології» (Харків, 2015), «Розробки молодих вчених в сучасній дерматовенерології» (Харків, 2016), «Новітні технології діагностичних, лікувальних та профілактичних заходів в дерматовенерології та методи і стан їхнього впровадження» (Харків, 2016), «Сучасні підходи до діагностики, профілактики та інноваційні технології лікування інфекцій, що передаються статевим шляхом, поширених дерматозів, організаційні задачі» (Харків, 2017), «Медична наука на перетині спеціальностей: сьогодення та майбутнє» (Харків, 2017), «Сучасні перспективи і шляхи подальшого розвитку дерматовенерологічної служби України» (Херсон, 2017), «Новітні впровадження молодих вчених в сучасній дерматовенерології» (Харків, 2018).
Публікації. За темою дисертації опубліковано 24 друковані роботи, з них 12 статей, з яких 4 – у моноавторстві (5 – у фахових наукових журналах, 7 – у журналах, що входять до міжнародних наукометричних баз Index Copernicus, Googlе Scholar та Російський індекс наукового цитування, 2 статті – у закордонних виданнях), 10 тез доповідей, посібник для лікарів, отримано 1 патент України на корисну модель.
Структура та обсяг дисертації. Дисертаційна робота викладена на 218 сторінках машинописного тексту. Складається зі вступу, огляду літератури, опису матеріалів і методів дослідження, 5 розділів власних досліджень, обговорення результатів дослідження, висновків, рекомендацій, списку використаної літератури та двох додатків. Робота ілюстрована 77 рисунками та містить 4 таблиці. Бібліографічний список містить 274 джерел, з них 173 – кирилицею і 101 – латиницею.
РОЗДІЛ 1
ОГЛЯД ЛІТЕРАТУРИ
1.1 Епідеміологія та етіопатогенез акне
Акне або вугрова хвороба є широко розповсюдженим хронічним захворюванням шкіри зі складним патогенезом, що вимагає тривалої комбінованої терапії. Більшість вітчизняних і закордонних авторів розглядають акне як порушення функціонування всього організму [39, 58, 271].
На акне страждає 9,4 % світового населення, що робить його восьмим найпоширенішим захворюванням у всьому світі [54, 259, 262]. Акне посідає перше місце у структурі косметологічної патології і третє – за частотою звернення хворих до дерматологічних закладів [4].
За даними Американської академії дерматології, 85 % мешканців США хоча б раз у житті страждали на акне, а 20 % населення хворіють на активну форму захворювання [182].
У доступній літературі не знайдено відомостей щодо захворюваності на акне в Україні, але експерти припускають, що акне й акнеформні дерматози є одними з найпоширеніших у структурі всіх захворювань шкіри [2].
Серед дерматозів, залучених до патологічного процесу видимих частин шкіри, стійкий хронічний перебіг акне сприяє суттєвому зниженню якості життя, призводячи до психологічних розладів, розвитку депресії і навіть виникнення суїцидальних намірів [84].
Клінічні ознаки акне найчастіше починають виявлятися у підлітковому віці. Так, за даними досліджень, 90 % підлітків у Бельгії та Китаї страждають на акне [182], в Англії цей показник становить 50 % [183], у Саудівській Аравії – 53,5 % [211].
Акне зустрічається у дітей та підлітків усіх вікових груп. Численними дослідженнями виявлено різний рівень захворюваності на акне у новонароджених (від 10 % до 50 %); дитячі акне спостерігаються нечасто (менше 10 %). Вугрова хвороба частіше виявляється у період статевого дозрівання і вражає 80 % людей у віці від 12 до 24 років, а у вікових групах 25–34 і 35–44 років захворюваність становить відповідно 8 % і 3 %. Тяжкі форми захворювання зустрічаються у 5–14 % випадків [270]. Серед дівчат захворюваність складає 23 %, серед юнаків – до 35 %. Частота виникнення й тривалість перебігу акне у обох статей мають відмінності. У дівчаток акне виникає й регресує раніше, ніж у хлопчиків. Найбільший пік частоти виникнення вугрової хвороби реєструється у дівчаток 13–14 років, а у хлопчиків – у 15–16 років. Згодом у юнацький період рівень захворюваності на важкі клінічні форми вугрової хвороби знижується у дівчаток та зростає у хлопчиків [254]. У більшості підлітків до 18–20-річного віку відбувається регрес елементів, однак у 20 % інволюція акне сповільнена. У 10 % спостережень висипи зберігаються до 25–45 років. Навіть за умови адекватного лікування частота рецидивів впродовж 5 років після закінчення терапії, за даними різних авторів [230, 231], становить від 20 до 48 %.
Останнім часом все частіше зустрічаються пацієнти з виявами захворювання у зрілому віці. Згідно низці досліджень, у 38 % осіб вугрові висипання виявлялися у віці 25–35 років, а у 12,5 % – у віці 35–45 років [22, 224, 242]. Стрес як тригерний чинник відзначали 50 % жінок [28, 205], а загострення акне при стресі спостерігали у 71 % [179].
Дані літератури вказують на важливе значення порушень гінекологічного статусу організму в патогенезі вугрової хвороби у жінок репродуктивного віку [48, 131, 153, 244, 268].
Згідно літературних джерел, переважна більшість наукових досліджень останнього десятиліття з проблеми акне, зокрема в Україні, проведена із залученням осіб жіночої статі, які страждають на різні клінічні форми цього дерматозу [49, 132, 227]. Відмінності організму жінок і чоловіків (генетичні, анатомічні, фізіологічні, гормональні та ін.) можуть впливати на певні патогенетичні ланки розвитку акне, а також на характер і тяжкість перебігу цього дерматозу в осіб різної статі [105, 170]. Встановлено, що у дорослих чоловіків акне виникають рідше, ніж у жінок. Водночас персистуючі після 20 років юнацькі акне у чоловіків є тяжчими (конглобатні акне, фульмінантні акне, акневаскуліт, акне спини). Дослідники відмічають порушення рівня балансу статевих гормонів у чоловіків, що має вагоме значення у патогенезі розвитку різних форм вугрової хвороби [88, 89].
Клінічні вияви акне створюють проблему для пацієнтів та лікарів через велику поширеність, тривалий перебіг та можливі післявугрові зміни шкіри [29, 61, 66].
На сучасному етапі простежується тенденція до зростання рівня захворюваності на акне, що вказує на важливе медичне та медико-соціальне значення проблеми [85, 189]. Незважаючи на те, що акне незначно погіршує фізичний стан хворого, воно є постійним стресовим чинником, що призводить до психоемоційних реакцій та обмежень у всіх сферах життєдіяльності [63, 65, 108]. Навіть за умови адекватного лікування частота рецидивів упродовж п’яти років після закінчення терапії становить від 20 % до 48 % [81, 99].
Акне має виражений вплив на якість життя пацієнтів, включаючи фізичну, емоційну та соціальну складові [43].
Отже, можна зазначити наявність психовегетативних порушень, перебування пацієнтів у стані хронічного стресу, соціальної дезадаптації [115, 130, 141, 144]. У зв’язку з наявністю у хворих шкірних проявів, постійних психотравмуючих ситуацій, виникає фіксація на своєму захворюванні, що нерідко ускладнює терапію. Тому при виборі терапії акне у кожному конкретному випадку необхідно враховувати швидкість настання ефекту з метою мінімізації психічних розладів [195].
Однією з найповніших класифікацій акне є класифікація, яку запропонували G. Plewig, A. Kligman у 1994 р. Перевагою цієї роботи стало найбільш повне об’єднання існуючих форм акне. Ця класифікація одна з небагатьох, в якій автори спробували відобразити та об’єднати діагнози, ґрунтуючись на причинних етіологічних чинниках:
1. Неонатальні вугрі.
2. Ювенільні вугрі.
3. Юнацькі вугрі (комедональні, папулопустульозні, конглобатні, acne inverse, acne fulminans, твердий персистуючий набряк обличчя при акне).
4. Вугрі дорослих (локалізовані на спині, тропічні, післяювенільні вугри у жінок, післяменопаузальні, допінгові [27], тестостероніндуковані блискавичні вугрі у дуже високих підлітків чоловічої статі).
5. Контактні вугрі: косметичні, acne vulgaris як реакція на помаду, хлоракне, жирні та смоляні вугрі.
6. Комедональні вугрі внаслідок дії фізичних чинників: поодинокі комедони (хвороба Фавра-Ракушо) [34], сонячні комедони, малорка акне, механічні вугрі, акне внаслідок дії іонізуючого випромінювання.
Синдром Фавра-Ракушо вперше описали французькі дерматологи М. J. Favre (1932) і J. Racouchot (1937) як дистрофічну зміну еластичних волокон шкіри у літніх чоловіків, що супроводжується утворенням комедонів і кіст. Згідно їх опису, захворювання розвивається зазвичай у літніх чоловіків з надлишковою масою тіла на ділянках шкіри, що піддаються інсоляції (скроневі ділянки, вушні раковини, потилиця) [34].
Згідно з останніми даними, захворювання розвивається частіше у чоловіків у другій декаді життя, після 50 років, масова частка становить близько 6 %. Частіше страждають чоловіки з 4-м і 5-м типом шкіри за Фітцпатріком. Часто в їх анамнезі переважають тривалі періоди інсоляції, пов’язані з професією (моряки, фермери). У результаті інсоляції відбувається пошкодження еластичних волокон шкіри, що патогістологічно проявляється атрофією шкіри, витонченням еластичних волокон, гіперкератозом, утворенням комедонів, які відрізняються від комедонів при акне відсутністю запалення, з часом у результаті закупорки сально-волосяних фолікулів утворюються вузли і кісти.
Особливістю даної нозології є схильність до малігнізації при відсутності лікування і недотриманні рекомендацій з догляду за шкірою. Підвищений ризик розвитку актинічного і себорейного кератозу, злоякісного лентиго, базаліом, нерідко множинних, та інших новоутворень. Синдром Фавра-Ракушо характеризується як акнеформний дерматоз.
Однак в останні роки з’явилися нові дані у трактуванні деяких питань акне, тому ця класифікація потребує внесення доповнень та змін.
Становить інтерес спроба створення етіопатогенетичної класифікації, яку запропонували К. Н. Суворова та Н. В. Котова з доповненнями. Відповідно до цієї класифікації, виділяють такі види акне:
А. Конституціональні акне, ідіопатичні акне.
1. Себорейні акне у дитячому, підлітковому, юнацькому вікових періодах.
2. Пізні акне: передменструальні акне; післяменопаузальні акне, пізні гіперандрогенні акне, конглобатно-кістозні вугри у чоловіків із хромосомним синдромом полісемії ігрек (XYY) та синдромом Клайнфельтера.
Б. Спровоковані акне.
1. Артифіціальні (механічні, травматичні).
2. Масляні (зокрема професійні, смоляні та дігтярні).
3. Косметичні.
4. Екскорийовані акне.
В. Особливі форми акне.
1. Грамнегативні фолікуліти.
2. Піодермія обличчя.
3. Резистентне акне.
Оцінка ступеня тяжкості відіграє визначальну роль у виборі методу та об’єму лікування. Існує безліч варіантів класифікацій оцінки ступеня тяжкості, кожна з яких має певні переваги для практичної роботи [2, 9, 17]. Для визначення тяжкості перебігу акне однією з найбільш зручних є класифікація Американської академії дерматології [106, 258]. На підставі об’єктивної оцінки елементів висипу пропонують виділяти 4 ступені вугрової хвороби залежно від вираженості клінічних виявів та поширеності висипань: І – відкриті та закриті комедони, поодинокі папули; ІІ – від 2 до 15 папул, незначна кількість пустул; ІІІ – виражене запалення, численні папулопустульозні висипання, поодинокі вузли; IV – виражене запалення у глибоких шарах дерми, великі вузли, кісти. Недоліком цієї класифікації є відсутність ступенів тяжкості залежно від поширеності процесу.
Відповідно до Паризької класифікації 2002 р., виділяють три ступені акне: І (легкий) – комедональний та папулопустульозний (за наявності не більше 10 елементів); ІІ (середньої тяжкості) – папулопустульозний (більше 10 елементів) та/або вузлуватий (від 5 до 40 елементів); ІІІ (тяжкий) – конглобатний (більше 5 вузлів, більше 40 папулопустул) [106].
Відомим є метод оцінки тяжкості перебігу захворювання за С. Н. Cook та співавт. [204] та у модифікації B. S. Allen и J. G. Smith [180]. Шкала дозволяє проводити оцінку тяжкості захворювання на підставі площі ураження, кількості та особливостей висипних елементів за 8-бальною системою.
Для диференційної діагностики акне та акнеподібних дерматозів суттєве значення мають вікові критерії, виникнення і тривалість захворювання. За існуючою класифікацією акне за віковим критерієм виділяють: неонатальні акне, акне немовлят, акне дорослих [17].
Виходячи з викладеного, можна зробити висновок, що методи класифікації акне є різноманітними за своїм характером. Єдиної загальновизнаної системи поки що не існує. У процесі останніх наукових досліджень додаються нові дані. Вони вносять свої корективи, тому можна сказати, що методика класифікації поки ще перебуває на стадії вдосконалення.
1.2 Особливості мікробіоценозу шкіри у хворих на акне
Мікроорганізми, які мешкають на шкірі, завжди були в центрі уваги фахівців-дерматологів: детально вивчався їх склад, особливості колонізації, вплив на фізіологічні функції шкіри і розвиток шкірних захворювань [25, 73, 219, 228, 236]. Стандартні мікробіологічні методики включали посів на різні живильні середовища та мікроскопію. Досягнення останнього десятиліття в галузі генетичних досліджень збагатили сучасну дерматологію новими високоінформативними методиками, що дало змогу детально проаналізувати різноманіття бактерій, грибів і вірусів, що мешкають на шкірі та її придатках. Виявлено чіткий взаємозв’язок між організмами та чинниками, що зумовлюють вроджену й адаптивну імунну відповідь у шкірі в нормі та при патології [199]. Ці відомості суттєво розширили уявлення фахівців щодо патогенезу таких захворювань як атопічний дерматит, акне та інші запальні дерматози.
Шкіра є найактивнішою біологічною структурою людського тіла [3, 8, 18, 51, 98], яка виконує анатомічну, фізіологічну та психо-соціальну функції [53, 98, 133]. З одного боку, шкіра являє бар’єр, який захищає макроорганізм від зовнішніх впливів, а з іншого – це складна екосистема (мікробіом), де мікроорганізми живуть у певних фізіологічних умовах [75, 201, 256].
Мікробіоценоз, як цілісна екологічна система, перебуває в стані динамічної рівноваги між мікрофлорою та макроорганізмом [118]. Уявлення щодо нормального мікробіоценозу шкіри людини сприяє розумінню головних особливостей її мікросистеми та змін, спричинених різними несприятливими впливами [145, 156]. Дослідження мікробіоценозу шкіри продемонстрували різноманітність нормальної мікрофлори [80]. Згідно сучасних уявлень, нормоценоз або автофлору розглядають як сукупність мікробних біоценозів, характерною ознакою яких є відносна сталість видового й кількісного складу на шкірі та слизових оболонках [80, 158].
Нині фахівці, описуючи мікроорганізми, оперують такими поняттями як «мікробіота» та «мікробіом». Так, під терміном «мікробіота» розуміють усе різноманіття мікроорганізмів (бактерій, грибів, вірусів), що мешкає у всьому макроорганізмі, зокрема шкіра, слизові оболонки порожнин рота, носа, дихальних шляхів тощо [203]. Водночас існуючий термін «мікробіом» позначає сукупність мікроорганізмів, об’єднаних одним органом або анатомічною зоною. Отже, говорячи про мікробіоту шкіри та її придатки, використовують поняття мікробіом, маючи на увазі комплекс мікроорганізмів, що беруть участь у складному діалозі між шкірою і зовнішнім середовищем [15, 191].
Відповідно до прийнятої концепції, нормальну мікрофлору розглядають як з позиції тривалості перебування на шкірі, так і за місцем локалізації. За тривалістю перебування на шкірі виділяють три категорії мікробів: транзиторні, тимчасові та постійні резиденти [203]. За місцем локалізації автофлору поділяють на поверхневу, пов’язану з десквамуючим епітелієм, і глибоку, розташовану у волосяних фолікулах і протоках сальних залоз [98]. На нормальній шкірній поверхні всі види мікроорганізмів перебувають у симбіозі, продукти життєдіяльності яких не чинять шкідливого впливу на шкіру. Отже, нормальна мікрофлора та повноцінне функціонування шкірного епітелію виступають як хімічні та біологічні захисні чинники шкірного покриву й організму в цілому [228, 238].
При порушеннях стану здоров’я та функціонування систем організму змінюється й біологічний стан шкірного епітелію, що спричиняє дисбаланс у мікробному біоценозі [36, 64, 91, 142, 252]. Баланс мікроорганізмів на шкірі є умовою благополуччя цієї екосистеми, тоді як відхилення від норми носійства призводять до розвитку та маніфестації шкірних захворювань [188].
Отже, симбіоз мікро- та макроорганізмів дуже нестійкий. Так, організм людини, впливаючи на мікроорганізми, може змінювати їх властивості, а мікрофлора ж, у свою чергу, постійно й активно впливає на людину.
Отримані в останні роки дані генетичних досліджень у галузі мікробіології та дерматології створили можливість описати на шкірі основні таксономічні ранги мікроорганізмів, або філи (phyla). Всередині філів виділено також роди (genera) та види (species). Так, E. Grice et al. детально охарактеризували різноманітність мікробіому шкіри здорової дорослої людини. Дослідники виявили 19 основних філів, серед яких переважали Actinobacteria (52 %), Firmicutes (24 %), Proteobacteria (17 %) та Bacteroidetes (7 %). E. Grice et al. підтвердили різноманітність складу мікрофлори [217, 264, 268]. Виявлено за допомогою 16S рРНК філотипування зі зразків із 20 різних ділянок шкіри від 10 здорових добровольців 19 філів і 205 родів. Дотепер встановлено, що переважаючими на шкірі людини є бактерії, які належать до родів Staphylococcus, Propionibacterium і Corynebacterium, меншою мірою присутні Micrococcus, Streptococcus, Brevibacterium, Acinetobacterium і Pseudomonas [199]. Водночас вдалося визначити топографічну різноманітність мікроорганізмів, їх домінування на різних ділянках шкіри [217, 237, 265]. В одному з останніх досліджень продемонстровано, що зі зразків на шкірі людини може бути виділено понад 2300 бактеріальних, понад 1300 вірусних, майже 400 грибних і приблизно 70 архейних геномів [247].
Отже, можна дійти висновку, що відомості про стан мікробіому здорової шкіри дають змогу деталізувати склад мікробіому в ділянках сальних залоз в нормі та при патології, що сприяє виявленню ланок патогенезу акне.
Як відомо, основні ланки патогенезу акне являють такі чинники: гіпертрофія сальних залоз, фолікулярний гіперкератоз, мікробна колонізація та запалення [120, 167]. Водночас зазначено, що мікробний чинник відіграє значну роль, спричиняючи інфікування патологічних осередків як мікробною монокультурою, так і змішаною бактеріальною або бактеріально-грибковою [135, 172].
Переважна більшість дослідників вважає, що Propionibacterium acnes (P. acnes) відіграє головну роль у розвитку запалення при акне. Хоча P. acnes є нормальним представником мікробіоценозу сальних залоз, збільшення його кількості призводить до активізації місцевого імунітету [82]. За таких умов P. acnes, живлючись гліцерином шкірного сала, спричиняють збільшення кількості вільних жирних кислот, що порушує процеси зроговіння кератиноцитів та ускладнює перебіг акне [181].
Дані досліджень свідчать, що при акне з ділянок патологічних осередків, крім P. аcnes, часто виділяють інші види бактерій, зокрема Staphylococcus aureus (до 30–43 %). Так, проведене мікробіологічне дослідження осередків ураження при акне у 30 хворих виявило високу частоту роду Staphylococcus, що дозволило дослідникам припустити, що ці мікроорганізми можуть пролонгувати запальний процес, спричинений іншими мікроорганізмами [10, 220]. За даними літератури, тяжкість патологічного процесу у хворих на акне залежить від питомої ваги патогенних стафілококів та можливості їх персистенції в осередках ураження [122, 149, 154, 260].
На ділянках шкіри з великою кількістю сальних залоз переважають пропіонібактерії і стафілококи [6]. Нові дослідження мікробіому людини в нормі та при патології підкреслюють значення популяції стафілококів у підтримці екосистеми шкіри, зокрема роль Staphylococcus aureus в етіології і патогенезі дерматозів [155]. Сальна залоза формує майже позбавлену кисню нішу, яку заселяють у основі Propionibacterium spp., а у ділянці устя – ліпофільні аероби, зокрема Malassezia spp. [267].
Дослідники зазначають, що потенційну роль і характеристики тих чи інших мікроорганізмів у патогенезі акне треба розглядати стосовно уявлень щодо фази процесу, що перебігає в часі. Вочевидь, що склад мікробіоти може розрізнятися на початкових стадіях розвитку елементів акне і в розвиненій стадії запалення, в комедональній, пустульозній і вузловій формах захворювання [138]. Так, засіви з комедонів можуть давати однакову або схожу частоту виділення пропіонібактерій і стафілококів (51–96 %) [101, 246]. У посівах з папульозних елементів акне частіше виділяють пропіонібактерії, здебільшого при більш зрілих елементах висипки, водночас стерильними виявляються 20–54 % папул при акне [246]. Частина пустул при акне також виявляється стерильною, однак приблизно в 70 % випадків виділяються пропіонібактерії, майже у 60 % випадків – стафілококи. За даними С. Н. Рахманової та співавт. [145], при акне виділено у комедонах 34 види мікроорганізмів, серед яких, у порядку спадання, спостерігалися пропіонібактерії, Malassezia spp., стафілококи та Candida spp., у пустулах – стафілококи, Candida spp., Malassezia spp. і пропіонібактерії.
Fitz-Gibbon S. et al. [247] провели дослідження пропіонібактерій у здорових людей і хворих на акне та виявили п’ять філотипів: IA, IB, IC, II і III [253]. Дотепер очевидного взаємозв’язку між філотипами та характером перебігу акне не виявлено. Водночас тільки філотип IC асоційований із цим дерматозом, а філотип III був відсутній у пацієнтів із акне.
Перспективність отриманих даних полягає в тому, що вони можуть стати основою для розробки нових препаратів, які впливають селективно на певний філотип, що є важливим у ситуації зростання антибіотикорезистентності [174, 190, 202, 220]. З іншого боку, вибірковий вплив на філотип пропіонобактерій може бути значущим у пацієнтів, що складають групи ризику з розвитку тяжких акне (особи з обтяженою спадковістю, ранньою центрофаціальною комедональною формою, ранньою вираженою себореєю тощо) [72, 215].
Дослідження мікробного пейзажу шкіри у 120 хворих на акне виявило високу інтенсивність мікробної колонізації шкіри та збільшення кількості таксономічних груп з переважанням асоційованих форм мікроорганізмів. Malassezia furfur, Candida albicans, P. acnes були обов’язковими учасниками мікробних асоціацій. При мікст-інфекціях відмічається тенденція до тяжчого перебігу акне, особливо за наявності кандидозної інфекції [93, 172].
Також зазначено, що особливості метаболізму хазяїна можуть вплинути на експресію патогенних властивостей збудника [261]. Недавні транскриптомні дослідження продемонстрували, що додавання вітаміну B12 до P. acnes in vitro призводить до підвищення продукування ними порфіринів, залучених до патогенезу запальної реакції [226]. Цей факт у подальшому може бути покладений, зокрема, в основу розуміння ґенезу деяких медикаментозних вугрів.
Дослідження з оцінки мікробної флори у хворих на папулопустульозну, індуративну, абсцедуючу та конглобатну форми акне виявило зміни мікробних співтовариств від різноманіття асоціацій аеробних асоціацій мікроорганізмів до аеробних і анаеробних мікроорганізмів з високим ступенем обсімененності вогнищ ураження [121].
Згідно дослідження, проведеного Р. Т. Ісаєвим [72], змішана мікробіота здебільшого спричиняє вугрові елементи при акне. Водночас у хворих на акне, крім P. acnes, виявлено S. aureus і C. albicans. Встановлено залежність тяжкості перебігу хвороби від наявності мікст-інфекції. Виявлено, що P. acnes і S. aureus, виділені від хворих, у 40,7–59,6 % випадків є резистентними до антибіотиків, які традиційно використовують при лікуванні вугрової хвороби.
М. А. Іонеску та співавт. [5], подали нові дані щодо мікробіому шкіри з акне, вродженого імунітету при дерматозах і деякі нові патофізіологічні механізми запального процесу, а також результати in vitro, ex vivo та in vivo досліджень впливів на молекулярні структури мікробіому та мікробіоплівки патогенних типів P. acnes, які призвели до суттєвого поліпшення стану 74 пацієнтів із вульгарним акне [4].
У науковій літературі останніх років відзначено тенденцію до зростання кількості стійких штамів мікробіоти шкіри при акне. Застосування антибактеріальних препаратів, крім різного роду побічних ефектів, і поряд з бактерицидними та бактеріостатичними властивостями, взагалі призводить до пригнічення не тільки патогенної, але й ліквідації представників індигенної мікробіоти. Унаслідок цього пошкоджена запаленням шкіра стає ще більш беззбройною для різного роду впливів навколишнього середовища, не встигаючи відновити мікробіоту. Це спричиняє розвиток спалаху акне з новою силою, навіть у короткий проміжок після припинення лікування [23, 30, 35, 59].
Г. П. Пекліна та співавт. [11] відзначили, що застосування стандартної антибактеріальної терапії у 89,9 % хворих на акне не забезпечувало стійкого позитивного результату, з чого випливає, що антибіотикотерапія навіть з огляду диференційованного підходу до збудника, забезпечує вплив лише на один з факторів патогенезу акне і враховуючи це не може забезпечити довготривалу ремісію.
Усе зазначене вище створює необхідність пошуку засобів і методів лікування, які б діяли вибірково на зміни кількісно-видового складу мікробіоти шкіри при акне, не знищуючи при цьому представників нормобіоти.
1.3 Патогістологічні характеристики морфологічних елементів при акне
Гістологічне дослідження та біопсія в складних випадках захворювань шкіри є конче необхідним. Аналіз гістограм сприяє розумінню запально-репаративного процесу [42]. Нажаль останнім часом досить нечасто вдаються до цього методу, нехтуючи можливостями гістологічного дослідження. У доступній літературі є невелика кількість робіт з цієї проблеми.
Було знайдено проведений порівняльний аналіз гістограм різних форм екземи, нейродерміту, атопічного дерматиту, псоріазу, червоного плоского лишаю, розацеозів, поверхневого кандидозу, мікозів стоп, зокрема акне. Аналіз гістограм свідчить, що при запальних шкірних реакціях при акне у дермі зосереджується перифолікулярний інфільтрат, лімфоцитарний за складом. Також спостерігається атрофія та руйнування волосяних фолікулів унаслідок перифолікуліту [25, 26, 78, 128]. Аналіз складу клітинного інфільтрату може використовуватися при плануванні обстеження хворого та визначення тактики лікування [94, 148, 177, 216, 235].
Було проведено аналіз морфологічних елементів висипки А. І. Новіковим та співавт. Виявлено відмінності в характері висипок залежно від локалізації процесу. Так, висипки папульозного характеру спостерігалися на шкірі обличчя, грудей і спини, пустули відзначалися також на всіх досліджуваних ділянках шкірного покриву (обличчя, груди, спина). Основні відмінності стосувалися поширення вузлів: у 100 % випадків вражалася шкіра обличчя, мінімальна кількість їх відзначена на спині (20 %), на шкірі грудей – 32 %. У процесі дослідження автори відзначили недостатню кількість патогномонічних ознак, характерних для акне.
В іншій роботі А. І. Новіков та співавт. провели дослідження 44 біоптатів шкіри папул і пустул при папулопустульозній формі акне [70]. Виявлено відповідність макроскопічних та мікроскопічних ознак морфологічних елементів. Подано гістологічний опис біоптатів, імуногістохімічним методом ідентифіковано популяції антигенпрезентуючих клітин та Т-лімфоцитів пам’яті. Визначено принципово різні механізми морфогенезу формування пустули і папули.
Незважаючи на незначну висвітленість у науковій літературі питань патогістології акне, на мою думку, при постановці остаточного діагнозу у складних та сумнівних випадках є обов’язковим проведення гістологічного дослідження для встановлення клітинних змін на субклітинному рівні та особливо важливим вважається вивчення особливостей динаміки гістологічної картини при застосуванні різних методів лікування та визначення їх ефективності [46, 47].
1.4 Сучасні неінвазивні методи діагностики акне
Нині в дерматології та онкології стали широко впроваджуватися неінвазивні методи діагностики, зокрема дерматоскопія (епілюмінесцентна мікроскопія), конфокальна лазерна мікроскопія, високочастотний ультразвук, оптична когерентна томографія, флуоресцентна діагностика. Використання цих методів дослідження дає змогу чітко ідентифікувати клінічні прояви новоутворень шкіри [41, 157].
Дерматоскопія, використовуючи ефект епілюмінесценції, створює можливість дослідження новоутворень шкіри зі збільшенням у 10–40 разів [24, 26, 56, 193]. Цей метод може бути застосований при диференціальній діагностиці шкірних захворювань, наприклад, волосяних кіст пушкового волосся, контагіозного молюска та вугрової висипки.
Існують також інші неінвазивні методи візуальної діагностики конфокальна лазерна скануюча in vivo мікроскопія – це принципово новий напрямок у вивченні структур шкіри. Метод базується на комп’ютерному аналізі відмінностей коефіцієнта відбиття (рефракції) світла для різних структур шкіри [92]. Конфокальна мікроскопія дозволяє виявити морфологічні аспекти, що характеризують різні типи вугрів. M. Manfredini et al. провели порівняльний аналіз конфокальних зображень, одержаних від 25 хворих із помірним і легким ступенями акне, з 10 зображеннями здорових добровольців [176]. Шкіра пацієнтів із акне порівняно зі здоровою шкірою пацієнтів виявила специфічні конфокальні особливості (яскраві кільця навколо волосяного фолікула). Пропонують використовувати цей метод для ідентифікація субклінічних змін при акне, а також при контролі ефективності лікування [223].
Оптичний відеомоніторинг або оптична топометрія, 3D-моделювання шкіри – безконтактні технології, що дають змогу в режимі реального часу об’єктивно оцінювати і аналізувати макро- і мікрорельєф шкіри з реєстрацією кількісних показників. Метод грунтується на аналізі одержаного зображення шкіри за допомогою спеціального програмного забезпечення. Цей метод застосовують для оцінки ступеня тяжкості акне. Зазначається ефективність методу оптичного моніторингу при аналізі успіхів лікування. До недоліків методу відносять неможливість визначення глибини порушених ураженням тканин [197].
У закордонній літературі обговорюється питання використання автоматизованих систем при обробці зображень у визначенні ступеня тяжкості акне, що сприяє об’єктивізації оцінки. Проте складність розпізнавання та інтерпретації дерматоскопічних ознак вимагає від лікаря, який виконує дослідження, спеціальної підготовки і накопичення певного клінічного досвіду. При підрахунку пошкоджень і порівнянні пацієнта з фотографічним стандартом пропонується розробити напівавтоматизовані або автоматизовані алгоритми, що базуються на методах обчислювальної візуалізації, що сприятиме моніторингу лікування [175, 185].
Отже, неінвазивні методи візуальної діагностики шкіри дозволяють швидко, в режимі реального часу об’єктивно фіксувати морфофункціональні зміни, які відбуваються в шкірі людини в нормі та при патології. Також ці методи дають можливість оцінювати динаміку запальних процесів, але практична відсутність відповідної апаратури та її дуже висока вартість не дає змоги застосувати ці методи, а тим більше у повсякденній практиці, тоді як епілюмінесцентний метод може бути широко застосований зокрема для оцінки адекватного вибору методу лікування та його ефективності на різних етапах.
1.5 Оцінка стану психоемоційної сфери у хворих на акне
Дерматологічні захворювання нерідко супроводжують людину все життя і призводять до формування психічних розладів, які значно знижують якість життя хворих, сприяючи їх дезадаптації у соціально-психологічному плані. За даними різних авторів, поєднання дерматологічної і психічної патологій становить близько 30–40 % [195, 229, 240].
На відміну від багатьох інших шкірних захворювань, при акне уражається обличчя, яке є однією з головних і провідних ланок міжособистісної та соціальної комунікації [33, 115]. Закордонні автори відносять акне до групи дерматозів, що спричиняють соматопсихічний резонанс внаслідок реального чи вигаданого естетичного дискомфорту [59, 62, 63]. Водночас шкірні проблеми в разі психологічної фіксації на своєму захворюванні стають психотравмуючим чинником [65, 66].
Виявлено негативний вплив акне на самооцінку і самосприйняття хворих, оцінку стану власного здоров’я, міжособистісні взаємини та соціальні функції [208, 209].
На тлі акне можливе формування уникаючої поведінки, соціальних фобій, тривоги, депресії. Депресія у загальній популяції пацієнтів з акне становить 8,8 % [266]. Метааналіз літератури виявив зменшення симптомів депресії, пов’язане з прогресом лікування акне [222].
Н. В. Волкова та Л. К. Глазкова проаналізували розповсюдженість психічних розладів серед пацієнтів амбулаторного профілю з діагнозом акне [38]. Поширеність психічних розладів тривожно-депресивного спектру становила 35,2 %, тривоги – 24,2 %, депресії – 26,2 %, поєднання тривоги та депресії – 43,74 %. В іншому дослідженні показники тривожності та депресії хворих на акне були високими – 89,19 % та 78,32 % відповідно.
Виявлено вплив гендерного чинника на формування тривожно-депресивних розладів [20, 62]. Пацієнтки відзначали відчуття внутрішнього напруження, емоційну нестійкість і підвищений рівень тривоги [43]. Формування тривожно-депресивних розладів і соціофобій у жінок не корелювало з тяжкістю вугрової хвороби [63]. Водночас існують роботи, автори яких звернули увагу на прямий паралелізм між ступенем тяжкості акне та вираженістю тривоги і депресії [43, 140, 143].
Акне може провокувати сенситивні реакції та іпохондричні розлади, призводячи до формування суїцидальних думок і спроб [31, 249]. Низка зарубіжних дерматологів рекомендує проводити обстеження пацієнтів із акне молодого та юного віку щодо наявності депресії і пропонують включити хворих із акне до групи суїцидального ризику. Проведені дослідження виявили, що депресія та суїцидальні думки, здебільшого, характерні для пацієнтів із акне, ніж для пацієнтів із осередковою алопецією, атопічним дерматитом і середньотяжким перебігом псоріазу [250]. Усе це ще більше ускладнює процес лікування пацієнтів із акне і вимагає обов’язково залучати до лікування лікаря-психотерапевта або психолога.
Підвищений ризик суїциду у підлітків із акне може бути обумовлений не тільки порушеннями психіки, але і проведеним лікуванням. Так, шведське ретроспективне когортне дослідження, що включало більше 5 тис. осіб у віці від 15 до 49 років з вугровою хворобою, виявило підвищений ризик суїцидальних спроб на тлі застосування ізотретиноїну [184].
Психічні розлади, що розвиваються на тлі акне, є причинами дезадаптації у соціальній, професійній сферах, сімейному житті [113, 221].
Захворюваність на акне впливає на міжособистісні стосунки. Такі хворі відрізняються невпевненістю у міжособистісних контактах, мають труднощі у спілкуванні з іншими, що призводить до залежної і підлеглої позиції [114].
Внутрішня картина хвороби, як основний комплекс вторинних, психологічних за своєю природою, симптомів захворювання, у низці випадків може ускладнювати перебіг хвороби, перешкоджати успішності лікувальних заходів, гальмувати перебіг реабілітаційного процесу [111, 178]. Проблеми комплаєнтності, або прихильності пацієнтів до запропонованої схеми терапії, відзначаються у 34–45 % пацієнтів дерматолога. Комплаєнтність при терапії акне, за даними закордонних авторів, становить від 12,5 % до 64 %; вона вища при системному лікуванні [186] і нижча у більш молодих хворих; у чоловіків; осіб, які не перебувають у шлюбі; безробітних; тих, хто отримує ліки безкоштовно, палить або вживає алкоголь [225, 274].
Незважаючи на впровадження ефективних засобів зовнішньої та системної терапії акне, загальну ефективність лікування та реабілітації пацієнтів нині не можна визнати задовільною. Відповіді на багато питань щодо ефективності терапії акне може дати вивчення якості життя пацієнтів, їх ставлення до захворювання та його лікування [250].
Дослідження якості життя пацієнтів дерматологічного профілю, зокрема акне, проводиться методом анкетування з використанням спеціальних інструментів – різних опитувальників: дерматологічного індексу якості життя (ДІЯЖ), Кардіффського індексу соціальної дезадаптації (CADI; Cardiff Acne Disability Index) і Assessment of Phychological and Social Effects of Acne (APSEA) [139, 173, 255].
Індекс CADI містить 5 питань із 4 варіантами відповідей до кожного, за які нараховують бали від 0 до 3. Максимальна кількість балів за тест – 15, мінімальна – 0. Чим більше балів, тим сильніше акне впливає на якість життя пацієнта. Опитувальник психологічного та соціального ефекту впливу вугрів APSEA містить 15 питань. Перші 6 питань мають по 4 варіанти відповідей, з яких треба обрати тільки один. За відповідь нараховується 0, 3, 6 або 9 балів. Останні 9 питань оцінюються за візуальною аналоговою шкалою від 0 до 10 балів. Максимальна кількість балів за тест – 144, мінімальна – 0. Чим більша сума балів, тим сильніше акне порушує якість життя пацієнта [7]. ДІЯЖ складається з 6 основних параметрів: симптоми та самопочуття, щоденна активність, дозвілля, робота і навчання, особисті відносини та лікування. Максимальна сума балів становить 30, а якість життя пацієнтів при цьому зворотно пропорційна кількості балів [97].
М. Л. Арипова та С. А. Хардикова [16] провели оцінку динаміки психоемоційного стану 22 пацієнтів із тяжким ступенем акне. Відзначалося значне зниження якості життя таких пацієнтів, що виявлялося у високих значеннях індексів CАDI, APSEA, ДІЯЖ. Монотерапія ізотретиноїном (акнекутан) призвела до стійкої ремісії шкірного процесу та підвищення якості життя, що виявлялося в зниженні індексів CАDI, APSEA, ДІЯЖ. Отже, застосування системного ізотретиноїну призвело до підвищення якості життя хворих на акне, що підтверджується зниженням індексів CADI, APSEA і ДІЯЖ у результаті лікування, за таких обставин динаміка індексів пов’язана з позитивною динамікою шкірного процесу.
Проведено обстеження 98 хворих на акне з оцінки впливу тривалості й тяжкості перебігу захворювання на показники якості життя осіб у гендерному, віковому, професійному та лікувальному аспектах. Встановлено погіршення якості життя в осіб, що хворіють на акне понад 4–5 років [250].
Викликає зацікавлення вивчення рівнів залучення психоемоційної сфери впродовж вугрової хвороби у дітей та підлітків [134, 251]. Дитячий дерматологічний індекс якості життя (Children’s Dermatology Life Quality Index, CDLQI) був розроблений спеціально для використання в педіатричній практиці та являє простий, але досить інформативний інструмент з вивчення якості життя у дітей і підлітків віком 5–16 років. З метою оцінки вираженості тривожної та депресивної симптоматики найпоширенішими є такі стандартизовані шкали, як госпітальна шкала тривоги та депресії (Hospital Anxiety Depression Scale), шкала оцінки депресії Carroll (Carroll Rating Scale for Depression), шкала соціального неспокою (Social Anxiety Scale) [248].
У дослідженні корейських вчених [207], до якого увійшло більше 500 школярів у віці 13–16 років, для оцінки психосоціальної сфери використовувалися опитувальник оцінки власного зовнішнього вигляду, опитувальник Розенберга для вивчення самооцінки, індекс відносин із однолітками та шкала Бека для оцінки депресії. Упродовж дослідження було виявлено, що на акне страждали 78,9 % підлітків, водночас у 10,2 % діагностовано помірну та тяжку форми цього захворювання. Зазначено, що психологічні та соціальні проблеми більш виявлені у жінок та підлітків обох статей із тяжкою формою акне. Тривалість анамнезу акне корелювала з рівнем ментального стресу.
У підсумку, треба наголосити на необхідності міждисциплінарного підходу до терапії акне за участю дерматологів, психологів та психіатрів. Крім того треба зазначити, що лікування акне, особливо його тяжких форм, є тривалим і потребує високої комплаєнтності хворих. Відсутність її може бути виявлена в ході оцінки психоемоційної сфери та може бути відповідним чином прокоректована.
1.6 Сучасні методи терапії акне
Вибір терапевтичної стратегії при акне має ґрунтуватися на аналізі двох основних критеріїв: ступеня тяжкості шкірного процесу та характеру його перебігу. Призначення відповідної терапії має здійснюватися з урахуванням типу шкіри, статі, віку, супутніх захворювань та ефективності попередніх методів лікування. Зовнішня терапія призначається хворим незалежно від ступеня і тяжкості захворювання. Показаннями для призначення системної терапії є акне середнього і тяжкого ступеня, психосоціальна дезадаптація, а також утворення рубців і неефективність зовнішнього лікування. Також дуже важливо проводити диференціацію показань до системної та місцевої терапії [1, 2, 61].
До групи сучасних патогенетичних засобів зовнішньої терапії акне належать місцеві ретиноїди (третиноїн, ретин-А тощо), азелаїнова кислота, місцеві антибіотики та бензоїлпероксид [60, 71, 74, 81, 86, 99, 151, 164, 192, 218]. Відповідно до існуючого алгоритму терапії, при акне I ст. тяжкості лікування обмежується призначенням топічного третиноїну та бензоїлпероксиду [159]. При акне ІІ–ІІІ ст. застосовують топічні ретиноїди з бензоїлпероксидом та/або системну терапію оральними антибіотиками або гормональними препаратами, а при акне ІV ст. призначають ізотретиноїн або топічні ретиноїди з оральними антибіотиками та гормональне антиандрогенне лікування [2, 127, 152, 172].
Заслуговує на увагу дослідження застосування топічних ретиноїдів на основі адапалену. Автор наводить переваги при використанні зовнішньої терапії засобів, що містять адапален [1].
Азелаїнова кислота (скінорен) також достатньо ефективний противугровий препарат, що має антикератинізувальні, комедонолітичні, протизапальні та протимікробні властивості [59, 96, 123]. Водночас окремі дослідники рекомендують призначати скінорен при келоїдно-кістозній формі акне. Експериментальними та клінічними дослідженнями встановлено, що азелаїнова кислота безпосередньо не впливає на морфологію та функціонування сальних залоз [166].
Упродовж останнього десятиліття серед дерматовенерологів тривають дискусії щодо раціональності застосування місцевих антибіотиків при акне. Це пов’язано з тим, що антибіотики, які входять до складу місцевих противугрових препаратів, у разі тривалого застосування сприяють формуванню резистентних штамів бактерій [246, 263].
У літературних повідомленнях останніх років запропоновано методики поєднаного застосування бензоїлпероксиду з топічними антибіотиками для запобігання розвитку антибіотикостійких штамів бактерій та посилення поєднаного антимікробного ефекту [212, 213], а також методики комбінованого місцевого лікування акне топічними ретиноїдами та бензоїлпероксидом. Водночас, згідно з результатами досліджень окремих авторів, бензоїлпероксиду не властива себосупресивна дія [88]. Крім того, зазначається, що цей препарат може спричиняти контактний дерматит та посилювати чутливість шкіри до інсоляції.
У комплексному лікуванні хворих на акне застосовують також місцеві хімічні антисептики (хлоргексидин, іхтіол) та антимікробні засоби рослинного походження [89, 161].
Зовнішнє застосування антибіотиків і препаратів з антибактеріальною дією показане при запальних формах легкої та середньої тяжкості; при тяжких формах акне – як доповнення до системної антибіотикотерапії [116]. Механізм дії місцевих антибіотиків полягає в інгібуванні метаболізму пропіонібактерій акне, зниженні рівня вільних жирних кислот, пригніченні хемотаксису, внаслідок чого зменшується запальна реакція. Більшість авторів розглядають їх як альтернативу призначенню пероральних антибіотиків [139, 140, 163].
Системна терапія вугрової хвороби передбачає застосування антибіотиків і ретиноїдів, а також препаратів антиандрогенної дії. Нині запропоновано кілька різних схем та комбінацій системної терапії при вугровій хворобі [3, 52, 100, 102, 103, 107, 174, 231, 234].
Незважаючи на те, що на сучасному етапі акне не розглядають як інфекційне захворювання, треба враховувати антимікробну ефективність антибіотиків з погляду їхньої дії, спрямованої на пригнічення росту P. acnes, зменшення рівня вільних жирних кислот у загальному обсязі поверхневих ліпідів, а також інгібіції синтезу хемотоксичних чинників P. acnes, антиоксидантного та протизапального ефекту. Пероральне призначення антибіотиків є доцільним при середньотяжкому і тяжкому клінічному перебігу акне, коли на запальні елементи висипки не впливає зовнішня терапія. Антибіотикотерапію при акне проводять переважно тетрациклінами та макролідами. Водночас антибіотики тетрациклінового ряду (тетрациклін, доксициклін, еритроміцин) традиційно вважають основними антибіотиками у пероральній терапії акне [21]. Дослідники вказують на достатньо високу ефективність коротких курсів лікування антибіотиками макролідами [19].
Сучасні схеми лікування акне передбачають тривалі курси перорального прийому антибіотиків. Саме тоді виникають побічні ефекти, які знижують імунні реакції, що, у свою чергу, призводить до послаблення захисних функцій шкіри, розвитку фототоксичних реакцій, гепатиту, інтракраніальної гіпертензії, пігментації слизових оболонок, унаслідок чого погіршуються прогноз та перспективи одужання. Побічні ефекти рекомендується зменшувати шляхом індивідуального підбору оптимальної дози антибіотика та паралельного призначення антимікотичних препаратів.
Нині серед зарубіжних та вітчизняних лікарів-дерматовенерологів тривають дискусії стосовно доцільності тривалих курсів антибіотикотерапії при акне [13, 83, 187]. Це зумовлено зростанням резистентності бактерій в організмі до антибіотиків у разі їх тривалого застосування. Процес резистентності розвивається завдяки закріпленню мутацій РНК, які зменшують ефективність терапії, створюють умови для переходу захворювання в тяжчі форми, хронізації процесу, сумнівних результатів лікування з подальшим розвитком грамнегативних фолікулітів і фолікулітів, спричинених Pityrosporum ovale, негативного впливу на макроорганізм. З огляду на це виникає необхідність альтернативного підбору антибіотиків або диференціювання показань до призначення системних антибіотиків і системного ізотретиноїну, зокрема у пацієнтів зі значною дисморфофобією щодо захворювання та схильністю до рубцювання і появи вираженої післязапальної пігментації, особливо у разі III фототипу шкіри [85, 273].
Окремі автори встановили розвиток резистентних штамів P. аcnes у 60 % пацієнтів, які приймали антибіотики тетрацикліни або макроліди загальним курсом лікування більше як 3 місяці. Зазначається, що збільшення кількості резистентних штамів P. аcnes є прямопропорційним тривалості вживання антибіотика [25, 57].
С. Н. Ахтямов та співавт. [17] на підставі результатів проведених клінічних спостережень рекомендують для досягнення регресу запальних проявів акне обмежити прийом антибіотиків впродовж 1–2 міс. із подальшим проведенням протирецидивного лікування зовнішніми ретиноїдами.
З метою підвищення ефективності лікування антибіотиками та зменшення кількості резистентних штамів бактерій на шкірі інші дослідники [244] рекомендують призначати хворим на акне перорально антибіотики у комбінації із зовнішніми лікарськими засобами, зокрема, третиноїн та бензоїлпероксид, що сприяє збільшенню проникнення антибіотика у протоки сальних залоз .
Європейське керівництво з лікування акне 2012 р. рекомендує застосовувати при акне ІІ–ІІІ ст. системні ретиноїди як препарати першої лінії терапії . Активним діючим компонентом цих препаратів є ізотретиноїн – стереоізомер трансретиноєвої кислоти (третиноїну) [48, 129, 152, 194, 274].
У системній терапії при тяжких клінічних формах вугрової хвороби застосовують також препарат ізотретиноїну «Роаккутан». Це найпотужніший противугровий препарат системної дії, який запобігає утворенню рубців та дає змогу досягати вилікування або тривалої ремісії [104, 140, 214, 215]. Накопичений останніми роками клінічний досвід застосування «Роаккутану» сприяв розробленню удосконалених схем його застосування [4, 14, 112, 131, 140, 201].
У 2001 р. створено нову форму ізотретиноїну – «Акнекутан» або «Акнетін» – запатентована технологія LIDOSE [102, 103, 106]. Завдяки інноваційній технології, ізотретиноїн у препараті перебуває у вигляді суспензії, що складається з двох фракцій – розчиненої у жирових наповнювачах і нерозчиненої. Інноваційна форма випуску дає змогу зменшити дозу препарату зі збереженням високої ефективності та мінімальним ризиком розвитку побічних явищ. «Акнетін» успішно застосовується при лікуванні акне різних ступенів тяжкості [133, 136, 137], зокрема у підлітків [160]. Встановлена висока ефективність лікування з досягненням повної клінічної ремісії в усіх хворих на середньотяжкі та тяжкі акне, відзначено відсутність серйозних небажаних ефектів та ускладнень під час проведення лікування [103, 104, 117].
На сучасному етапі в Україні найчастіше використовують «Акнетін». У літературних джерелах наведено дані щодо переваг цього препарату, призначення доз для дітей та дорослих, протипоказання до застосування [44, 45, 108, 168]. Прийом «Акнетіну» супроводжується певними побічними ефектами, навіть за умови застосування запобіжних медико-косметичних заходів. Проте побічні ефекти є прогнозованими, а очікуваний терапевтичний ефект значною мірою переважає можливі ризики [108, 164].
Сучасні противугрові засоби представлені як системними, так і місцевими препаратами, що діють переважно тільки на один чинник патогенезу акне. Будь-які місцеві противугрові препарати (ретиноїди та ретиноїдоподібні сполуки, азелаїнова кислота, бензоїлу пероксид, антибіотики, препарати з цинком) не гарантують пацієнту стійку та тривалу ремісію процесу після припинення терапії [126].
Виходячи з основ етіології і патогенезу акне, для лікування цього захворювання у жінок адекватними і патогенетично обґрунтованими є речовини, які мають супресивну дію на стан гіперандрогенії, тобто антиандрогени, які зайняли міцні позиції у міжнародних алгоритмах ведення жінок з акне легкого та середнього ступенями тяжкості [57, 124, 269]. Головними мішенями гормональної терапії є андрогени, що їх продукують яєчники та надниркові залози, а також андрогенові рецептори шкіри [233].
Серед препаратів, що впливають на вираженість андрогенізації, найширшого застосування набули комбіновані оральні контрацептиви (КОК) [200, 231]. Описано досвід використання КОК Джес і Джес Плюс з погляду етіопатогенетичного підходу до терапії акне у жінок [130]. Комбінація препарату Діане-35, який містить прогестерон із антиандрогенною активністю та етинілестрадіол, особливо ефективний у жінок із пізнім акне [260]. Як свідчать літературні повідомлення [17, 77, 179], позитивний терапевтичний ефект «Діане-35» зареєстровано в 70 % пацієнток із пізнім акне. Після припинення відповідної терапії кількість рецидивів становила 40 % [180].
До стероїдних антиандрогенів, рекомендованих сьогодні в комплексній терапії акне, належить спіронолактон. Препарат – антагоніст альдостерону – блокує рецептори андрогенів безпосередньо в сальних залозах, пригнічуючи синтез шкірного сала, а також інгібує біосинтез андрогенів [3, 17].
В останнє десятиліття у терапії акне широко застосовують інші контрацептиви з низьким вмістом прогестинів, зокрема прогестини третього покоління: гестоден, дезогестрел, норгестимат. Ці препарати рекомендується призначати хворим на акне впродовж 3–4 циклів [35].
Як свідчать результати клінічних спостережень, антиандрогенний ефект гормональної терапії зростає у разі комбінованого застосування контрацептивних препаратів із ципротерону ацетатом (андрокур), який суттєво зменшує продукцію шкірного сала. Пропонувалося також посилювати пригнічення секреції шкірного сала шляхом комбінації естрогенів із кортикостероїдами у низьких дозах. Глюкокортикостероїди у низьких дозах сприяють протизапальному та антиандрогенному ефектам, особливо у хворих на акне з природженою гіперплазією надниркових залоз [44, 192].
Особливості патогенетичних механізмів розвитку акне, а також варіабельність клінічних форм захворювання обумовлюють різноманіття методів лікування. Вочевидь, що для успішної терапії акне потрібен індивідуальний підхід у підборі як системних (при тяжчих або ускладнених формах), так і топічних препаратів, які мають призначатися з урахуванням особливостей розвитку та перебігу хвороби [40, 212, 215].
Останнім часом у науковій літературі з’являється дедалі більше робіт, присвячених використанню лікарських засобів у поєднанні з косметологічними процедурами [50, 68, 119]. B. Dreno et al. уперше дали рекомендації з терапії акне у дорослих жінок, в яких окремим розділом виклали рекомендації щодо допоміжної терапії та косметичної корекції [242, 244]. Я. А. Юцківська відзначила ефективність зовнішнього лікування акне азелаїновою кислотою в поєднанні з процедурою контрольованої мікродермабразії [171].
Отже, відзначено можливість поєднання медикаментозної терапії з методами естетичної корекції [12, 76, 162].
Косметологічні методи лікування традиційно використовуються як допоміжні під час фармакотерапії, а після її завершення як основні [109]. Мета косметологічної терапії акне, здебільшого, полягає в санації шкіри, відновленні її бар’єрних властивостей і системи антибактеріального захисту, а також ексфоліації потовщення рогового шару з подальшою нормалізацією кератинізації та евакуації шкірного сала. Крім того, важливо запобігти формуванню рубців і пігментних плям при загоєнні акне. Унаслідок комплексного косметологічного впливу відбувається усунення гіперколонізації мікроорганізмами, гіперкератозу, відновлення фізіологічної кератинізації, запобігання патологічного рубцювання та післязапальної пігментації [93, 218, 239].
У період загострення акне можливим є проведення санації осередків запалення методами фототерапії (фотодинамічна терапія, лазеротерапія) [165, 241]. Ультразвукова терапія та фонофорез із протизапальними препаратами застосовуються при інфільтративних і вузлувато-кістозних формах акне [147, 167]. Подано дані щодо лікування 20 пацієнтів, хворих на акне середньої тяжкості, із застосуванням фотодинамічної терапії у поєднанні з засобами системної антибактеріальної терапії. У 86 % пацієнтів спостерігалося стійке поліпшення стану шкірних покривів [171].
Кріотерапія призначається при папуло-пустульозних висипаннях та має протизапальну та підсушуючу дію, зменшує саловиділення, сприяє розсмоктуванню інфільтратів. Крім того, вплив холоду викликає звуження кровоносних судин і зменшує почервоніння шкіри. Зазначається можливість аплікації холодоагентів локально безпосередньо на елементи запалення [50, 71].
Хімічні пілінги застосовують при лікуванні комедональної і папуло-пустульозної форм акне, а також атрофічних рубців і післязапальної гіперпігментації [37, 162, 196, 210]. За допомогою пілінгів можна впливати на одну з ланок патогенезу акне – патологічний фолікулярний гіперкератоз. Альфа-гідроксикислоти, за даними численних досліджень, сприяють усуненню фолікулярного гіперкератозу, прискорюючи процес ексфоліації, мають комедонолітичну дію, зменшують розмір пір, запобігають формуванню нових запальних елементів акне [50]. Клінічні спостереження підтверджуються даними гістологічних досліджень [204]. Після проведення пілінгу знижується рН на поверхні шкіри, поліпшується відтік вмісту фолікула, усуваються анаеробні умови, що сприяють розмноженню P. аcnes, зменшується ступінь мікробної колонізації шкіри [150, 168, 232].
Мезотерапія – ще один ефективний метод дерматокосметології, ефективний у терапії комедонів, запальних елементів без гнійного вмісту, атрофічних рубців післяакне, вторинної післязапальної гіперпігментації [119, 153]. Наявність елементів із гнійним вмістом є протипоказанням для проведення мезотерапії.
Біоревіталізація (ін’єкції препаратами нестабілізованої гіалуронової кислоти) найчастіше використовується для корекції атрофічних рубців після акне [119, 272].
Правильно призначена комбінована терапія, яка включає методи з різним механізмом дії, не тільки зменшує прояви акне, але і має ревіталізуючий ефект. Унаслідок такого лікування досить швидко спостерігається ефект, який зберігається тривалий час, сприяючи підвищенню якості життя [198, 206]. Злагоджені дії косметолога та дерматолога визначають правильну послідовність, поєднуючи базові лікувальні заходи та заходи косметичної корекції, що є запорукою успіху на шляху вирішення проблем акне.
* * *
Таким чином, акне як хронічне рецидивуюче захворювання шкіри за розповсюдженістю посідає одне з провідних місць серед дерматозів людини. Високий рівень захворюваності на акне, різноманітність та тяжкість клінічних проявів, зміни соціальної та психічної сфери хворих, відсутність єдиного підходу до лікування зумовлюють медико-соціальну значимість подальшого дослідження проблеми акне. Незважаючи на численні дослідження мікробіоти шкіри при акне, цей аспект патології залишається актуальним, що пов’язано насамперед із збереженням тенденції до зростання резистентності, а також частими випадками лише тимчасового позитивного терапевтичного ефекту з подальшим більш тяжким і стійким перебігом. Різноманіття патогенетичних чинників обумовлює труднощі лікування акне і вимагає подальшої розробки лікувально-профілактичних заходів.
Матеріали цього розділу висвітлено у наступних публікаціях:
1. Кутасевич Я.Ф., Бронова И.М. Базовая и адъювантная терапия при тяжелых формах акне. Український журнал дерматології, венерології, косметології. 2015. № 2 (57). С. 74–79 [103].
2. Бронова И.М., Хатем С.М. Редкие нозологии: клинический случай синдрома Фавра-Ракушо. Дерматологія та венерологія. 2017. № 2 (76). С. 53–55 [34].
РОЗДІЛ 2
МАТЕРІАЛИ ТА МЕТОДИ
2.1 Клінічні методи
У дослідження увійшли 142 пацієнта з акне, які спостерігалися з приводу даного захворювання на базі ДУ «Інститут дерматології та венерології НАМН України» у період 2014-2017 рр. Пацієнти були обстежені загальноклінічно (клінічний аналіз крові, біохімічний аналіз крові, кров на сифіліс), за показаннями вони були консультовані суміжними спеціалістами: гастроентерологом, отоларингологом, ендокринологом-гінекологом. Діагноз ставився на підставі клінічних, анамнестичних даних і скарг пацієнтів.
Враховуючи, що не існує єдиної класифікації ступенів тяжкості перебігу акне, у своєму дослідженні використовували наступну класифікацію тяжкості дерматозу:
– легкий – наявність здебільшого закритих і відкритих комедонів практично без ознак запалення. При легкому ступені можлива наявність менше 10 папулопустульозних елементів на шкірі обличчя;
– середній – від 10 до 40 папулопустульозних елементів на шкірі обличчя;
– важкий – понад 40 папулопустульозних елементів на шкірі обличчя, а також абсцедуючі, флегмонозні (вузлувато-кістозні) або конглобатні вугрі.
2.2 Мікробіологічні методи
Бактеріологічні дослідження були проведені на базі лабораторії мікробіології ДУ «Інститут дерматології та венерології НАМН України», лабораторія має свідоцтво про атестацію № 100-295/2015 від 20.11.2015 року (дійсне до 19.11.2018) та дозвіл на роботу зі збудниками III-IV груп патогенності.
До групи спостереження увійшов 61 пацієнт з акне середнього та тяжкого ступеня.
Мікробіологічне дослідження проводилося пацієнтам триразово: до початку, в процесі, після закінчення терапії. До контрольної групи увійшли 20 осіб – клінічно здорових осіб.
Забір матеріалу для культуральних досліджень проводили з найбільш уражених ділянок шкіри обличчя або тулуба метод змивів із засівом на селективні живильні середовища. Ідентифікацію виділених грампозитивних факультативно-аеробних, грамнегативних аеробних і неферментуючих бактерій проводили з використанням рутинних методів класичної бактеріології на підставі морфологічних, культуральних і біохімічних особливостей (Наказ МОЗ СРСР № 535, 1985). Визначення чутливості виділеної мікрофлори до протимікробних засобів проводилося на таких препаратах: пеніцилін, гентаміцин, доксициклін, азитроміцин, кліндаміцин, лінкоміцин, ципрофлоксацин, хлорамфенікол, фузидієва кислота. Популяція метицилін-резистентних S. aureus (MRSA) і СоNS (коагулазонегативних стафілококів) була оцінена в загальній групі пацієнтів, з використанням оксациліну. Визначення чутливості до препаратів проводили диск-дифузійним способом за вдосконаленим методом Кербі-Бауера за допомогою стандартних дисків з антибіотиками (Наказ МОЗ України № 167, 2007). Штами резистентні і проміжно-резистентні були об’єднані в групу стійких до даного антибіотика.
2.3 Морфологічні методи
Патогістологічне дослідження біоптатів з уражених ділянок шкіри на тулубі у пацієнтів з важким ступенем акне проводилося тричі: до, в процесі і після проведеної терапії та проведено на базі ДУ «Інститут дерматології та венерології НАМН України» в лабораторії патоморфології. Опис консультовано професором Губіною-Вакулик Г.І. Забір матеріалу проводився принципово зі шкіри тулуба, щоб рубці після загоєння не залишалися на ділянках шкіри, які помітні при спілкуванні (шкіра обличчя).
Метод біопсії був інцизійним з попередньою анестезією і наступною обробкою і перев’язками згідно хірургічним вимогам. Біоптати були зафіксовані в 10 % розчині нейтрального формаліну, після проводки в спиртах зростаючої концентрації залиті в формалін. Було виготовлено мікропрепарати, забарвлені гематоксиліном та еозином. Світлове мікроскопування здійснювалося на мікроскопі Ах-Plus (Zeiss, ФРН).
Біоптати були зафіксовані в 10 % розчині нейтрального формаліну, після проводки в спиртах зростаючої концентрації залиті в парафін. Виготовлені мікрозрізи (товщиною 5-6 мкм) забарвлені гематоксиліном та еозином. Світлове мікроскопування здійснювалося на мікроскопі Axiostar-plus (Zeiss, ФРН), мікрофотографії отримані із застосуванням цифрової фотокамери Progress-C10.
Проведена каріометрія епітеліоцитів шипуватого шару епідермісу (програмне забезпечення «ВидеоТест», РФ).
Імуногістохімічне дослідження процесів проліферації та апоптозу епітеліоцитів, а також наявність Т-лімфоцитів-супресорів/цитолітиків у дермі здійснено із застосуванням первинних моноклональних антитіл до Ki-67, поліклональних антитіл до каспази-3, моноклональних антитіл до CD8 (TermoScientific, США) на базі відділу патоморфології центральної науково-дослідної лабораторії при Харківському національному медичному університеті та проконсультовано професором кафедри патоморфології Губіною-Вакулик Г.І. Титр антитіл підбирався згідно рекомендацій виробника з використанням у якості розчинника спеціального розчину «Antibody Dіluent» (TermoScientific, США). Для ідентифікації реакції використовували систему візуалізації «Quanto» (TermoScientific, США), з нанесенням в якості хромогену 3-діамінобензидин тетрахлориду (DAB) (TermoScientific, США). Для відокремлення незабарвлених структур зрізи додатково обробляли гематоксиліном Майєра.
2.4 Інструментальні методи
Дерматоскопічне дослідження проводилося пацієнтам з акне тяжкого ступеня, які отримували системні ретиноїди за допомогою дерматоскопа «Heine Delta 20+» у 16-кратному збільшенні: до початку, в процесі і після закінчення терапії.
2.5 Методи анкетування
Психологічний стан пацієнтів з акне оцінювався за допомогою методики оцінки ситуаційної та особистісної тривожності, виходячи зі шкали самооцінки (Спілбергера-Ханіна).
Тест допомагає визначити тривожність, яка як особистісна риса означає мотив або набуту поведінкову позицію, яка змушує людину сприймати широке коло об’єктивно безпечних обставин, як ті, що містять загрозу, спонукаючи реагувати на них станами тривоги, інтенсивність яких не відповідає величині реальної небезпеки [20]. Тест складається з двох частин і містить у собі 40 суджень, які потрібно підтвердити або спростувати.
2.6 Статистичні методи
Порівняння ефективності видів терапії та динаміки регресу акне проводилося методами математичної статистики. На попередньому етапі обробки даних були виключені спостереження з викидами, які визначалися за допомогою критерію варіаційного розмаху і критерію Діксона [79]. В результаті були виключені 5 спостережень, так що в групах залишилося 18, 18 і 20 пацієнтів.
Для порівняння статистичної значущості відмінностей середніх в групах використовувалися непараметричні критерії Манна-Вітні, Краскела-Уолліса (порівняння незалежних вибірок – схеми лікування) і Вілкоксона (порівняння залежних вибірок – динаміка лікування) [79]. Нульова гіпотеза про рівність середніх при порівнянні груп відхилялася при рівні значущості р <0,05. Обчислення проводилися за допомогою програм «Microsoft Office Excel 2010» і «StatSoft Statistica 13».
РОЗДІЛ 3
КЛІНІЧНА ХАРАКТЕРИСТИКА ХВОРИХ НА АКНЕ
Під спостереженням на базі ДУ «Інститут дерматології та венерології НАМН України» перебувало 162 особи, з яких 142 пацієнта з акне: 58 (40,8 %) чоловіків і 84 (59,1 %) жінки та контрольна група 20 клінічно здорових осіб.
Легкі форми акне спостерігалися у 16 пацієнтів, середньо-тяжкі – у 97 пацієнтів, тяжкі у 28 пацієнтів.
Серед жінок превалювали середньотяжкі форми дерматозу – 56 пацієнток (66,6 %), важкі форми акне – 9 пацієнток (10,7 %) і 16 (11,2 %) пацієнток з акне легкого ступеня. Серед чоловіків превалювали середньотяжкі форми акне (41 пацієнт – 70,6 %) і важкі форми – 18 пацієнтів (29,4 %). Вік пацієнтів коливався в діапазоні 8-50 років.
Серед пацієнтів, які мали молодший шкільний вік, – 1 пацієнтка 8 років (0,7 %), у середньому шкільному віці (13-16 років) спостерігалося 12 (8,4 %) пацієнтів: 7 (4,9 %) чоловіків та 5 (3,5 %) жінок. Вікова група від 17 до 22 років склала 52 (36,6 %) пацієнти [28 чоловіків (19,7 %) і 24 жінки (16,9 %)], пацієнтів віком 23–35 років було більше – 57 (40,1 %) осіб [14 чоловіків (9,85 %) та 43 жінки (30,3 %)], у віковому діапазоні 36-60 років спостерігалося 20 пацієнтів: 12 (8,45 %) жінок та 8 чоловіків (5,63 %) – згідно з класифікацією вікової періодизації Академії педагогічних наук СРСР (1965 р.).
Таблиця 3.1 – Розподіл дослідних хворих за статтю та віком
| Стать | Вік 8-12 | Вік 13-16 | Вік 17-22 | Вік 23-35 | Вік 36-60 |
| Жінки | 1( 0,7%) | 5 (3,5%) | 24(16,9%) | 43(30,2%) | 12(8,45%) |
| Чоловіки | – | 7(4,9%) | 28(19,7%) | 14(9,85%) | 8(5,63%) |
| Всього | 1(0,7%) | 12 (8,4%) | 52(36,6%) | 57(40,1%) | 20 (14,1%) |
Факторами, що свідчать про ризик розвитку тяжких форм акне, є підвищене саловиділення (себорея), вік початку акне (після 17 років або в препубертатному періоді), прояви акне на тулубі, спадковість. Приміром раннього початку акне може слугувати наступний клінічний випадок.
Клінічний випадок №1. Пацієнт Д., 14 років звернувся зі скаргами на висип на шкірі обличчя та тулуба. З анамнезу відомо, що хлопчик хворіє з 11 років. Раніше неодноразово лікувався: отримував системну і зовнішню антибактеріальну терапію, автогемотерапію, вітаміни. Зі слів пацієнта і мами, поліпшення наставало на нетривалий період і повного регресу висипки не відбувалося. Супутньої патології не має.
При огляді: дерматоз має поширений симетричний характер. Папулопустульозні елементи на шкірі обличчя і верхнього плечового поясу, на щоках елементи мали зливний характер з ознаками флуктуації. Шкіра обличчя і тіла з ознаками жирної себореї, множинні відкриті та закриті комедони з деформованими і розширеними устями сально-волосяних фолікулів у себозалежних зонах. На шкірі бічних поверхонь шиї множинні інфільтрати. Лімфовузли без патологічних змін (рис. 3.1).
Діагноз: акне тяжкого ступеня. Був обстежений загальноклінічно: патологічних відхилень і протипоказань до терапії системними ретиноїдами немає.
Супутня патологія спостерігалася у 67 (47,1 %) пацієнтів: у 22 чоловіків (51,1 % від кількості пацієнтів чоловічої статі) і у 45 жінок (53,5 % від кількості пацієнток). Серед жінок переважала патологія: гіперандрогенія різного генезу (надниркова, яєчникова) – 29 жінок, синдром полікістозних яєчників – 6 пацієнток, фіброміома матки – 3 жінки, гіперпролактинемія – 6 жінок. На проведену гістеректомію та поліпи матки вказали також 2 жінки. Більш того, 3 пацієнтки з гіперандрогенією в анамнезі вказали зриви вагітності, маткові кровотечі. З приводу основного захворювання вони отримували антиандрогени, оральні контрацептиви, фолієву кислоту і верошпірон. Зі слів гінекологів, якими вони були консультовані, ці препарати повинні були опосередковано вплинути на стан шкіри та інтенсивність висипу. Тільки 4 пацієнтки вказали, що оральні контрацептиви в монотерапії в анамнезі поліпшили стан шкіри. Дискінезію жовчовивідних шляхів мали 12 жінок, хронічний тонзиліт – 4, хронічний холецистит – 3, хронічний гастрит – 2. Лямбліоз та аскаридоз було діагностовано у двох пацієнток, у однієї з пацієнток було діагностовано мікоз стоп.
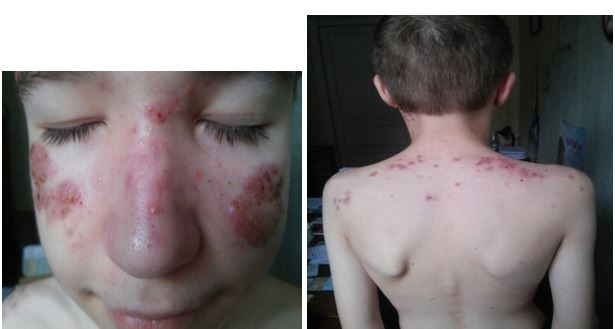
Рисунок 3.1 – Пацієнт Д., 14 років – до лікування. Фото пацієнта
в процесі терапії та після лікування у розділі 4.
Серед чоловіків переважали наступні супутні захворювання: хронічний тонзиліт – у 14 осіб, хронічний гастрит – у 11 осіб, хронічний холецистит – у 13 чоловіків, цукровий діабет – у 2 пацієнтів, простатит – у 2 чоловіків, токсокароз – у 2 пацієнтів, стимуляція гормонами росту в анамнезі – у 1 пацієнта, ожиріння – у 2 пацієнтів, сколіоз – у 1 пацієнта, мікоз стоп – у 2 пацієнтів.
Клінічний випадок № 2. Пацієнт К., 17 років. Звернувся зі скаргами на висип на обличчі і тілі. З анамнезу відомо, що пацієнт хворіє близько 4 років. Неодноразово лікувався: отримував системну антибактеріальну терапію (доксициклін, цефтриаксон), зовнішні засоби у вигляді комбінацій антибіотиків, цинку або бензоїлпероксид. Відзначав короткочасний позитивний ефект, але рецидив наступав приблизно через місяць, коли з’являлися нові гноячкові висипи. На момент огляду: дерматоз мав поширений характер, представлений множинними папуло-пустулами, відкритими і закритими комедонами, свіжими і давніми рубцями постакне на шкірі обличчя, шиї, тулуба (рис. 3.2). Соматичний статус: ожиріння за жіночим типом, сколіоз. В анамнезі були часті ангіни, хронічний тонзиліт. Обстежено у отоларинголога: рекомендовано місцеве лікування у вигляді полоскань і місцевих антисептиків. Обстеження у ендокринолога: патологію не виявлено.
Діагноз: Акне тяжкого ступеня. Ожиріння, сколіоз, хронічний тонзиліт.
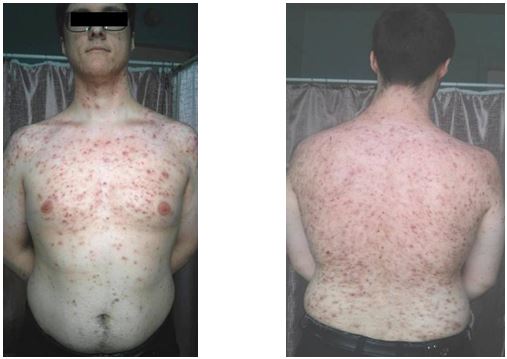
Рисунок 3.2 – Пацієнт К., 17 років, акне тяжкого ступеня, ожиріння,
сколіоз, хронічний тонзиліт.
Клінічний випадок № 3. Пацієнт Т., 23 роки, звернувся в ДУ «Інститут дерматології та венерології НАМН України» зі скаргами на висип на шкірі обличчя, волосистої частини голови, шиї, верхніх кінцівок, тулуба. З анамнезу відомо, що мав затримку росту і отримав курс стимуляції соматотропним гормоном, після чого через кілька місяців зазначив появу перших елементів висипу на шкірі обличчя і тулуба. Висип прогресував, він звернувся за допомогою за місцем проживання. Були призначені антибіотики з роду цефалоспоринів, «бовтанки», склад яких вказати не може. На момент огляду дерматоз мав поширений, симетричний характер, представлений папуло-пустулами різного діаметру, множинними відкритими і закритими комедонами, множинними рубцевими атрофічними і гіпертрофічними елементами постакне лівідного відтінку на шкірі обличчя, тулуба, верхніх та нижніх кінцівок (рис. 3.3). Загальноклінічне обстеження патологічних відхилень і супутньої патології не виявило.
Діагноз: акне тяжкого ступеня.
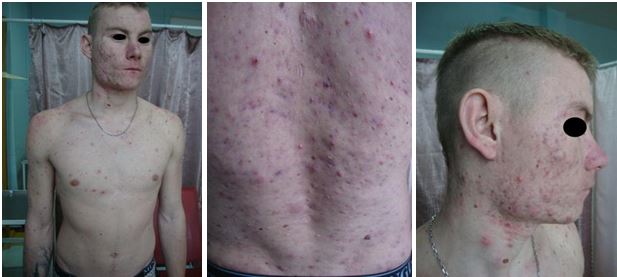
Рисунок 3.3 – Пацієнт Т.,23 роки. В анамнезі стимуляція розвитку соматотропным гормоном. До лікування.
З анамнезу у пацієнтів, які увійшли до дослідження, було з’ясовано, що понад 50 % хворих мали рецидиви після проведеної терапії або збільшення інтенсивності в період максимальних сезонних температурних стрибків. 16 хворих відзначали збільшення або появу висипу влітку, 46 осіб відзначили посилення висипу взимку і пов’язували її з переохолодженням, 22 пацієнти відзначили погіршення стану шкіри або посилене прогресування висипу і влітку і взимку.
Під час дослідження звернувся пацієнт, якому було встановлено діагноз – фолікуліт абсцедуючий підриваючий Гоффмана – рідкісне хронічне гнійне захворювання, яке зустрічається у чоловіків 18-40 років.
Причину розвитку пов’язують з оклюзією сально-волосяних фолікулів. Часто поєднується з конглобатними вуграми і гідраденітом.
Клінічно фолікуліт Гоффмана характеризується глибокими запальними вузлами на волосистій частині голови з випадінням волосся над ними. Вузли зазвичай зливаються і утворюють абсцеси, при розтині яких формуються фістульні ходи, як би підриваючи шкіру. Процес нерідко поширюється на більшу частину голови і персистує роками. Можливий спонтанний регрес запалення з утворенням рубців, у тому числі келоїдних.
Клінічний випадок № 4. Пацієнт Л., 33 роки звернувся за допомогою в ДУ «Інститут дерматології та венерології НАМН України» зі скаргами на висип на шкірі обличчя, волосистої частини голови і тіла (рис. 3.4). З анамнезу відомо, що пацієнт страждав на акне з 20 років, періодично проходив курс лікування взимку, так як висип прогресував після переохолоджень. Отримував системну антибактеріальну терапію, вітаміни, антимікотики, гепатопротектори, зовнішньо антибактеріальні засоби з тимчасовим позитивним ефектом від 1 до 3 місяців. З анамнезу відомо, що в зимовий час пацієнт захоплюється підводним полюванням, яке можна вважати постійно впливаючим фактором переохолодження. Останнє погіршення спостерігалося з грудня 2016 року. Обстежено загальноклінічно: патологічних відхилень і протипоказань до терапії не було. При обстеженні органів малого тазу виявлено хронічний простатит.
Діагноз: акне тяжкого ступеня. Підриваючий фолікуліт Гоффмана.
Особливістю анамнезу у чоловіків також було відзначено прийом спортивних добавок 15 пацієнтів, які містять протеїни, можливо стимулятори росту м’язової тканини гормонального походження – ці пацієнти мали важкі форми акне з тривалим торпідним перебігом і погано піддавалися терапії (зі слів пацієнтів).
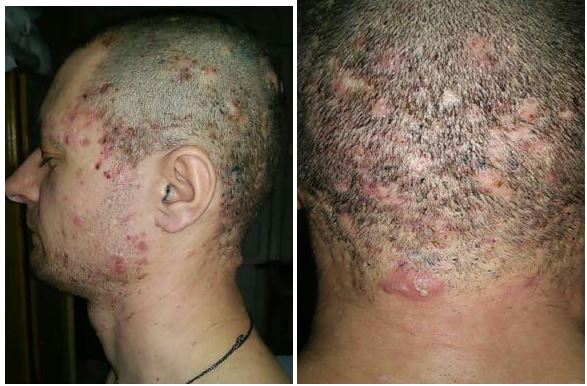
Рисунок 3.4 – Пацієнт Л., 33 роки – до лікування. Фото пацієнта в процесі лікування та після лікування у розділі 4.
Клінічний випадок № 5. Пацієнт С., 22 роки звернувся зі скаргами на висип на обличчі і тулубі. З анамнезу відомо, що пацієнт займається бодібілдингом, відвідує спортзал, приймає декілька видів спортивних добавок впродовж 1,5-2 років. Висип з’явився близько року тому у вигляді множинних відкритих і закритих комедонів на обличчі й тілі, посилилася жирність шкіри. Звернувся по допомогу, так як останні два місяці кількість елементів висипу стала збільшуватися, з’явилися гнійні елементи на шкірі тулуба і зі слів пацієнта «захворювання заважає йому спати», бо лежати на спині стало дуже болісно для нього, а вранці він прилипає до простирадла через велику кількість гною. При огляді: висип мав поширений характер. Представлений великими інфільтратами на обличчі, тулубі, великими папуло-пустулами з рясним гнійним вмістом з тенденцією до злиття на шкірі міжлопаткової зони і зони грудини. У ділянці грудини був великий ерозивно-виразковий елемент з гнійно-геморагічною кіркою за типом «гнійного озера». На шкірі обличчя, тулуба, шиї множинні відкриті та закриті комедони, глибокі рубцеві зміни постакне (рис. 3.5). Соматичний статус без особливостей. Був обстежений: у клінічному аналізі крові – лейкоцитоз – 14 ∙109/л, ШОЕ – 25 мм/год. Дослідження крові на ВІЛ, гепатити, сифіліс – негативні. Був поставлений діагноз акне важкого ступеня, індукований прийомом «спортивних» добавок.
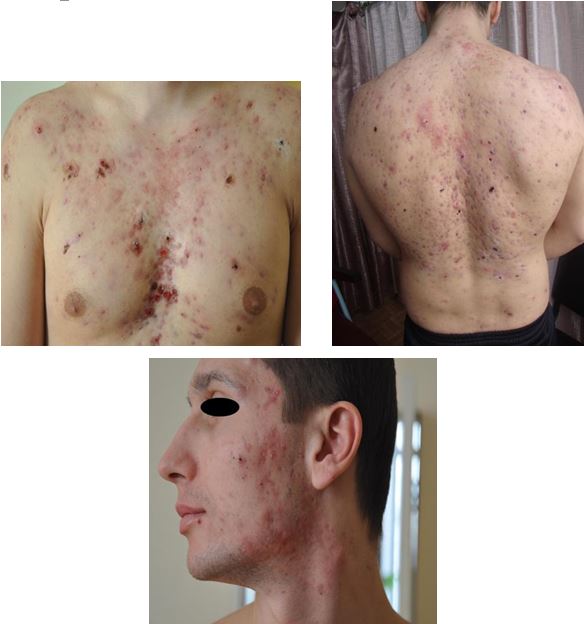
Рисунок 3.5 – Пацієнт С.22 роки, в анамнезі прийом спортивних добавок.
До терапії. Фото та динаміка процесу саногенезу при лікуванні
в розділі 4.
Клінічний випадок № 6. Пацієнт Н., 20 років. Звернувся зі скаргами на висип. В анамнезі прийом спортивних добавок близько 6 місяців. Пацієнт відзначає, що висип дебютував у пубертатному віці, але значне посилення висипу він помітив через 2 місяці після початку застосування спортивних добавок. При огляді звертала на себе увагу множинна і незліченна кількість відкритих і закритих комедонів на шкірі обличчя, вушних раковин, шиї, верхнього плечового пояса, тулуба, інфільтрати, глибокі рубці постакне і депігментовані макули з лущенням по краю (рис. 3.6).
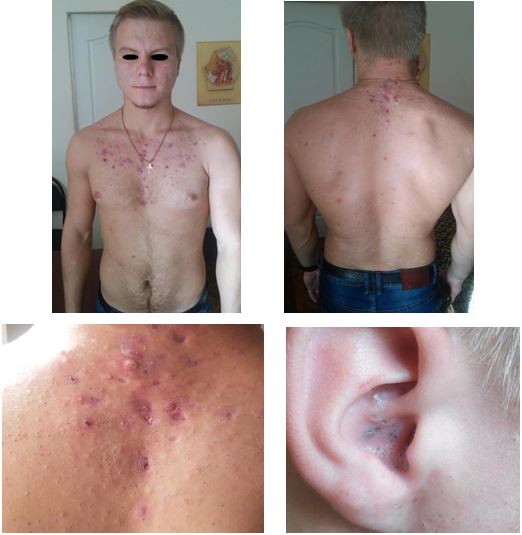
Рисунок 3.6 – Пацієнт Н., 20 років, в анамнезі прийом спортивних
добавок. Звертає на себе увагу наявність комедонів навіть
на внутрішній поверхні вушних раковин.
Діагноз: акне тяжкого ступеня, індуковане прийомом спортивних добавок. Висівковий лишай. Від лікування відмовився за сімейними обставинами. Були надані рекомендації щодо відміни «спортивних» добавок.
Аналізуючи дані анамнезу за зверненнями встановлено, що на прийом до дерматолога вперше прийшли 56 (39,4 %) пацієнтів. До цього вони займалися самолікуванням або відвідували косметологів. Косметолога відвідували 67 (79,7 %) жінок і 23 (39,6 %) чоловіків. Серед процедур, які вони вказали, практично всім проводилися гігієнічні чистки (механічні, апаратні), курси хімічних пілінгів. Три пацієнтки отримали курс ін’єкційної мезотерапії при папуло-пустульозній формі акне – без ефекту, вони ж проходили курс лазерного лікування акне і відзначали посилення висипу. Серед пацієнток жіночої статі відзначалися екскорійоване акне у 16 пацієнток, 2 пацієнтки мали «механічні» акне, які пов’язували з проходженням курсу масажу в салонах або на спа-курортах.
Клінічний випадок №7. Пацієнтка Г., 31 рік. Звернулася зі скаргами на висип на шкірі плечей і грудей. З анамнезу відомо, що вона відвідувала масажний кабінет і пройшла курс масажу 10 процедур. Масаж проводився при нанесенні на шкіру масажної олії. Висип почав прогресувати через місяць після закінчення курсу масажу. Пацієнтка зверталася за допомогою. Їй було призначено в поліклініці за місцем проживання системну антибактеріальну терапію і «левомеколь» зовнішньо. Позитивної динаміки не спостерігалося і пацієнтка звернулася за допомогою до ДУ «Інститут дерматології та венерології НАМН України». При огляді дерматоз мав поширений симетричний характер, локалізувався переважно на шкірі грудей, верхньої частини спини, верхньому плечовому поясі. Висип представлено великими папуло-пустулами на гіперемійованому тлі, відкритими і закритими комедонами, рубцевими елементами (рис. 3.7).
Поставлено діагноз: Акне тяжкого ступеня.
Патологічних змін при загальноклінічному обстеженні не виявлено.
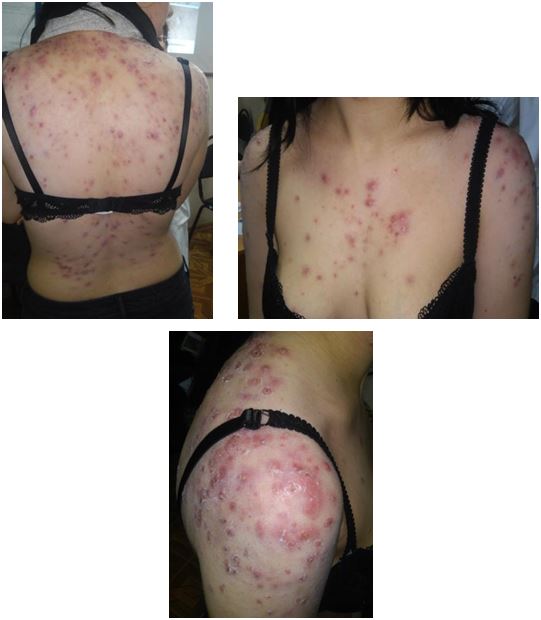
Рисунок 3.7 – Пацієнтка Г., 31 рік, з акне тяжкого ступеня. До лікування.
В анамнезі проходження курсу масажу із застосуванням масажної олії.
Фото після лікування – в розділі лікування.
З даних анамнезу відомо, що 65 пацієнтів раніше отримували системну терапію у вигляді антимікробних препаратів (метронідазолу, доксицикліну, азитроміцину). Також на прийом звернулася пацієнтка, яка протягом 2 років приймала доксициклін у дозі 50 мг на добу. Системні ретиноїди в анамнезі отримували 6 пацієнтів, з них 5 чоловіків і 1 жінка, при цьому лікування було недостатньо тривалим (1–3 місяці).
Клінічний випадок № 8. Пацієнт З., 29 років, звернувся зі скаргами на висип на шкірі обличчя. З анамнезу відомо, що хворіє близько трьох років. Лікувався за місцем проживання: перший курс терапії отримав два роки тому: антибіотики, зовнішні антибактеріальні засоби. Ремісія після терапії тривала близько 4 місяців. Стан шкіри прогресивно погіршувався, пацієнт звернувся до іншого дерматолога, де йому було призначено системні ретиноїди. Рекомендований прийом ретиноїдів тривав два місяці в дозі 16 мг і 1 місяць в дозі 8 мг на добу. пацієнт зазначив поліпшення стану шкіри, але через місяць після закінчення прийому препаратів знову почав прогресувати висип. При огляді дерматоз мав локалізований симетричний характер. Розташований переважно на шкірі обличчя. Представлений крупними папуло-пустулами, інфільтратами, комедонами на гіперемійованому тлі, тканини шкіри обличчя набряклі (рис. 3.8).
Діагноз: акне тяжкого ступеня. Обстежено: патологічних змін і протипоказань до терапії системними ретиноїдами немає.
Особливість випадку в тому, що пацієнт отримував раніше патогенетичну терапію в недостатньому обсязі.
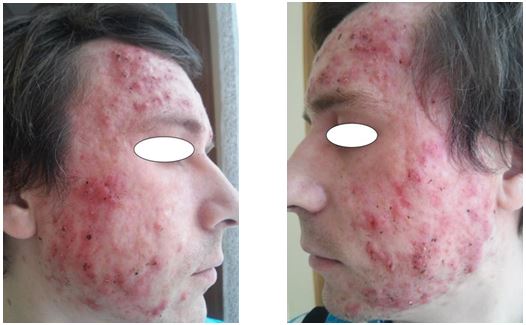
Рисунок 3.8 – Пацієнт З., 29 років, до лікування. В анамнезі недостатній прийом системних ретиноїдів, що обумовило швидку появу рецидиву.
Під наглядом перебував також пацієнт чоловічої статі з екскорійованими акне.
Клінічний випадок № 9. Пацієнт А., 18 років звернувся до ДУ «Інститут дерматології та венерології НАМН України» зі скаргами на висип на шкірі обличчя та тулуба. Відомо, що хворів близько року. Займався самолікуванням: за порадою друзів використовував примочки з борною кислотою і гарячі компреси. Зі слів хворого це полегшувало його стан і «розм’якшувало» кірки на обличчі. При огляді звертала на себе увагу застійна гіперемія на обличчі. Дерматоз мав поширений симетричний характер. Представлений папуло-пустулами різного діаметру, інфільтратами з тенденцією до злиття на обличчі на яскраво гіперемійованому, місцями лівідному, тлі, гнійно-геморагічні кірки, рубцеві зміни – постакне. Висип на тулубі був представлений великими папуло-пустулами. Відзначалася множина відкритих і закритих комедонів (рис. 3.9).
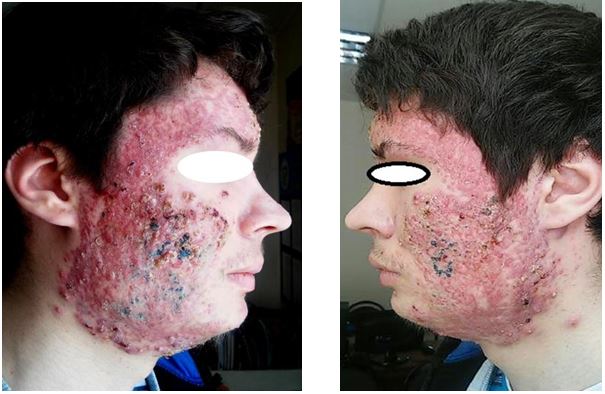
Рисунок 3.9 – Пацієнт з акне тяжкого ступеня – до лікування. Фото після лікування – в розділі лікування.
Діагноз: акне тяжкого ступеня. При обстеженні патологічних відхилень не виявлено.
Особливість клінічного випадку в тому, що пацієнт самолікуванням значно погіршував стан шкіри та провокував ще більше загострення.
Клінічний випадок № 10. Пацієнтка Н., 33 років, звернулася за допомогою до ДУ «Інститут дерматології та венерології НАМН України» зі скаргами на висип на шкірі обличчя. З анамнезу відомо, що захворювання дебютувало два роки тому на тлі стресу (зміни в особистому житті: розлучення). Пацієнтка зверталася за допомогою до дерматолога, де їй був призначений доксициклін по 100 мг на добу з подальшим переходом на 50 мг на добу, тривало. На момент звернення вона отримувала доксициклін два роки. У цей період поліпшення стану шкіри не було, і пацієнтка зверталася за допомогою до терапевтів, де їй було рекомендовано курс «очищення печінки», антипаразитарна терапія. Неодноразово зверталася за допомогою до косметологів, де був проведений курс хімічних пілінгів і курс мезотерапії коктейлями, склад яких вона не може вказати. У процесі двох років звернень вона зазначила, що через посилення висипу вона стала відчувати дискомфорт у спілкуванні з людьми і так як її робота була в сфері обслуговування (індустрія краси), вона змушена була від неї відмовитися. У результаті двох років пошуків вирішення своєї проблеми вона відзначила значне погіршення свого психоемоційного стану та стану шкіри. На момент огляду: дерматоз мав локалізований симетричний характер, відзначався набряк тканин обличчя, виражена застійна гіперемія, множинні інфільтрати і папуло-пустули з тенденцією до злиття, інфільтрати, відкриті комедони в себозалежних зонах, місцями ділянки сухості, спричинені самостійним застосуванням спиртового розчину саліцилової кислоти (рис. 3.10). При спілкуванні психоемоційно лабільна, постійно плаче, висловлює думки суїцидальної спрямованості, демонструє високий рівень тривожності.
При опитуванні зазначила нерегулярність менструального циклу. Була обстежена в ендокринолога-гінеколога. Поставлено діагноз: гіперпролактинемія, гіперандрогенія. Рекомендовано оральні контрацептиви тривалістю 3-6 місяців. При загальноклінічному обстеженні патологічних змін не виявлено.
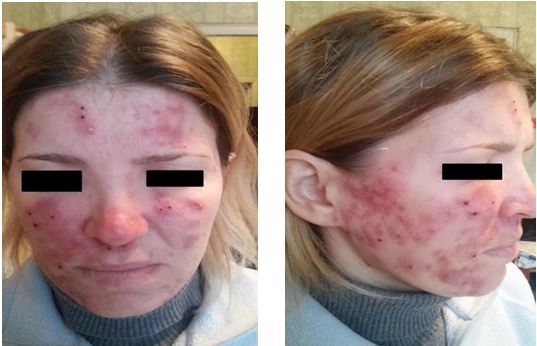
Рисунок 3.10 – Пацієнтка Н., 33 роки, в анамнезі довготривалий прийом доксицикліну. Фото до початку терапії.
Зовнішня терапія акне в анамнезі у 48 пацієнтів містила антибіотики або комбінацію антибіотиків і кератолітиків у вигляді бензоїлпероксиду або азелаїнової кислоти. Отримання топічних ретиноїдів у анамнезі відзначили 17 осіб, 14 з яких вказали на дискомфорт у період застосування і недостатній ефект від очікуваного. Рецидиви, враховуючи те, що акне є хронічним рецидивуючим дерматозом спостерігалися у всіх 76 пацієнтів, які раніше отримували терапію. У середньому цей показник становив 2-3 місяці ремісії.
При зборі даних про спадковість 47 осіб відзначили, що мають спадковий фактор по лінії батька, а 21 – по лінії матері або обох батьків.
Клінічний випадок № 11. На прийом звернулася мама з донькою 8 років. Скарги при зверненні: висип на обличчі. З анамнезу відомо, що перші висипи стали з’являтися близько року тому на шкірі носа. Висип прогресував і вони вирішили звернутися по допомогу. При опитуванні було з’ясовано, що батько дівчинки має жирну шкіру, множинні елементи постакне у вигляді рубців і періодично страждає від себореї та лупи. Локальний статус: висип мав поширений характер. Був представлений відкритими і закритими комедонами в себозалежних зонах на шкірі обличчя і тулуба. На шкірі підборіддя, лоба і шкірі спини в міжлопатковій зоні кілька пустул (рис. 3.11). Устя сальноволосяних фолікулів розширені, місцями деформовані. Зі слів матері супутньої патології у дівчинки немає, але вона дуже емоційно сприймає дефекти своєї зовнішності.
Був поставлений діагноз: акне легкого ступеня тяжкості, комедональна форма.
Рекомендовано обстеження у ендокринолога та педіатра, зовнішня терапія.
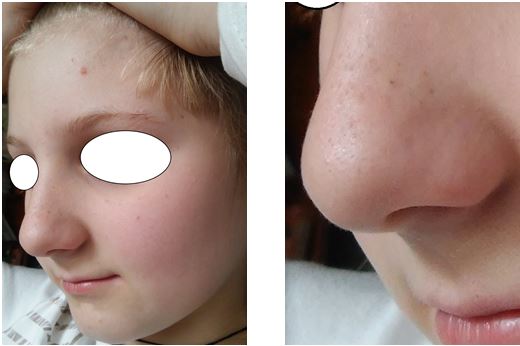
Рисунок 3.11 – Пацієнтка Н., 8 років. Фото до початку терапії.
З рідкісних форм акне спостерігався пацієнт 50 років із синдромом Фавра-Ракушо, який звернувся зі скаргами на висип на шкірі обличчя.
Клінічний випадок № 12. Хворий С., 50 років. Дебют висипу пацієнт помітив близько 10 років тому. Звертався за медичною допомогою неодноразово: проводилась екстракція комедонів, медикаментозного лікування не отримував. З анамнезу відомо, що пацієнт відзначав періоди тривалої інсоляції (працював рибалкою). Супутня патологія: гіпертонічна хвороба 2 ступеня, цукровий діабет, ожиріння. При огляді: дерматоз мав локалізований характер, розташований на шкірі обличчя в лобових і скроневих ділянках, мав симетричне розташування. Елементи представлені рельєфними зонами гіперпігментації, вузликовими утвореннями, місцями з жовтуватою поверхнею, множинними відкритими і закритими комедонами. Звертає на себе увагу виражена складчастість шкіри в осередках висипу, гіперплазія сальних залоз. Йому було запропоновано різні види терапії і з огляду на те, що цей дерматоз відносять і до акнеформних нозологій і до преканкрозів, був обраний метод лазерної корекції.
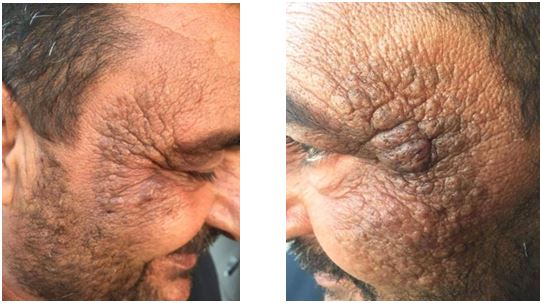
Рисунок 3.12 – Пацієнт з синдромом Фавра-Ракушо.
* * *
З огляду на епідеміологічні та клінічні дані, а також анамнез пацієнтів, які увійшли до дослідження, можна відзначити, що акне є хронічним, часто рецидивуючим дерматозом, на виникнення та перебіг якого можуть впливати різні чинники: ендокринна патологія, захворювання шлунково-кишкового тракту, ЛОР-органів та інші, у тому числі погодні фактори, самолікування. Статистика рецидивів, неуспішності або незадоволеності пацієнтом попередньою терапією передбачає пошук нових терапевтичних схем, які дозволять максимально підвищити якість і ефективність лікування пацієнтів з акне.
Матеріали цього розділу висвітлено у наступних публікаціях:
1. Бронова И.М. Акне, индуцированное приемом анаболических стероидов. Дерматологія та венерологія. 2015. № 1 (67). С. 89–92 [27].
2. Кутасевич Я.Ф., Бронова И.М. Базовая и адъювантная терапия при тяжелых формах акне. Український журнал дерматології, венерології, косметології. 2015. № 2 (57). С. 74–79 [103].
3. Бронова И.М., Хатем С.М. Редкие нозологии: клинический случай синдрома Фавра-Ракушо. Дерматологія та венерологія. 2017. № 2 (76). С. 53–55 [34].
4. Коморбидная патология у группы пациентов со средней степенью тяжести акне / Я.Ф. Кутасевич, И.А. Олейник, И.А. Маштакова, В.Ю. Мангушева, И.М. Бронова. Матеріали Всеукраїнської наук.-практ. конф. за участю міжнародних спеціалістів «Сучасні технології в рішенні організаційних, епідеміологічних, клінічних та діагностичних задач дерматовенерології», яка присвячена 80-річчю кафедри дерматовенерології Донецького національного медичного університету ім. М. Горького, 13 червня 2014 р., м. Донецьк. Журнал дерматовенерології та косметології ім. М. О. Торсуєва. 2014. № 1–2 (32). С. 133 [90].
5. Бронова І.М. Вплив ендокринологічних та психологічних чинників на епідеміологію акне у жінок. Збірник робіт за матеріалами науково-практичної конференції «Дерматовенерологія в розробках молодих науковців», 19-20 листопада 2015 року, м. Київ. Дерматовенерологія. Косметологія і сексопатологія. 2015. № 3–4. С. 108 [28].
6. Бронова І.М. Особливості загострень акне у пацієнтів, що отримували різні види патогенетичної терапії. V Ювілейний міжнародний медичний конгрес «Впровадження сучасних досягнень медичної науки у практику охорони здоров’я» : Матеріали конгресу, м. Київ, 19–21 квітня 2016 р. К., 2016. С. 84 [30].
7. Кутасевич Я.Ф., Бронова И.М. Гендерные особенности течения акне. Научные труды первой научно-практической международной конференции Ассоциации дерматовенерологов Армении «Ереванские дерматовенерологические чтения» (Ереван, 2015). Научно-медицинский журнал. 2015. № 10. С. 94 [105].
